Clear Sky Science · de
Das onkogene Fusionsprotein CCDC6-RET ist eine duale ATP- und ADP‑abhängige Kinase
Warum diese Krebsstudie wichtig ist
Krebsarten der Lunge und der Schilddrüse werden oft von fehlfunktionierenden Versionen von Zellkommunikationsproteinen, den Kinasen, angetrieben. Eine solche fehlerhafte Variante, das CCDC6‑RET‑Fusionsprotein, tritt häufig beim papillären Schilddrüsenkarzinom und in einigen Lungenkrebserkrankungen auf, besonders nach Strahlenexposition. Diese Studie zeigt, wie dieses Fusionsprotein sich selbst einschaltet und warum es ungewöhnlich gut an die gestresste, energiearme Umgebung in Tumoren angepasst sein könnte, und eröffnet damit neue Ansatzpunkte für gezielte Therapien.
Eine genetische Mischung, die Tumoren nährt
In gesunden Zellen sitzt das RET‑Protein in der Zellmembran und vermittelt Wachstumssignale. In vielen Schilddrüsenkarzinomen und in einer Untergruppe von Lungenkrebsen brechen DNA‑Stränge und verbinden sich an falschen Stellen neu, wodurch ein Hybridgen entsteht, das Teile des CCDC6‑Proteins mit dem aktiven Teil von RET verknüpft. Das Ergebnis, CCDC6‑RET genannt, ist ein eigenständiger Signalgeber, der keine normalen externen Signale mehr benötigt. Die Autor:innen stellten dieses Fusionsprotein in großen Mengen in Insektenzellen her und zeigten, dass es in Lösung sehr stabile Paare, sogenannte Dimere, bildet. Diese Dimere waren hochaktiv, phosphorylierten sich an zahlreichen Stellen selbst und reagierten stark auf bekannte RET‑Blocker, was bestätigt, dass das im Labor hergestellte Protein sich wie sein tumorförderndes Gegenstück verhält.
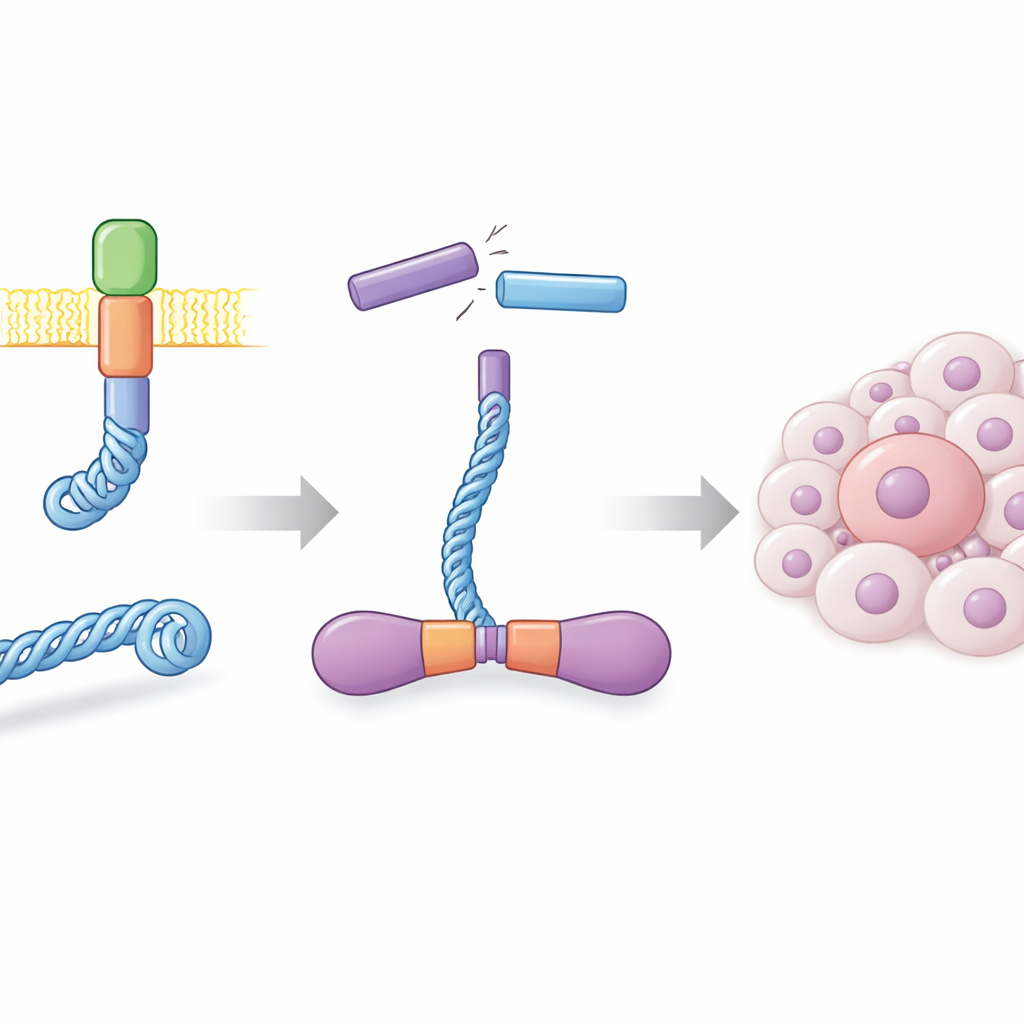
Eine Kinase, die mit zwei Treibstoffen läuft
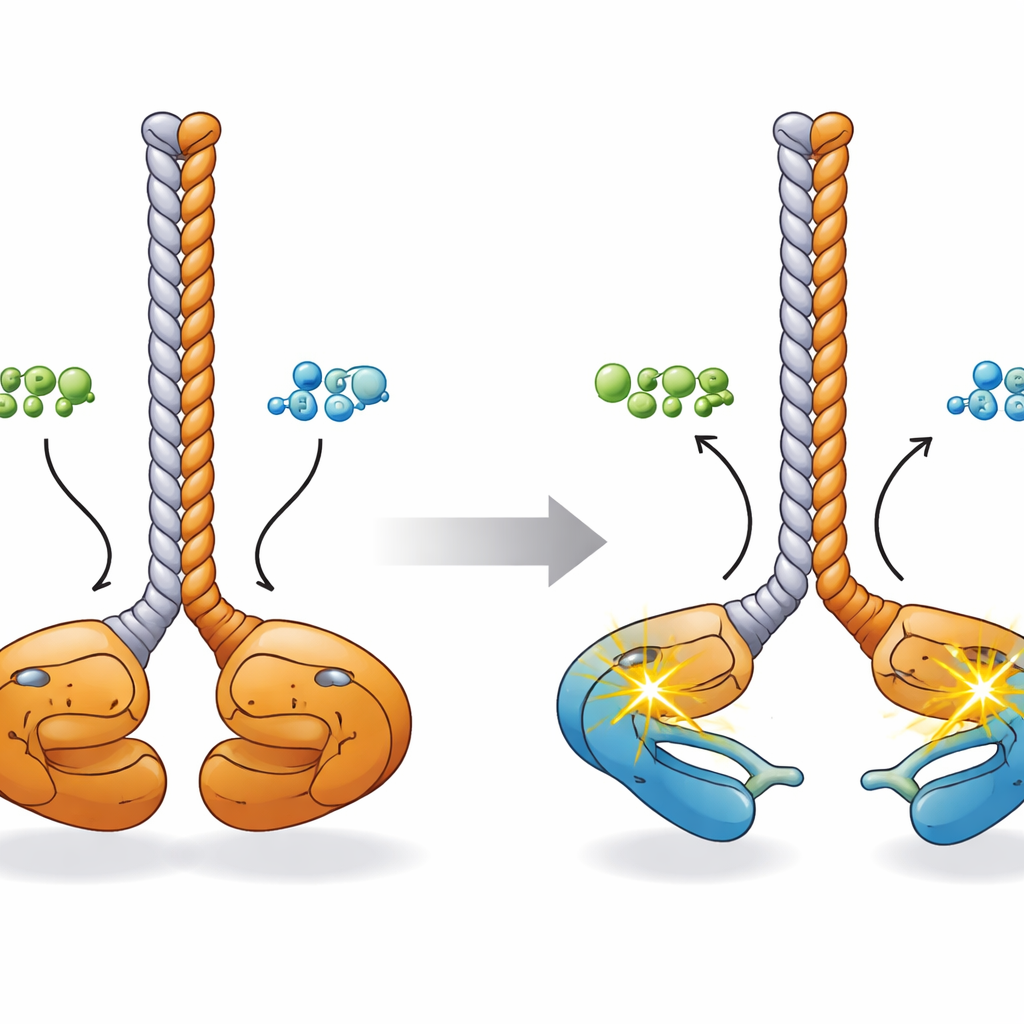
Die meisten Kinasen verwenden ATP, die primäre Energieeinheit der Zelle, als Phosphatquelle für ihre Reaktionen. Als die Autor:innen die Aktivität von CCDC6‑RET mit biochemischen Tests und zeitaufgelöster Massenspektrometrie analysierten, entdeckten sie Überraschendes: Die Phosphorylierung des Proteins nahm nicht nur mit ATP, sondern auch mit ADP zu, dem energieärmeren Produkt, das nach Verbrauch von ATP übrigbleibt. Folgeexperimente zeigten, dass CCDC6‑RET an beide Nukleotide bindet und entweder als Phosphatspender nutzen kann, wobei ATP schnellere Reaktionen ermöglicht. Bei moderaten ADP‑Spiegeln bleibt die Fusion aktiv, sehr hohe ADP‑Konzentrationen beeinträchtigen jedoch die ATP‑getriebene Aktivität, was darauf hindeutet, dass ADP die Kinase je nach Menge sowohl antreiben als auch regulieren kann.
Fein abgestimmte Schalter an der Proteinoberfläche
Das Team kartierte anschließend genau, wo sich CCDC6‑RET selbst phosphoryliert. Sie fanden mehrere Stellen nicht nur im katalytischen Kern von RET, sondern auch im CCDC6‑Abschnitt, darunter zuvor unbekannte Positionen. Zwei benachbarte Tyrosine in einem flexiblen Segment, der sogenannten Aktivierungsschleife, spielten unterschiedliche Rollen. Eine Position (Tyr 900) scheint für das richtige Falten und die Stabilität der Fusionsproteins entscheidend zu sein, während die andere (Tyr 905) für die effiziente Phosphorylierung anderer Proteine wesentlich ist. Eine Mutation an Tyr 905 beeinträchtigte größtenteils nicht die Fähigkeit des Proteins zur Selbstmodifikation, schwächte jedoch seine Fähigkeit, ein zugegebenes Peptidsubstrat zu phosphorylieren. Das zeigt, dass »Selbstaktivierung« und »Signalisierung nach außen« teilweise getrennt gesteuert werden. Diese differenzierte Kontrolle könnte dem Fusionsprotein helfen, dauerhaft aktiv zu bleiben, ohne seine strukturelle Integrität zu verlieren.
Die beweglichen Teile des Proteins in 3D sichtbar machen
Um zu verstehen, wie diese chemischen Veränderungen mit der Struktur zusammenhängen, setzten die Forschenden ein dreidimensionales Bild aus prädiktiven KI‑Modellen, Elektronenmikroskopie, Kleinwinkel‑Röntgenstreuung und Quervernetzungs‑Massenspektrometrie zusammen. Im Ruhezustand nimmt das CCDC6‑RET‑Dimer eine »face‑to‑face«‑Konfiguration ein: Die beiden Kinasedomänen liegen nahe beieinander an der Basis eines gemeinsamen, aus CCDC6‑Segmenten gebildeten Coiled‑Coil‑Schafts, wobei sich ihre Aktivierungsschleifen berühren. Beim Binden von ATP oder ADP schwenken diese Kinaselappen auseinander wie die Spitzen eines Chopsticks. Computersimulationen legen nahe, dass in diesem offeneren Zustand jede Kinase in der Lage ist, ihre eigene Aktivierungsschleife »in cis« zu phosphorylieren und so das Dimer für schnelle Signalübertragung an andere zelluläre Ziele vorzubereiten.
Was das für Krebs und zukünftige Therapien bedeutet
Tumorzellen leben oft an der Grenze einer Energiekrise, mit geringerem ATP‑ und erhöhtem ADP‑Spiegel im Vergleich zu gesunden Zellen. Eine Fusionskinase, die sowohl mit ATP als auch mit ADP arbeiten kann — und deren Substratpräferenz sich unter ADP‑reichen Bedingungen sogar verschieben kann — könnte daher in der rauen Mikroumgebung solider Tumoren einen Überlebensvorteil besitzen. Indem diese Arbeit aufklärt, wie CCDC6‑RET aufgebaut ist, wie es dimerisiert, wie es beide Formen zellulären Treibstoffs nutzt und welche Phosphorylierungsstellen am wichtigsten sind, liefert sie einen detaillierten Bauplan für die Entwicklung neuer Wirkstoffe. Solche Medikamente könnten nicht nur das aktive Zentrum blockieren, sondern auch darauf abzielen, das Dimer zu destabilisieren, das Umschalten der Aktivierungsschleife zu stören oder die ungewöhnliche Abhängigkeit des Enzyms vom Energiehaushalt der Zelle auszunutzen.
Zitation: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Schlüsselwörter: RET‑Fusion, papilläres Schilddrüsenkarzinom, Lungenadenokarzinom, Aktivierung von Proteinkinasen, ATP‑ und ADP‑Stoffwechsel