Clear Sky Science · pt
A proteína de fusão oncogênica CCDC6-RET é uma quinase dependente tanto de ATP quanto de ADP
Por que este estudo sobre câncer importa
Os cânceres de pulmão e tireoide frequentemente são impulsionados por versões defeituosas de proteínas de comunicação celular chamadas quinases. Uma dessas versões alteradas, a proteína de fusão CCDC6-RET, aparece com frequência no câncer papilífero da tireoide e em alguns cânceres de pulmão, especialmente após exposição à radiação. Este estudo revela como essa proteína de fusão se liga e por que pode estar particularmente adaptada ao ambiente tumoral estressado e pobre em energia, abrindo novas abordagens para tratamentos direcionados.
Uma mistura genética que alimenta tumores
Em células saudáveis, a proteína RET fica na membrana celular e ajuda a transmitir sinais de crescimento. Em muitos cânceres de tireoide, e em um subconjunto de cânceres de pulmão, quebras e reentrâncias no DNA acontecem em locais errados, criando um gene híbrido que funde parte da proteína CCDC6 à região efetora do RET. O resultado, chamado CCDC6-RET, é um motor de sinalização independente que não depende mais de sinais externos normais. Os autores produziram essa proteína de fusão em grande quantidade usando células de inseto e mostraram que ela forma pares muito estáveis, ou dímeros, em solução. Esses dímeros eram altamente ativos, adicionando grupos fosfato a si mesmos em muitos sítios e respondendo fortemente a fármacos conhecidos que bloqueiam RET, confirmando que a proteína produzida em laboratório se comporta como sua contraparte que dirige o câncer.
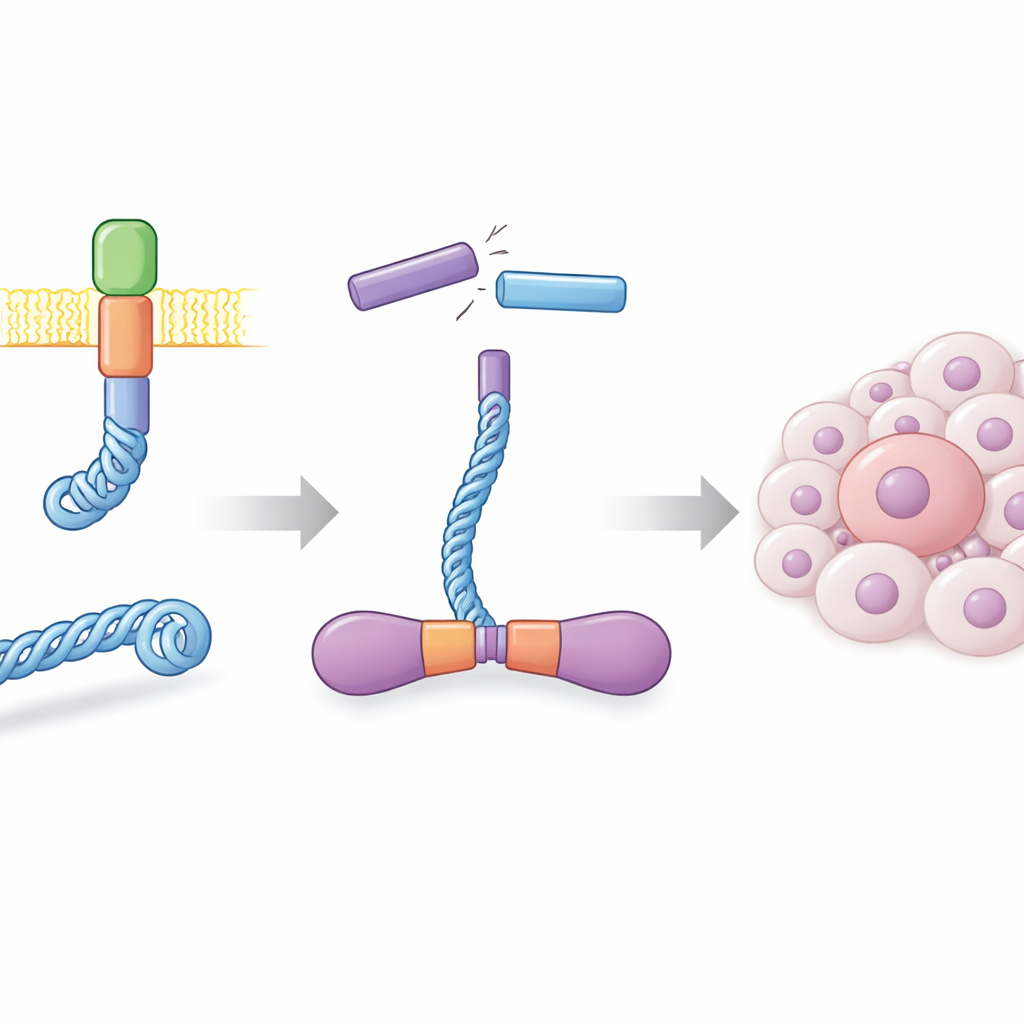
Uma quinase que roda com dois tipos de combustível
A maioria das quinases usa ATP, a moeda energética primária da célula, como fonte de fosfato para suas reações. Quando os autores analisaram a atividade da CCDC6-RET usando ensaios bioquímicos e espectrometria de massa com resolução temporal, notaram algo surpreendente: a fosforilação da proteína aumentava não apenas com ATP, mas também com ADP, o produto de menor energia que sobra após o consumo de ATP. Experimentos complementares mostraram que a CCDC6-RET se liga a ambos os nucleotídeos e pode usar qualquer um como doador de fosfato, embora funcione mais rápido com ATP. Em níveis moderados de ADP a fusão permanece ativa, mas concentrações muito altas de ADP começam a interferir na atividade dependente de ATP, sugerindo que o ADP pode tanto alimentar quanto regular essa enzima cancerígena dependendo de sua abundância.
Chaves de controle refinadas na superfície da proteína
A equipe mapeou exatamente onde a CCDC6-RET se fosforila. Eles encontraram múltiplos sítios não apenas no núcleo catalítico do RET, mas também na porção CCDC6, incluindo sítios até então desconhecidos. Dois tirosinos vizinhos em um segmento flexível chamado laço de ativação desempenharam papéis distintos. Um sítio (Tyr 900) parece crucial para o dobramento e estabilidade adequados da proteína de fusão, enquanto o outro (Tyr 905) é essencial para a fosforilação eficiente de outras proteínas. Mutar Tyr 905 poupou em grande parte a capacidade da proteína de se modificar, mas prejudicou sua habilidade de atuar sobre um peptídeo substrato adicionado, revelando que “autoativação” e “sinalização para fora” são controladas de forma parcialmente separada. Esse controle sutil pode ajudar a proteína de fusão a permanecer ativada sem perder integridade estrutural.
Revelando as partes móveis da proteína em 3D
Para entender como essas mudanças químicas se relacionam com a forma, os pesquisadores montaram uma imagem tridimensional usando modelos preditivos de inteligência artificial, microscopia eletrônica, espalhamento de raios X em ângulo pequeno e espectrometria de massa com cross-linking. Em seu estado de repouso, o dímero CCDC6-RET adota uma configuração “face a face”: os dois domínios quinase ficam próximos na base de um eixo em coiled-coil compartilhado formado pelos segmentos CCDC6, com seus laços de ativação em contato. Ao se ligar ATP ou ADP, esses lóbulos quinase se abrem como as pontas de um par de hashis. Simulações computacionais sugerem que, nesse estado mais aberto, cada quinase pode alcançar e fosforilar seu próprio laço de ativação (“in cis”), preparando o dímero para sinalização rápida a outros alvos celulares.
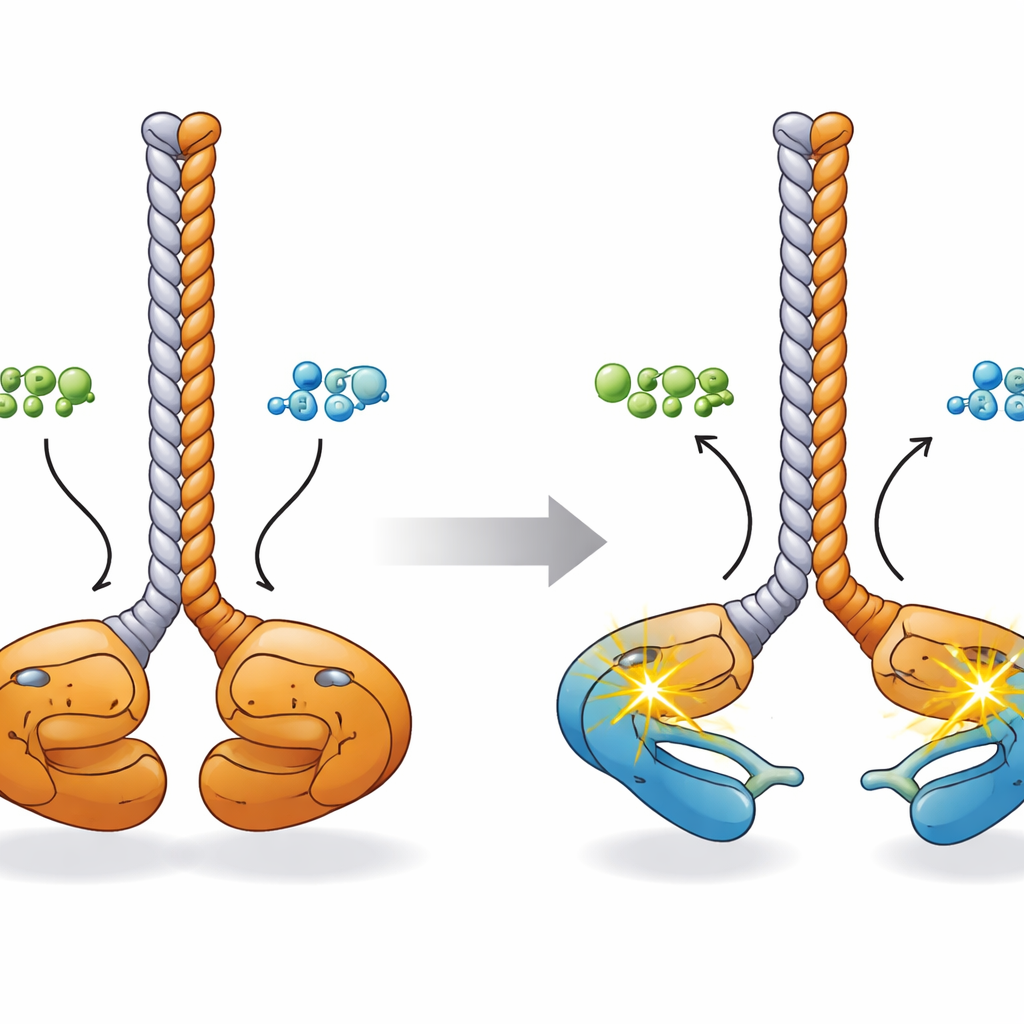
O que isso significa para o câncer e terapias futuras
As células tumorais frequentemente vivem à beira de uma crise energética, com níveis de ATP mais baixos e ADP mais altos do que células saudáveis. Uma quinase de fusão que pode funcionar com ATP ou ADP — e até mudar sua preferência de alvo para diferentes aminoácidos em condições ricas em ADP — pode, portanto, ter vantagem de sobrevivência nos microambientes hostis de tumores sólidos. Ao esclarecer como a CCDC6-RET é construída, como dimeriza, como usa ambas as formas de combustível celular e quais sítios de fosforilação são mais importantes, este trabalho oferece um roteiro detalhado para projetar drogas de nova geração. Tais fármacos poderiam visar não apenas o sítio ativo, mas também destruir o dímero, interferir na troca do laço de ativação ou explorar a dependência incomum da enzima pelo balanço energético da célula.
Citação: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Palavras-chave: fusão RET, câncer papilífero da tireoide, adenocarcinoma de pulmão, ativação de quinase proteica, metabolismo ATP ADP