Clear Sky Science · ar
بروتين الاندماج المسبب للسرطان CCDC6-RET هو كيناز يعتمد على كل من ATP وADP
لماذا تهم هذه الدراسة حول السرطان
غالبًا ما تكون سرطانات الرئة والغدة الدرقية مدفوعة بنُسخ معطوبة من بروتينات تواصل خلوية تُسمى الكينازات. أحد هذه النسخ المعطوبة، بروتين الاندماج CCDC6-RET، يظهر بشكل متكرر في سرطان الغدة الدرقية الحليمي وبعض سرطانات الرئة، خصوصًا بعد التعرض للإشعاع. تكشف هذه الدراسة كيف يُشغل هذا البروتين المُندمج نفسه ولماذا قد يكون مُتكيفًا بشكل غير معتاد مع البيئة الداخلية للورم الفقيرة بالطاقة والمجهدة، مما يفتح زوايا جديدة للعلاج المستهدف.
خليط جيني يغذي الأورام
في الخلايا السليمة، يوجد بروتين RET في غشاء الخلية ويساعد على نقل إشارات النمو. في العديد من سرطانات الغدة الدرقية، وفي شريحة من سرطانات الرئة، تحدث انقطاعات في الحمض النووي وإعادة وصل في أماكن خاطئة، مما يخلق جينًا هجينًا يدمج جزءًا من بروتين CCDC6 مع الطرف الفعّال من RET. النتيجة، المسماة CCDC6-RET، هي محرك إشارة قائم بذاته لم يعد بحاجة إلى إشارات خارجية طبيعية. أنتج الباحثون هذا البروتين المُندمج بكميات كبيرة باستخدام خلايا حشرية وأظهروا أنه يشكل أزواجًا مستقرة جدًا، أو ديمرات، في المحلول. كانت هذه الديمرات نشطة للغاية، تضيف مجموعات فوسفات لنفسها في مواقع عديدة وتستجيب بقوة لأدوية معروفة تثبط RET، مؤكدة أن البروتين المصنع في المختبر يتصرف مثل نظيره المُحفز للسرطان.
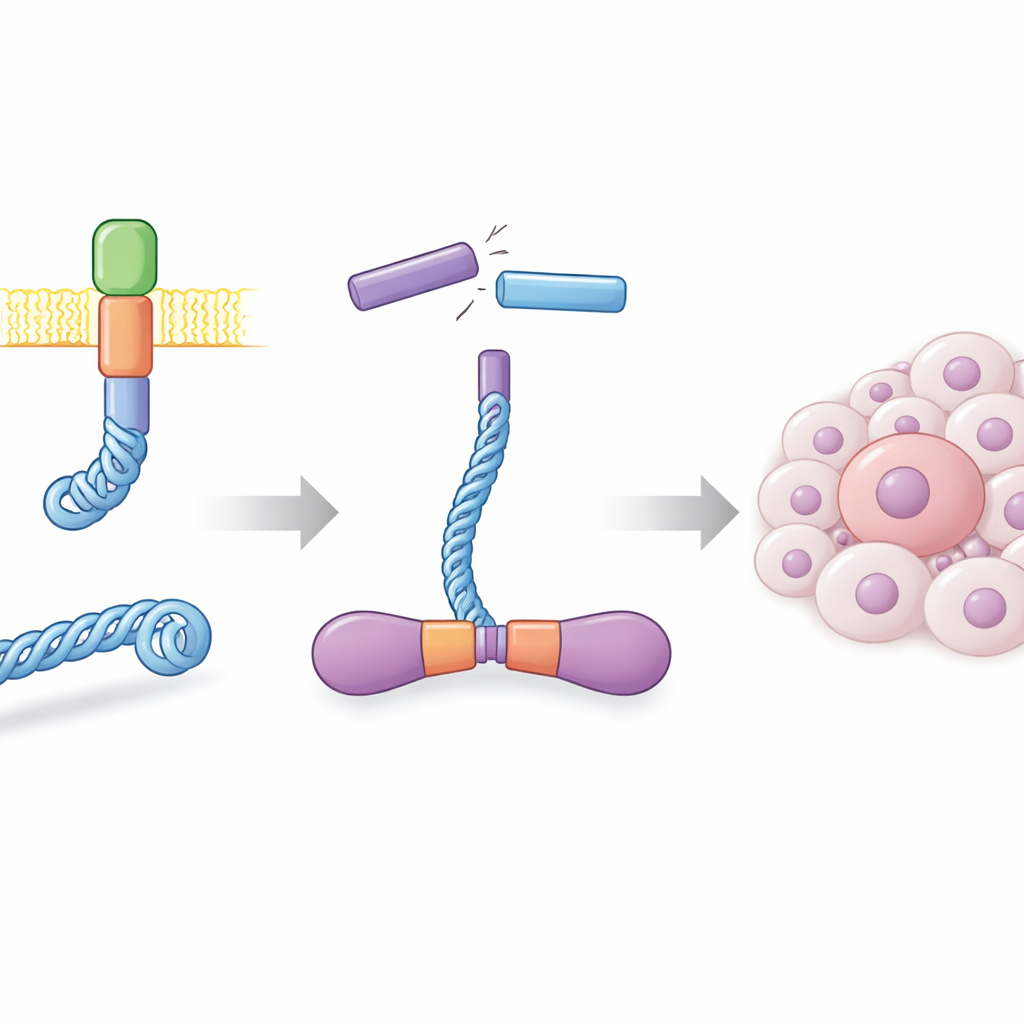
كيناز يعمل بوقودين
تستخدم معظم الكينازات ATP، العملة الأساسية للطاقة في الخلية، كمصدر للفوسفات في تفاعلاتها. عندما حلل الباحثون نشاط CCDC6-RET باستخدام اختبارات بيوكيميائية وطيفية زمنية الدقة، لاحظوا أمرًا مفاجئًا: ازداد فسفرة البروتين ليس فقط بوجود ATP بل أيضًا بوجود ADP، المنتج الأقل طاقة بعد استهلاك ATP. أظهرت تجارب لاحقة أن CCDC6-RET يربط كلا النيوكليوتيدين ويمكنه استخدام أي منهما كمانح للفوسفات، رغم أنه يعمل أسرع مع ATP. عند مستويات متوسطة من ADP يبقى الاندماج نشطًا، لكن تراكيز ADP العالية جدًا تبدأ بالتداخل مع النشاط المعتمد على ATP، مما يوحي بأن ADP يمكن أن يغذي وينظّم هذا الإنزيم السرطاني اعتمادًا على وفرة كل منهما.
مفاتيح تحكم مضبوطة على سطح البروتين
تابع الفريق خرائط مواقع فسفرة CCDC6-RET على نفسه بدقة. وجدوا مواقع متعددة ليس فقط في النواة الحفازة ل RET وإنما أيضًا في جزء CCDC6، بما في ذلك مواقع كانت غير معروفة سابقًا. لعبتا تيروسين متجاورتان في مقطع مرن يُسمى حلقة التنشيط أدوارًا مميزة. أحد المواقع (Tyr 900) يبدو أنه حاسم لطي البروتين واستقراره بشكل صحيح، بينما الآخر (Tyr 905) ضروري لفسفرة البروتينات الأخرى بكفاءة. أدت طفرة في Tyr 905 إلى إبقاء قدرة البروتين إلى حد كبير على تعديل نفسه مع إضعاف قدرته على العمل على ريبتيد ركيزة ببتيدية مضافة، كاشفةً أن «التنشيط الذاتي» و«الإشارة إلى الخارج» يتم التحكم فيهما بشكل منفصل إلى حد ما. قد يساعد هذا التحكم الدقيق البروتين المُندمج على البقاء نشطًا دون فقدان سلامته الهيكلية.
إظهار أجزاء البروتين المتحركة ثلاثية الأبعاد
لفهم كيف ترتبط هذه التغيرات الكيميائية بالشكل، جمع الباحثون صورة ثلاثية الأبعاد باستخدام نماذج تنبؤية بالذكاء الاصطناعي، الميكروسكوب الإلكتروني، تشتت أشعة إكس بزوايا صغيرة، وطيفية الكتلة بعد الربط المتقاطع. في حالته الراحة، يتبنى ديمر CCDC6-RET تكوينًا «وجهًا لوجه»: تجاور نطاقي الكيناز بالقرب من قاعدة جذع لولبي مشترك مُشكّل من مقاطع CCDC6، وتلامس حلقات التنشيط بعضها البعض. عند ربط ATP أو ADP، تتباعد فصوص الكيناز تلك مثل أطراف عيدان الأكل. تقترح المحاكاة الحاسوبية أنه في هذه الحالة الأكثر انفتاحًا يمكن لكل كيناز أن يصل ويفسفر حلقة التنشيط الخاصة به («in cis»)، مهيئًا الديمر لإطلاق إشارات سريعة نحو أهداف خلوية أخرى.
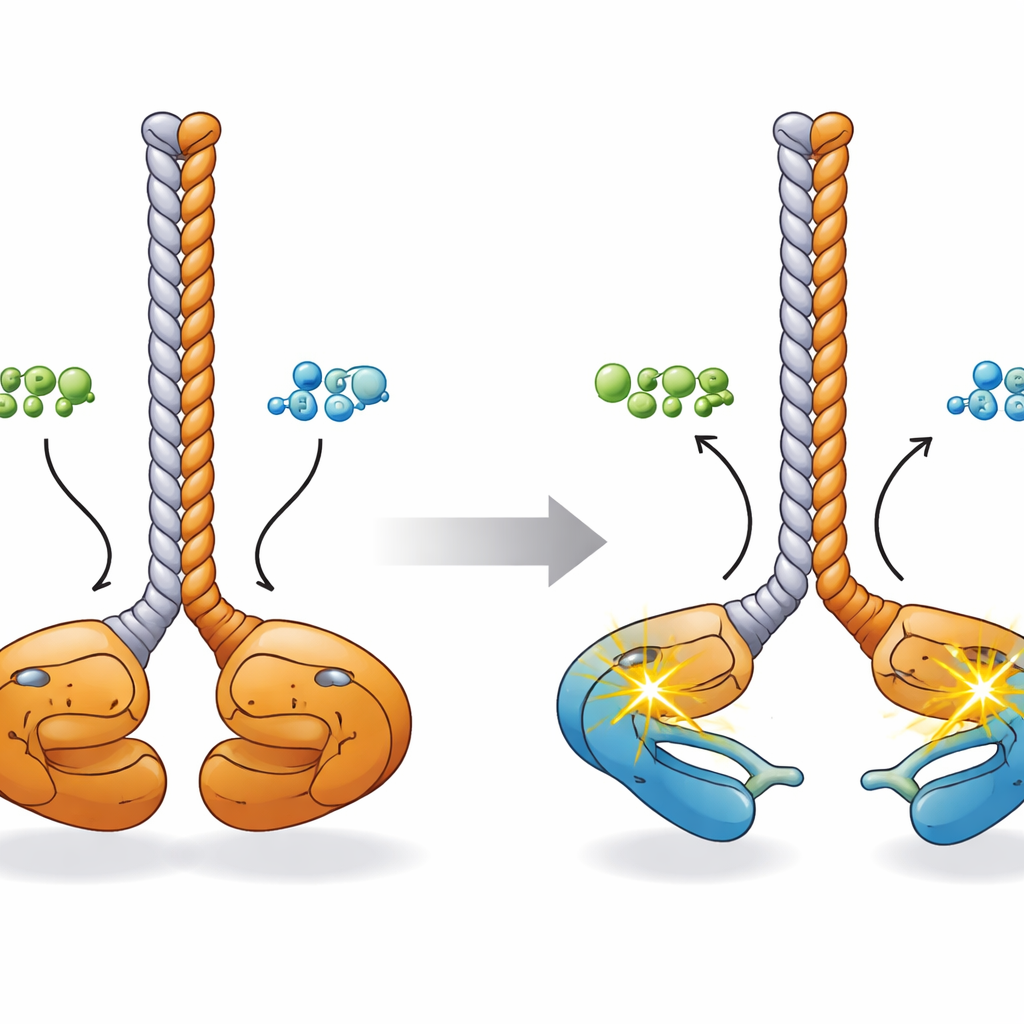
ما يعنيه هذا للسرطان والعلاجات المستقبلية
تعيش خلايا الورم غالبًا على حافة أزمة طاقة، بوجود ATP أقل وADP أعلى مقارنة بالخلايا السليمة. قد يمنح كيناز اندماجي قادرًا على العمل سواء مع ATP أو ADP—وحتى تحويل تفضيله تجاه أحماض أمينية مختلفة في ظل ظروف غنية بـADP—ميزة بقاء في البيئات الميكروية القاسية للأورام الصلبة. من خلال توضيح كيفية بناء CCDC6-RET، وكيف يتشكل إلى ديمر، وكيف يستخدم شكلَي وقود خلوية، وأي مواقع الفسفرة هي الأكثر أهمية، تقدم هذه الدراسة مخططًا تفصيليًا لتصميم أدوية الجيل القادم. يمكن أن تستهدف هذه الأدوية ليس فقط موقع النشاط، بل أيضًا تعطيل الديمر، أو التدخل في تبديل حلقة التنشيط، أو استغلال اعتماد الإنزيم غير الاعتيادي على توازن طاقة الخلية.
الاستشهاد: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
الكلمات المفتاحية: اندماج RET, سرطان الغدة الدرقية الحليمي, سرطان غدة الرئة الغدي, تنشيط كيناز البروتين, استقلاب ATP وADP