Clear Sky Science · fr
La protéine de fusion oncogénique CCDC6-RET est une kinase dépendante à la fois de l’ATP et de l’ADP
Pourquoi cette étude sur le cancer est importante
Les cancers du poumon et de la thyroïde sont souvent entraînés par des versions défaillantes de protéines de communication cellulaire appelées kinases. L’une de ces formes altérées, la protéine de fusion CCDC6-RET, apparaît fréquemment dans le cancer papillaire de la thyroïde et dans certains cancers du poumon, en particulier après exposition aux radiations. Cette étude révèle comment cette protéine de fusion s’active et pourquoi elle peut être particulièrement bien adaptée à l’environnement tumoral stressé et pauvre en énergie, ouvrant de nouvelles pistes pour des traitements ciblés.
Un mélange génétique qui alimente les tumeurs
Dans les cellules saines, la protéine RET est ancrée dans la membrane plasmique et contribue à relayer les signaux de croissance. Dans de nombreux cancers thyroïdiens, et dans une portion des cancers du poumon, des cassures et des recombinaisons de l’ADN créent un gène hybride qui fusionne une partie de la protéine CCDC6 avec l’extrémité fonctionnelle de RET. Le produit, appelé CCDC6-RET, fonctionne comme un moteur de signalisation autonome qui n’a plus besoin d’indices externes normaux. Les auteurs ont produit cette protéine de fusion en grande quantité dans des cellules d’insecte et ont montré qu’elle forme en solution des paires très stables, ou dimères. Ces dimères étaient fortement actifs, ajoutant des groupes phosphate sur eux-mêmes en de nombreux sites et répondant vigoureusement à des médicaments connus pour bloquer RET, confirmant que la protéine fabriquée en laboratoire se comporte comme son homologue impliqué dans le cancer.
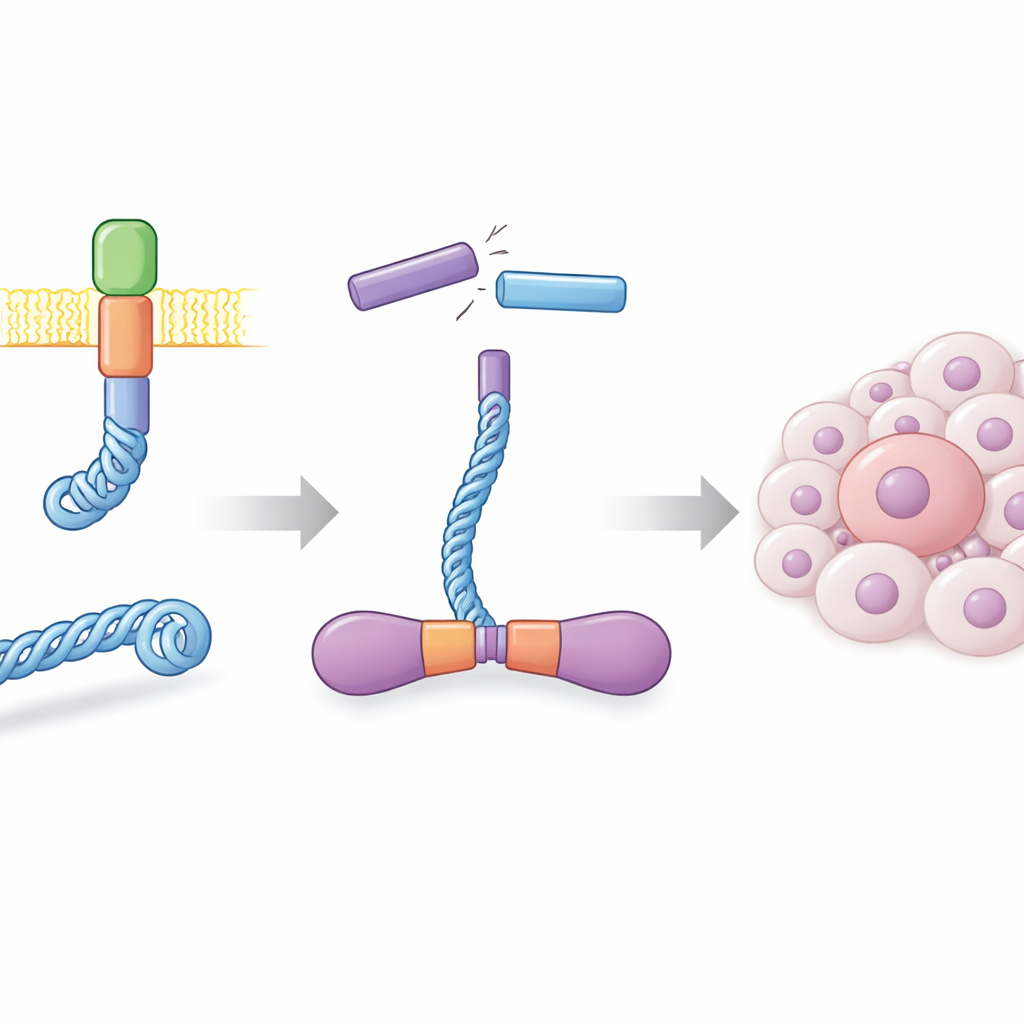
Une kinase qui fonctionne avec deux sortes de carburant
La plupart des kinases utilisent l’ATP, la principale monnaie énergétique de la cellule, comme source de phosphate pour leurs réactions. Lorsque les auteurs ont analysé l’activité de CCDC6-RET par des essais biochimiques et de la spectrométrie de masse résolue dans le temps, ils ont observé une surprise : la phosphorylation de la protéine augmentait non seulement en présence d’ATP mais aussi en présence d’ADP, le produit moins énergétique résultant de la dépense d’ATP. Des expériences supplémentaires ont montré que CCDC6-RET se lie aux deux nucléotides et peut utiliser l’un ou l’autre comme donneur de phosphate, bien qu’il fonctionne plus rapidement avec l’ATP. À des niveaux modérés d’ADP, la fusion reste active, mais des concentrations très élevées d’ADP commencent à gêner l’activité entraînée par l’ATP, ce qui suggère que l’ADP peut à la fois alimenter et réguler cette enzyme cancéreuse selon son abondance.
Des commutateurs finement réglés à la surface de la protéine
L’équipe a ensuite cartographié précisément les sites où CCDC6-RET se phosphoryle. Ils ont trouvé de multiples sites non seulement dans le noyau catalytique de RET mais aussi dans la portion CCDC6, y compris des sites jusque-là inconnus. Deux tyrosines voisines dans un segment flexible appelé boucle d’activation jouaient des rôles distincts. Un site (Tyr 900) semble crucial pour le repliement correct et la stabilité de la protéine de fusion, tandis que l’autre (Tyr 905) est essentiel pour la phosphorylation efficace d’autres protéines. La mutation de Tyr 905 préservait en grande partie la capacité de la protéine à se modifier elle-même mais annihilait sa capacité à agir sur un peptide substrat ajouté, révélant que « l’auto-activation » et la « signalisation vers l’extérieur » sont contrôlées de manière quelque peu distincte. Ce contrôle nuancé peut aider la protéine de fusion à rester active sans perdre son intégrité structurelle.
Dévoiler les parties mobiles de la protéine en 3D
Pour comprendre comment ces modifications chimiques se traduisent en changements de conformation, les chercheurs ont reconstitué une image tridimensionnelle en combinant des modèles prédictifs d’intelligence artificielle, la microscopie électronique, la diffusion des rayons X aux petits angles et la spectrométrie de masse après réticulation. À l’état de repos, le dimère CCDC6-RET adopte une configuration « face à face » : les deux domaines kinase sont proches l’un de l’autre à la base d’une tige en coiled-coil partagée formée par les segments CCDC6, leurs boucles d’activation se touchant. Après liaison de l’ATP ou de l’ADP, ces lobes kinases s’écartent comme les extrémités de baguettes. Des simulations informatiques suggèrent que, dans cet état plus ouvert, chaque kinase peut atteindre et phosphoryler sa propre boucle d’activation « en cis », préparant le dimère à une signalisation rapide vers d’autres cibles cellulaires.
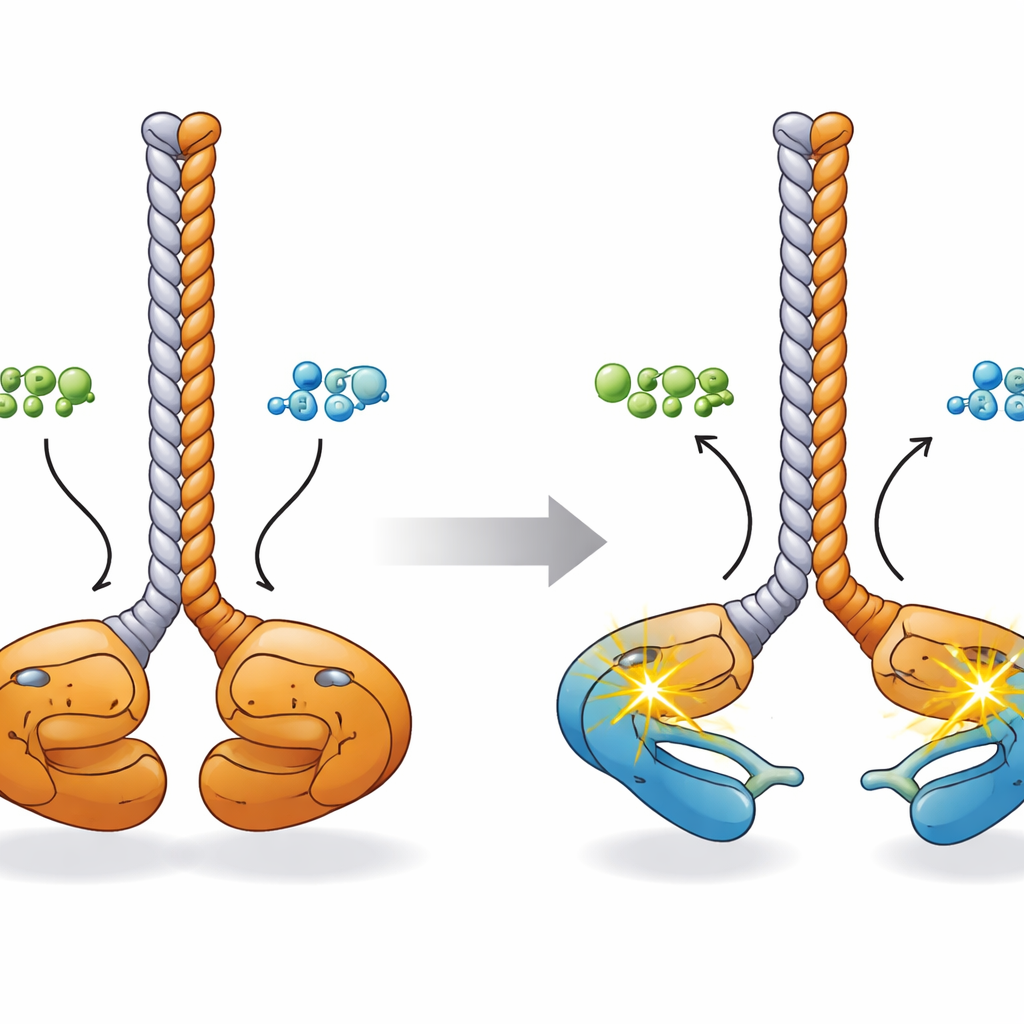
Ce que cela signifie pour le cancer et les thérapies futures
Les cellules tumorales vivent souvent au bord d’une crise énergétique, avec des niveaux d’ATP plus bas et d’ADP plus élevés que les cellules saines. Une kinase de fusion capable de fonctionner avec l’ATP ou l’ADP — et pouvant même modifier sa préférence de cible vers différents acides aminés dans des conditions riches en ADP — pourrait donc bénéficier d’un avantage de survie dans les microenvironnements hostiles des tumeurs solides. En clarifiant la structure de CCDC6-RET, la façon dont elle se dimerise, comment elle utilise les deux formes de carburant cellulaire et quels sites de phosphorylation sont les plus importants, ce travail offre une feuille de route détaillée pour concevoir des médicaments de nouvelle génération. De tels médicaments pourraient viser non seulement le site actif, mais aussi perturber le dimère, empêcher le basculement des boucles d’activation ou exploiter la dépendance inhabituelle de l’enzyme à l’équilibre énergétique de la cellule.
Citation: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Mots-clés: fusion RET, cancer papillaire de la thyroïde, adénocarcinome pulmonaire, activation de kinase protéique, métabolisme ATP ADP