Clear Sky Science · ru
Онкогенный белок слияния CCDC6-RET — киназа, зависящая как от ATP, так и от ADP
Почему это исследование рака важно
Рак легких и щитовидной железы часто вызывается дефектными версиями белков, обеспечивающих клеточную коммуникацию, — так называемых киназ. Одна из таких мутированных форм, белок слияния CCDC6-RET, часто встречается при папиллярном раке щитовидной железы и в некоторых опухолях легкого, особенно после облучения. В этом исследовании показано, как именно этот белок слияния включает собственную активность и почему он может быть особенно приспособлен к стрессовой, бедной энергией среде внутри опухолей, что открывает новые подходы к таргетной терапии.
Генетическая «склейка», подпитывающая опухоли
В нормальных клетках белок RET локализуется в мембране и участвует в передаче сигналов роста. В ряде раков щитовидной железы и в подмножествах рака легкого повреждения и неправильная перестройка ДНК приводят к образованию гибридного гена — часть белка CCDC6 соединяется с функциональной частью RET. Полученный белок, называемый CCDC6-RET, представляет собой автономный сигнальный двигатель, который больше не нуждается в обычных внешних сигналах. Авторы получили этот белок слияния в больших количествах в клетках насекомых и показали, что он образует очень стабильные пары, или димеры, в растворе. Эти димеры обладали высокой активностью, фосфорилируя сами себя в многочисленных местах и резко реагируя на известные ингибиторы RET, что подтверждает: в лабораторных условиях белок ведет себя как его онкогенная версия.
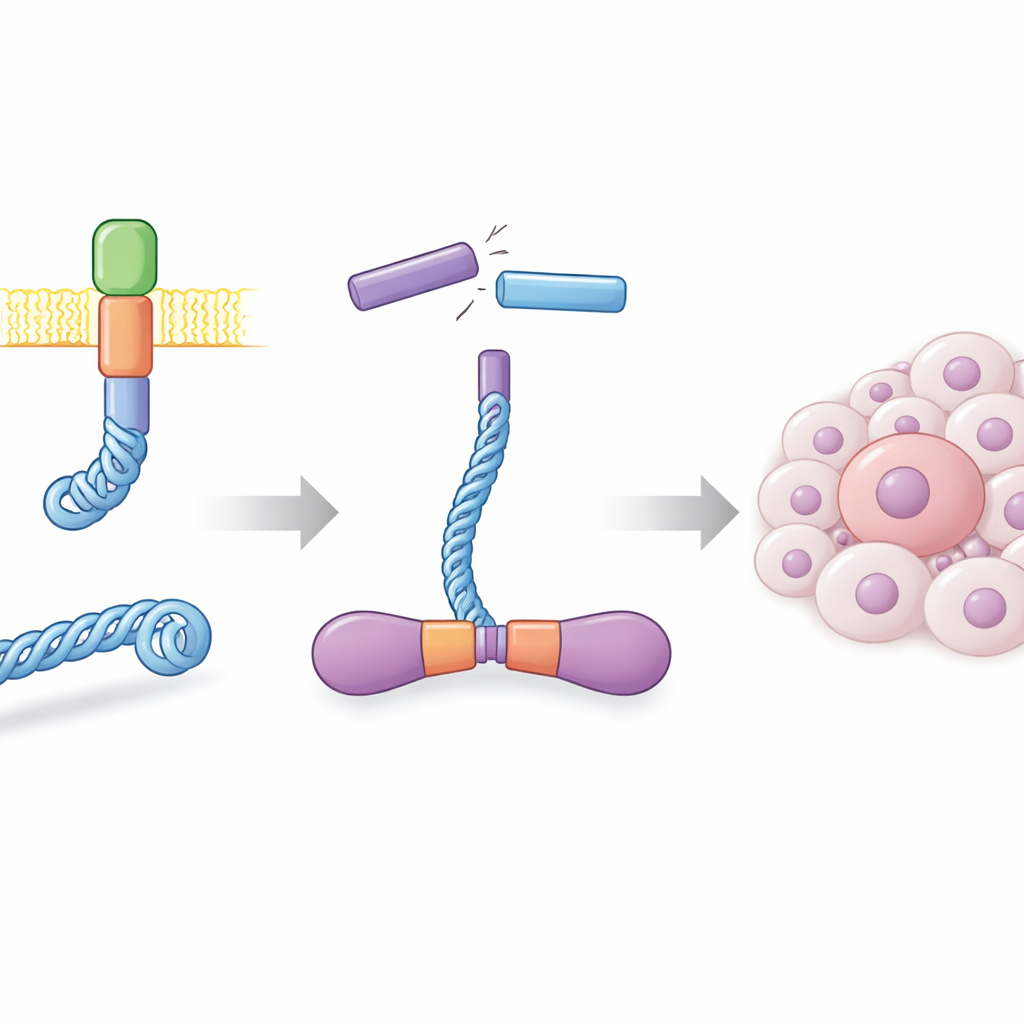
Киназа, работающая на двух типах «топлива»
Большинство киназ используют ATP, главный энергетический «валют» клетки, как источник фосфата для реакций. При биохимическом анализе активности CCDC6-RET с использованием методов ионного хроматографического и масс-спектрометрического анализа с временным разрешением исследователи заметили нечто неожиданное: фосфорилирование белка увеличивалось не только при добавлении ATP, но и при наличии ADP — молекулы с меньшей энергией, образующейся после расходования ATP. Последующие эксперименты показали, что CCDC6-RET связывает оба нуклеотида и может использовать любой из них в качестве донора фосфата, хотя с ATP он работает быстрее. При умеренных концентрациях ADP слияние остается активным, но очень высокие уровни ADP начинают мешать активности, управляемой ATP, что указывает на то, что ADP может и питать, и регулировать эту онкозависимую киназу в зависимости от своей концентрации.
Тонкая настройка управления на поверхности белка
Команда картировала точные участки самофосфорилирования CCDC6-RET. Они нашли несколько сайтов не только в каталитическом ядре RET, но и в части CCDC6, включая ранее неизвестные. Две соседние тирозиновые остатки в гибком сегменте, называемом петлей активации, играли разные роли. Один сайт (Tyr 900) оказался важен для правильного сворачивания и стабильности белка слияния, тогда как другой (Tyr 905) необходим для эффективного фосфорилирования других белков. Мутирование Tyr 905 в значительной мере не повлияло на способность белка модифицировать сам себя, но практически лишило его возможности действовать на добавленный пептидный субстрат, что показывает: «самоактивация» и «внешняя передача сигнала» контролируются в значительной степени раздельно. Такая тонкая регуляция может помочь белку слияния оставаться активным, не теряя структурной целостности.
Раскрытие подвижных частей белка в 3D
Чтобы понять, как эти химические изменения связаны с формой, исследователи собрали трёхмерную картину, используя предсказательные модели на основе искусственного интеллекта, электронную микроскопию, рентгеновское рассеяние под малым углом и масс-спектрометрию с перекрёстным сшиванием. В состоянии покоя димер CCDC6-RET принимает «лицо к лицу» конфигурацию: два киназных домена находятся близко друг к другу у основания общего коил‑коил стебля, сформированного сегментами CCDC6, при этом их петли активации соприкасаются. При связывании ATP или ADP эти лопасти киназ раздвигаются, как кончики пары палочек для еды. Компьютерные моделирования показывают, что в этом более открытом состоянии каждая киназа может достать и фосфорилировать свою собственную петлю активации («in cis»), подготавливая димер к быстрому сигналированию на другие клеточные мишени.
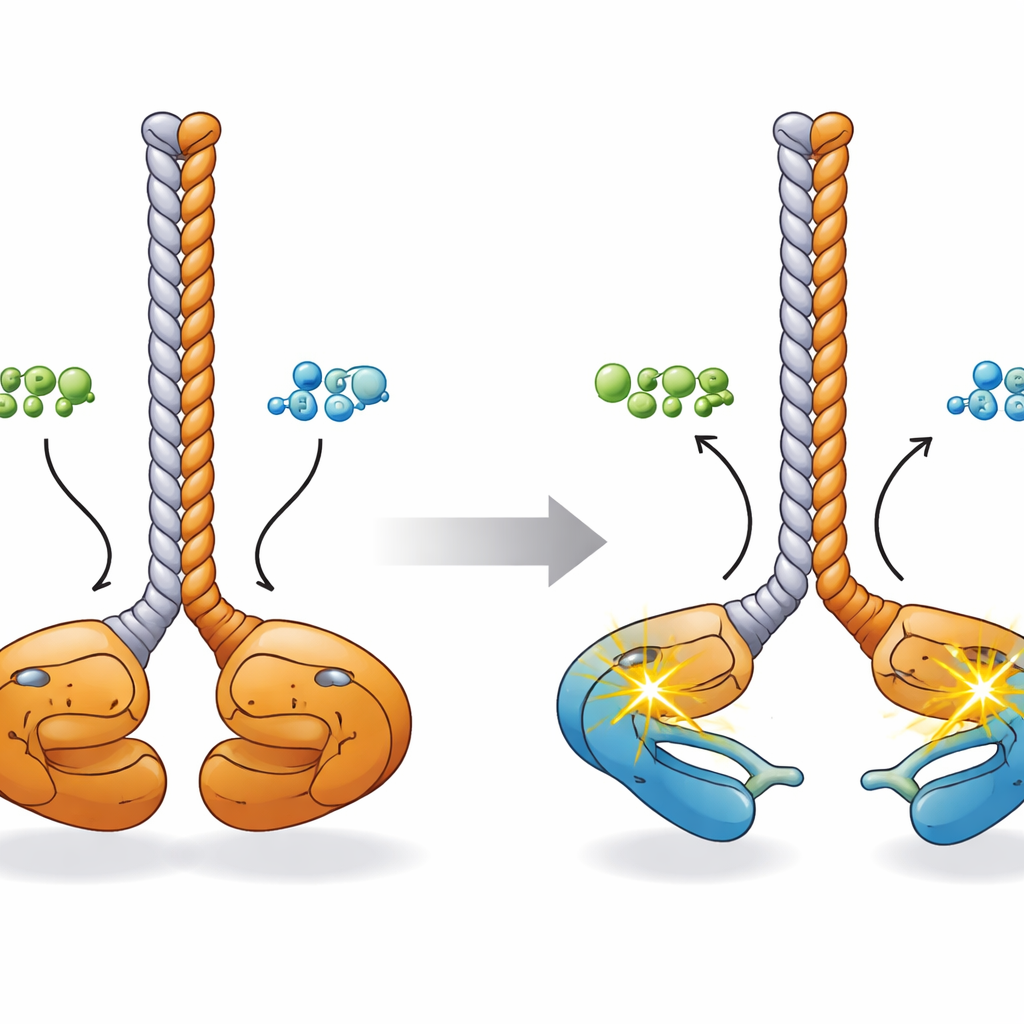
Что это значит для рака и будущих терапий
Клетки опухолей часто живут на грани энергетического кризиса, с пониженным уровнем ATP и повышенным уровнем ADP по сравнению со здоровыми клетками. Киназа‑слияние, способная функционировать и на ATP, и на ADP — и даже менять предпочтения по мишеням аминокислот в условиях, богатых ADP — может иметь преимущество в выживании в суровой микросреде солидных опухолей. Проясняя, как устроен CCDC6-RET, как он димеризуется, как использует обе формы клеточного «топлива» и какие сайты фосфорилирования ключевые, эта работа предлагает подробный план для разработки препаратов следующего поколения. Такие лекарства могли бы не только блокировать активный центр, но и нарушать димеризацию, мешать переключению петли активации или использовать необычную зависимость фермента от энергетического баланса клетки.
Цитирование: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Ключевые слова: слияние RET, папиллярный рак щитовидной железы, аденокарцинома легкого, активация протеиновой киназы, метаболизм ATP ADP