Clear Sky Science · sv
Den onkogena CCDC6-RET-fusionsproteinet är en kinas som är beroende av både ATP och ADP
Varför denna cancerstudie är viktig
Cancer i lunga och sköldkörtel drivs ofta av felaktiga versioner av cellernas kommunikationsproteiner, kallade kinaser. En sådan felaktig version, CCDC6-RET-fusionsproteinet, förekommer ofta i papillärt thyroideacancer och i vissa lungtumörer, särskilt efter strålningsexponering. Denna studie avslöjar hur det fusionsproteinet slår på sig självt och varför det kan vara ovanligt väl anpassat till den stressade, energifattiga miljön inne i tumörer, vilket öppnar nya angreppsvinklar för riktad behandling.
En genetisk ihopslagning som driver tumörer
I friska celler sitter RET-proteinet i cellmembranet och hjälper till att vidarebefordra tillväxtsignaler. I många thyroideacancerformer, och i en undergrupp av lungcancer, går DNA sönder och återfogas på fel ställen så att en hybridgen skapas som fuserar en del av CCDC6-proteinet till den aktiva änden av RET. Resultatet, kallat CCDC6-RET, blir en fristående signalmaskin som inte längre behöver normala yttre signaler. Författarna framställde detta fusionsprotein i stora mängder med hjälp av insektsceller och visade att det bildar mycket stabila par, eller dimerer, i lösning. Dessa dimerer var mycket aktiva, tillsatte fosfatgrupper till sig själva på många ställen och svarade starkt på kända RET-hämmande läkemedel, vilket bekräftar att proteinet framställt i laboratorium beter sig som sin cancerdrivande motsvarighet.
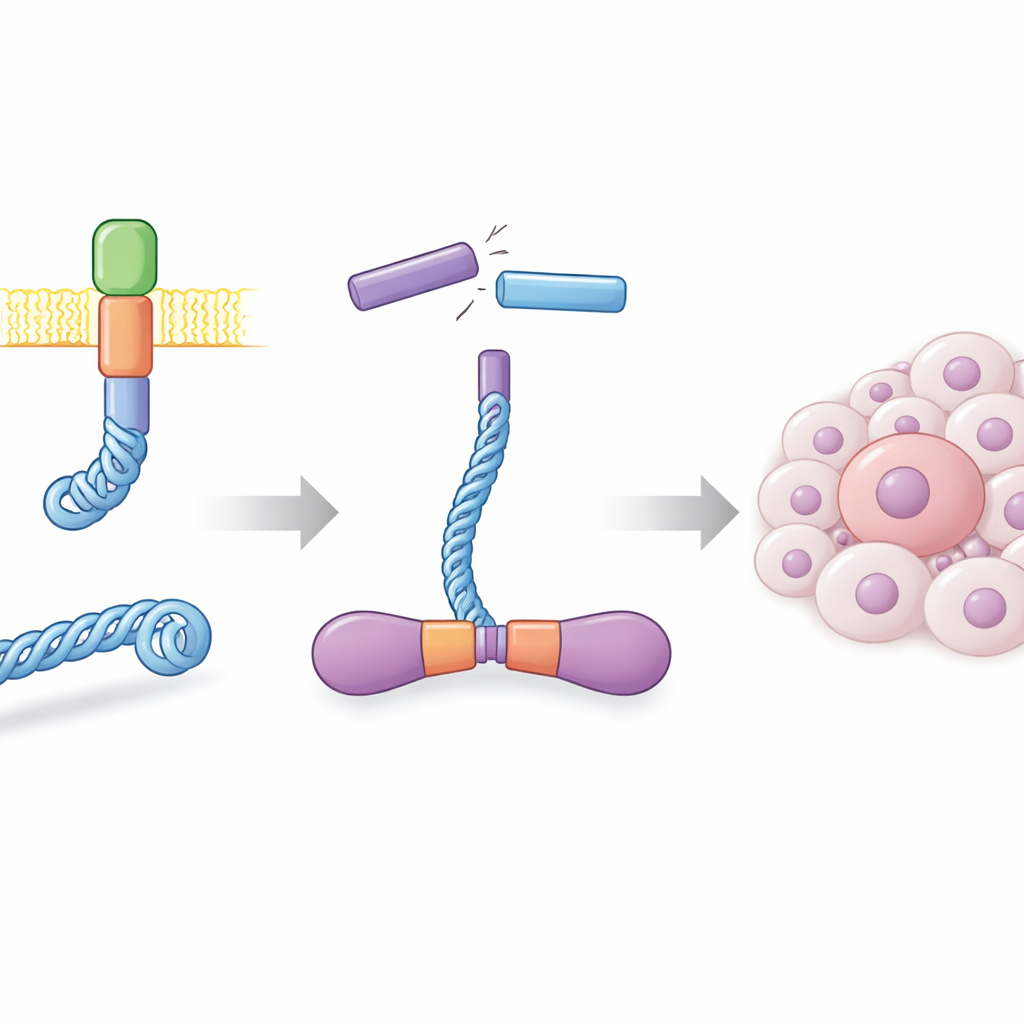
En kinas som drivs av två slags bränsle
De flesta kinaser använder ATP, cellens primära energivaluta, som källa till fosfat för sina reaktioner. När författarna analyserade CCDC6-RET:s aktivitet med biokemiska analyser och tidsupplöst massespektrometri noterade de något överraskande: proteinets fosforylering ökade inte bara med ATP utan även med ADP, den lägre energiform som blir kvar när ATP har förbrukats. Uppföljande experiment visade att CCDC6-RET binder båda nukleotiderna och kan använda antingen som fosfatdonator, även om det arbetar snabbare med ATP. Vid måttliga ADP-nivåer förblir fusionen aktiv, men mycket höga ADP-koncentrationer börjar störa ATP-driven aktivitet, vilket tyder på att ADP både kan driva och reglera detta cancerenzym beroende på dess mängd.
Finjusterade reglage på proteinets yta
Gruppen kartlade sedan exakt var CCDC6-RET fosforylerar sig själv. De fann flera platser inte bara i RET:s katalytiska kärna utan också i CCDC6-delen, inklusive tidigare okända positioner. Två närliggande tyrosiner i ett flexibelt avsnitt kallat aktiveringsloopen spelade distinkta roller. Den ena platsen (Tyr 900) synes vara avgörande för korrekt veckning och stabilitet hos fusionsproteinet, medan den andra (Tyr 905) är nödvändig för effektiv fosforylering av andra proteiner. Mutation av Tyr 905 påverkar i stort sett inte proteinets förmåga att modifiera sig självt men kraftigt försvagar dess förmåga att agera på ett tillsatt peptidsubstrat, vilket visar att ”självaktivering” och ”signalering utåt” i viss mån styrs separat. Denna nyanserade kontroll kan hjälpa fusionsproteinet att förbli aktiv utan att förlora sin strukturella integritet.
Att avslöja proteinets rörliga delar i 3D
För att förstå hur dessa kemiska förändringar hänger ihop med form tog forskarna fram en tredimensionell bild med hjälp av förutsägande artificiell intelligens-modeller, elektronmikroskopi, småvinkelröntgentspridning och tvärbindnings-massespektrometri. I sitt vilotillstånd antar CCDC6-RET-dimeren en ”ansikte-mot-ansikte”-konfiguration: de två kinasdomänerna ligger nära varandra vid basen av en gemensam coiled-coil-stjälk som bildas av CCDC6-segmenten, med sina aktiveringsloopar i kontakt. Vid bindning av ATP eller ADP svänger kinasloberna isär som spetsarna på ett par ätpinnar. Datorsimuleringar antyder att i detta mer öppna tillstånd kan varje kinas nå in och fosforylera sin egen aktiveringsloop (”in cis”), vilket förbereder dimeren för snabb signalering till andra cellulära mål.
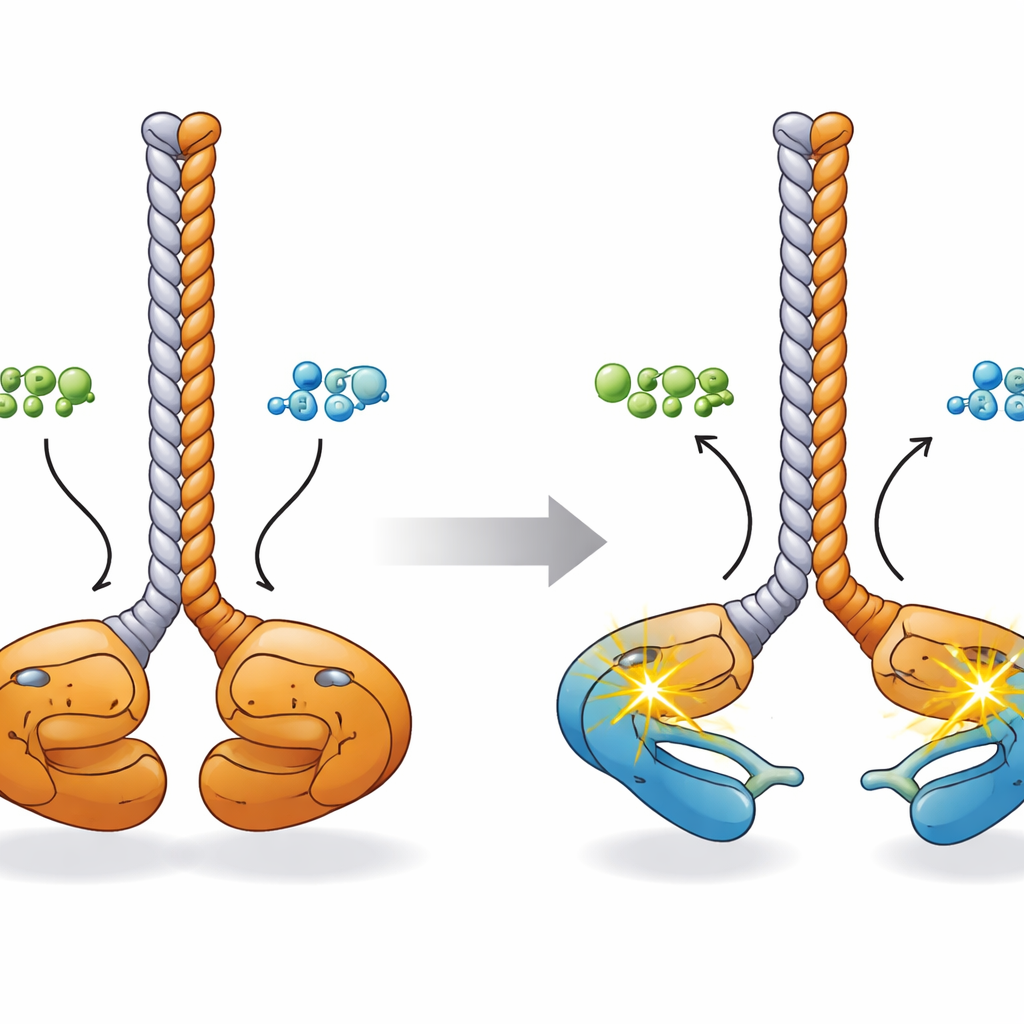
Vad detta betyder för cancer och framtida terapier
Tumörceller lever ofta på gränsen till en energikris, med lägre ATP- och högre ADP-nivåer än friska celler. En fusionskinas som kan fungera med antingen ATP eller ADP — och till och med ändra sitt målinriktning mot olika aminosyror under ADP-rika förhållanden — kan därför ha en överlevnadsfördel i de hårda mikro-miljöerna hos solida tumörer. Genom att klargöra hur CCDC6-RET är uppbyggd, hur den dimeriserar, hur den använder båda formerna av cellens bränsle och vilka fosforyleringsplatser som är viktigast, erbjuder detta arbete en detaljerad ritning för att utforma nästa generationens läkemedel. Sådana läkemedel skulle kunna inriktas inte bara på att blockera det aktiva sätet, utan också på att störa dimeren, störa växling i aktiveringsloopen eller utnyttja enzymets ovanliga beroende av cellens energibalans.
Citering: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Nyckelord: RET-fusion, papillärt thyroideacancer, lungadenokarcinom, aktivering av proteinkinas, ATP ADP-metabolism