Clear Sky Science · he
חלבון היתוך אונקוגני CCDC6-RET הוא קינאז התלוי הן ב-ATP והן ב-ADP
מדוע מחקר הסרטן הזה חשוב
סרטן הריאות והתריסית מונעים לעתים קרובות על ידי גרסאות פגומות של חלבוני תקשורת תאיים הנקראים קינאזות. גרסה פגומה אחת כזו, חלבון ההיתוך CCDC6-RET, מופיעה לעתים קרובות בסרטן בלוטת התריס הפפילרי ובחלק ממקרי סרטן הריאה, במיוחד לאחר חשיפה לקרינה. המחקר הזה חושף כיצד חלבון ההיתוך מפעיל את עצמו ולמה הוא עשוי להיות מותאם במיוחד לסביבה הלחוצה ודלה האנרגיה בתוך הגידול, ובכך פותח זוויות חדשות לטיפול ממוקד.
שיבוש גנטי שמזין את הגידולים
בתאים תקינים, חלבון RET ממוקם בממברנת התא ועוזר להעביר אותות גדילה. בהרבה ממקרי סרטן התריס ובתת-קבוצה של סרטן הריאה, שברים בקֶרֶת ה-DNA ומחברתם במקומות לא נכונים יוצרים גֵן היברידי הממזג חלק מחלבון CCDC6 עם קצה הפעיל של RET. התוצאה, שמכונה CCDC6-RET, היא מנוע איתות עצמאי שאינו צריך עוד אותות חיצוניים רגילים. המחברים ייצרו את חלבון ההיתוך הזה בכמויות גדולות בתאי חרקים והראו כי הוא יוצר זוגות יציבים מאוד, או דימרים, במצב תמיסה. דימרים אלה גילו פעילות גבוהה, הוסיפו קבוצות פוספט לעצמם במקומות רבים וענו בעוצמה על תרופות ידועות החוסמות את RET, מה שאישש כי החלבון המיוצר במעבדה מתנהג כמו מקבילו המניע סרטן.
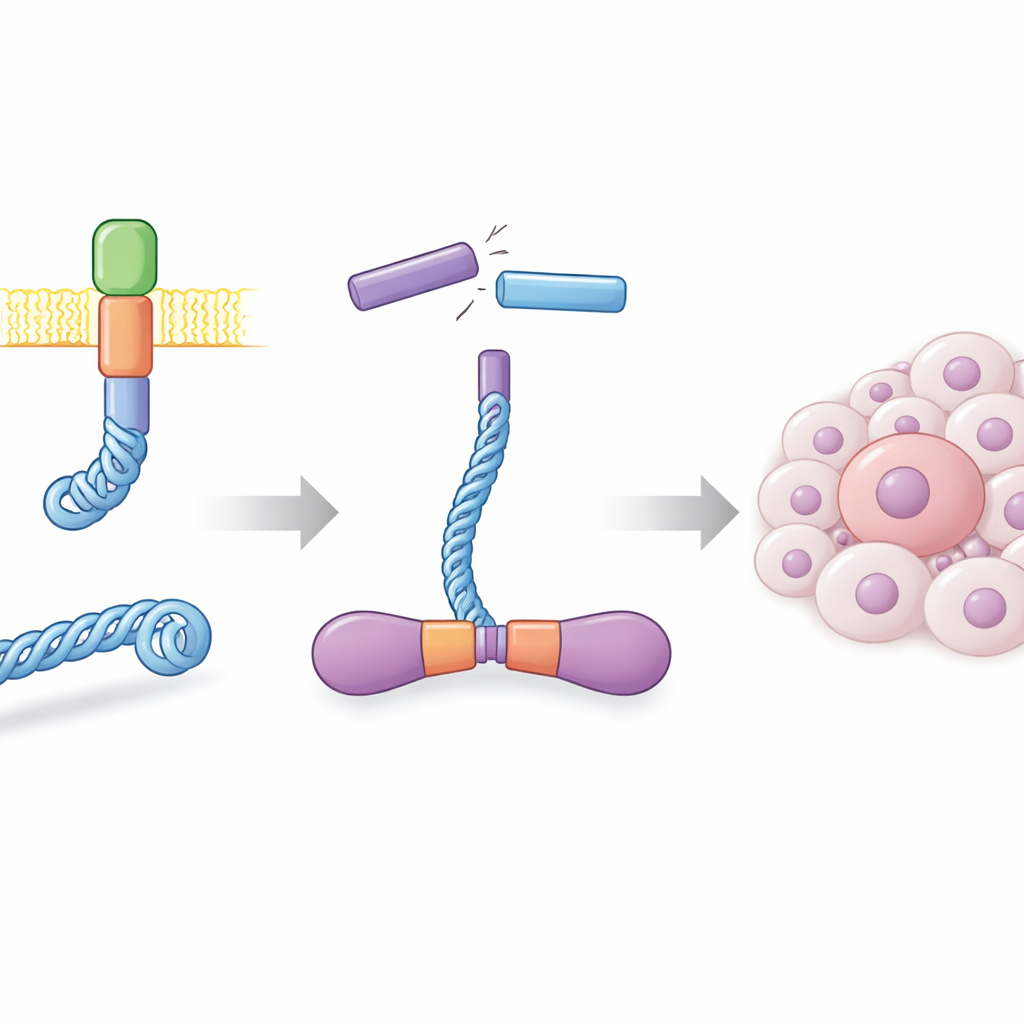
קינאז שרץ על שני סוגי דלק
רוב הקינאזות משתמשות ב-ATP, המטבע האנרגטי הראשי של התא, כמקור קבוצת הפוספט לתגובותיהן. כאשר החוקרים ניתחו את פעילות CCDC6-RET באמצעות ניסויי ביוכימיה ומסה-ספקטרומטריה מרובת-זמן, הם שמו לב לממצא מפתיע: הפוספורילציה של החלבון עלתה לא רק עם ATP אלא גם עם ADP, התוצר האנרגטי הנמוך שנשאר לאחר שה-ATP נוצל. ניסויים משלימים הראו כי CCDC6-RET קושר את שני הנוקלאוטידים ויכול להשתמש בכל אחד מהם כמי שמספק את הפוספט, אם כי הוא פועל מהר יותר עם ATP. ברמות ADP מתונות החלבון נשאר פעיל, אך ריכוזי ADP מאוד גבוהים מתחילים להפריע לפעילות המונעת על ידי ATP, מה שמרמז כי ADP יכול גם להזין וגם לווסת את אנזים הסרטן הזה בהתאם לשפע שלו.
מפסקים מכוילים בקפידה על פני שטח החלבון
הקבוצה המשיכה ולמפה בדיוק היכן CCDC6-RET מפוספורל את עצמו. הם מצאו מספר אתרים לא רק בליבה הקטליטית של RET אלא גם בחלק של CCDC6, כולל אתרים שלא היו ידועים קודם. שתי טירוזינות שכנות בחלק גמיש המכונה לולאת ההפעלה מילאו תפקידים מובחנים. אתר אחד (Tyr 900) נראה חיוני לקיפול נכון ויציבות חלבון ההיתוך, בעוד האתר השני (Tyr 905) הכרחי לפוספורילציה יעילה של חלבונים אחרים. שינוי מוטציה של Tyr 905 חסך במידה רבה את יכולת החלבון לשנות את עצמו אך פגע קשות ביכולתו לפעול מול תת-מולקולת פפטיד חיצונית, וחשף כי "הפעלה עצמית" ו"איתות כלפי חוץ" נשלטות במידה מסוימת בנפרד. בקרה מדויקת זו עשויה לעזור לחלבון ההיתוך להישאר פעיל מבלי לאבד את שלמותו המישורית.
גילוי חלקי התנועה של החלבון בתלת-ממד
כדי להבין כיצד השינויים הכימיים הללו מתייחסים לצורה, החוקרים הרכיבו תמונה תלת-ממדית באמצעות מודלים חיזוי המבוססים על בינה מלאכותית, מיקרוסקופיה אלקטרונית, פיזור קרני רנטגן בזווית קטנה ומסה-ספקטרומטריה לאחר צלבות. במצב המנוחה, דימר ה-CCDC6-RET מאמץ תצורת "פנים אל פנים": שתי הדומיינים הקינאזיים יושבים קרוב זה לזה בבסיס סְטֶיק קוֹייל משותף הנוצר על ידי מקטעי CCDC6, עם לולאות ההפעלה נוגעות זו בזו. כאשר ATP או ADP נקשרים, האונות הקינאזיות אלו מתרחקות זו מזו כמו קצות של מקלות אכילה. סימולציות ממוחשבות מרמזות שבמצב הפתוח יותר כל קינאז יכול להגיע ולפוספורל את לולאת ההפעלה שלו "באופן עצמאי" (in cis), מה שמכין את הדימר לאיתות מהיר למטרות תאיות אחרות.
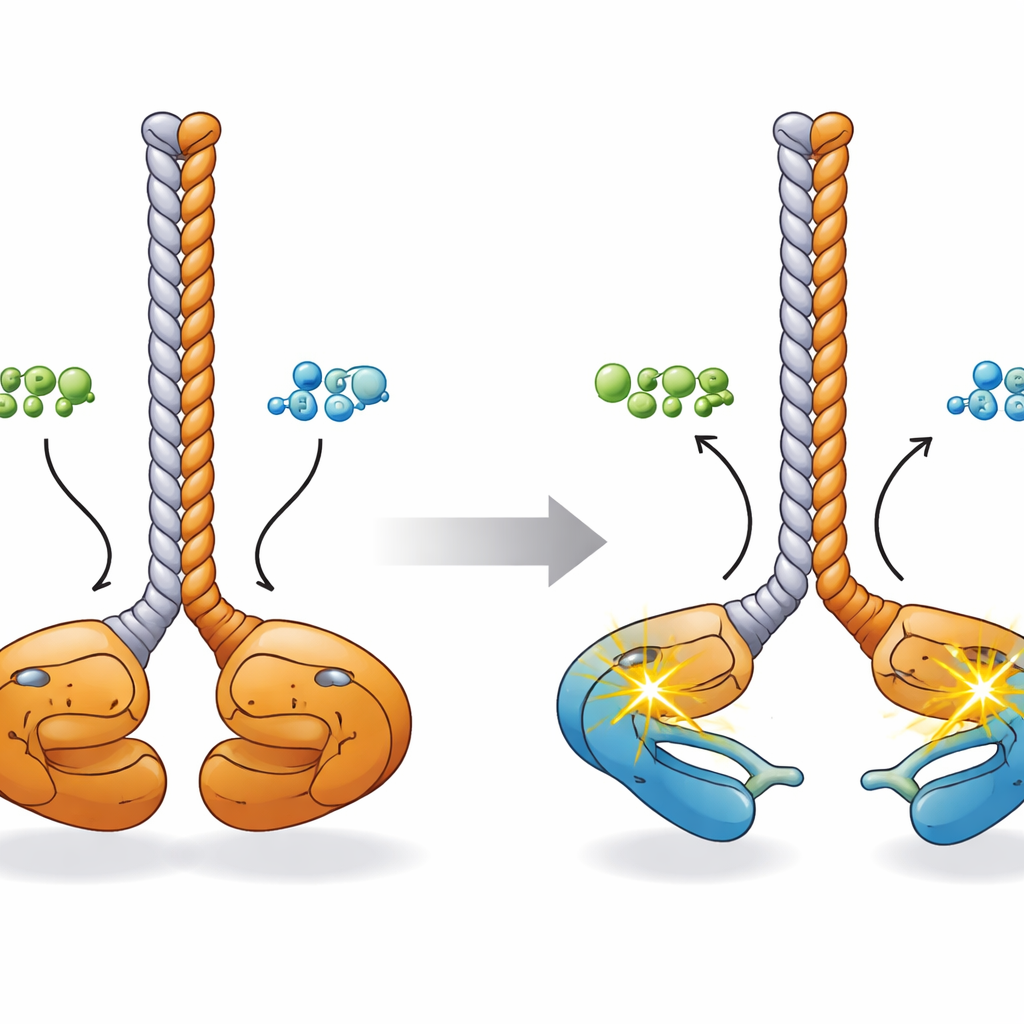
מה משמעות הדבר עבור סרטן וטיפולים עתידיים
תאי גידול לעתים קרובות חיים על סף משבר אנרגטי, עם רמות ATP נמוכות ורמות ADP גבוהות יותר מאשר בתאים בריאים. קינאז היתוך שיכול לפעול גם עם ATP וגם עם ADP—ואפילו לשנות את העדפת המטרות שלו לחומצות אמינו שונות בתנאים עשירים ב-ADP—עשוי לכן ליהנות מיתרון הישרדותי בסביבות הקשות של גידולים מוצקים. על ידי הבהרת האופן שבו CCDC6-RET בנוי, כיצד הוא מבצע דימריזציה, כיצד הוא משתמש בשתי צורות הדלק התאי ואילו אתרי פוספורילציה הם החשובים ביותר, עבודה זו מציעה שרטוט מפורט לעיצוב תרופות מדור הבא. תרופות כאלה יכולות לשאוף לא רק לחסום את אתר הפעילות, אלא גם להפריע לדימר, להפריע להחלפת לולאות ההפעלה או לנצל את התלות הבלתי שגרתית של האנזים באיזון האנרגטי של התא.
ציטוט: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
מילות מפתח: היתוך RET, סרטן בלוטת התריס הפפילרי, אדנוקרצינומה של הריאה, הפעלה של קינאז חלבוני, מטבוליזם ATP ADP