Clear Sky Science · it
La proteina di fusione oncogenica CCDC6-RET è una chinasi dipendente sia da ATP che da ADP
Perché questo studio sul cancro è importante
I tumori del polmone e della tiroide sono spesso guidati da versioni difettose di proteine di comunicazione cellulare chiamate chinasi. Una di queste varianti difettose, la proteina di fusione CCDC6-RET, ricorre frequentemente nel carcinoma papillare della tiroide e in alcuni tumori polmonari, specialmente dopo esposizione alle radiazioni. Questo studio rivela come quella proteina di fusione si attivi e perché possa essere particolarmente ben adattata all’ambiente stressato e povero di energia all’interno dei tumori, aprendo nuove possibilità per trattamenti mirati.
Un miscuglio genetico che alimenta i tumori
Nelle cellule sane, la proteina RET è localizzata nella membrana cellulare e contribuisce a trasmettere segnali di crescita. In molti carcinomi tiroidei, e in una sottoserie di tumori polmonari, il DNA subisce rotture e ricongiungimenti in punti errati, creando un gene ibrido che fonde una porzione della proteina CCDC6 con l’estremità funzionale di RET. Il risultato, chiamato CCDC6-RET, è un motore di segnalazione autonomo che non ha più bisogno dei normali segnali esterni. Gli autori hanno prodotto questa proteina di fusione in grande quantità usando cellule di insetto e hanno mostrato che in soluzione forma coppie molto stabili, o dimeri. Questi dimeri risultavano altamente attivi, autofilando numerosi siti e rispondendo in modo marcato a farmaci noti per bloccare RET, confermando che la proteina prodotta in laboratorio si comporta come la controparte che guida il cancro.
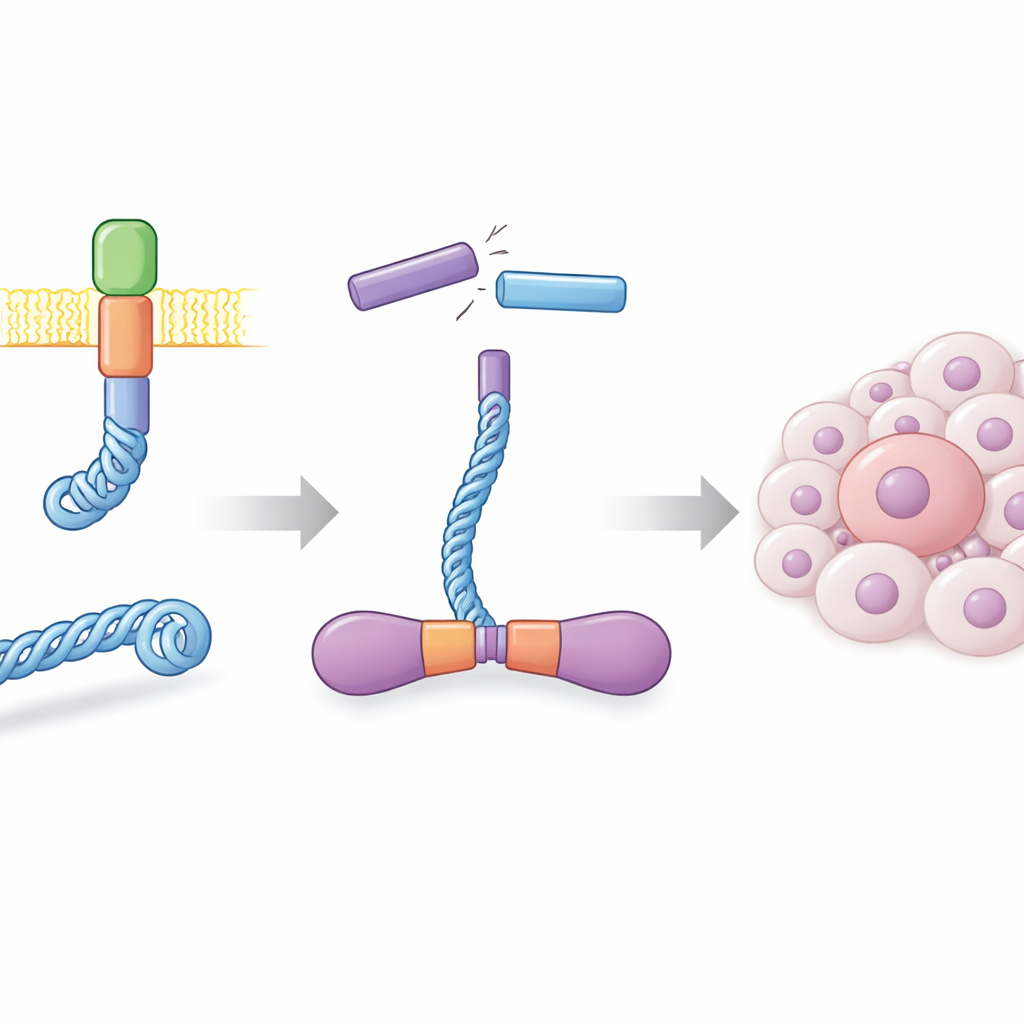
Una chinasi che funziona con due tipi di carburante
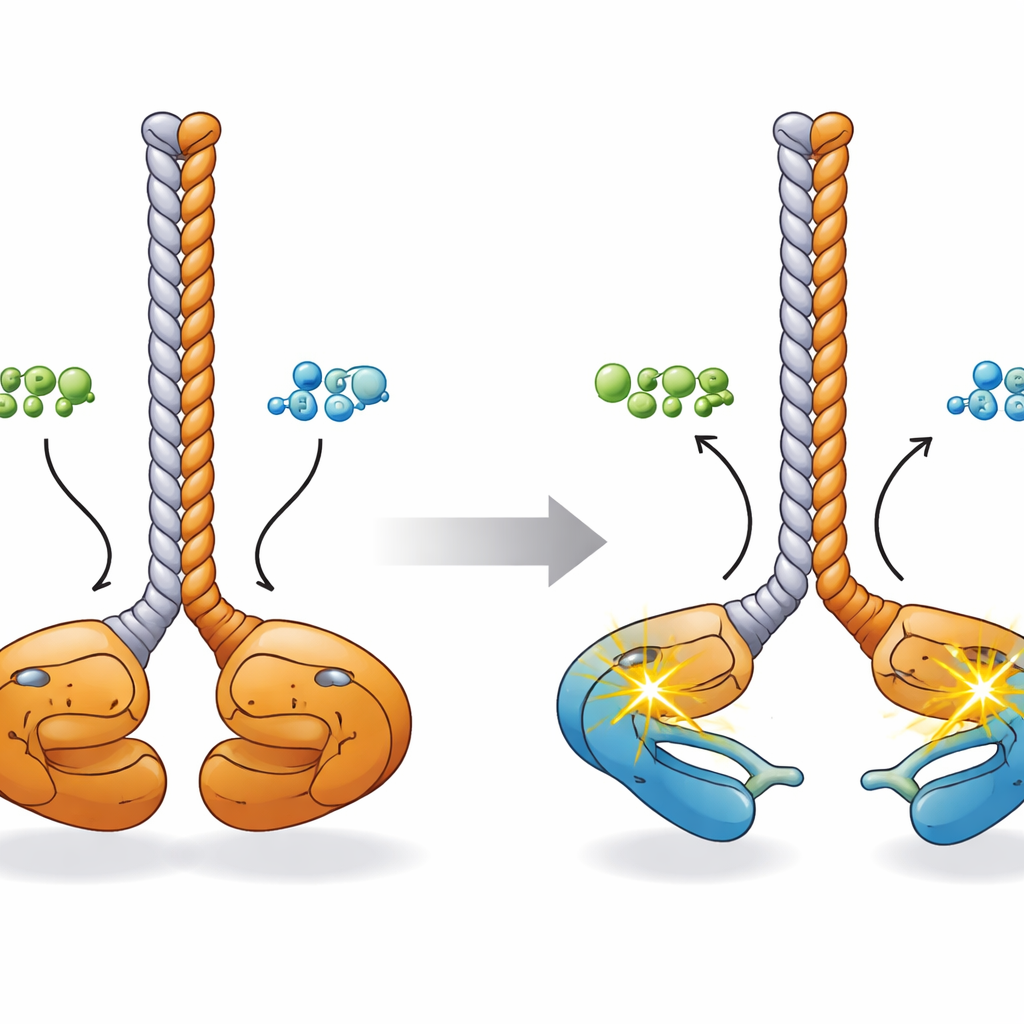
La maggior parte delle chinasi usa ATP, la principale valuta energetica della cellula, come fonte del gruppo fosfato per le proprie reazioni. Quando gli autori hanno analizzato l’attività di CCDC6-RET con saggi biochimici e spettrometria di massa risolta nel tempo, hanno osservato qualcosa di sorprendente: la fosforilazione della proteina aumentava non solo con l’ATP ma anche con l’ADP, il prodotto a più basso contenuto energetico lasciato dopo l’utilizzo dell’ATP. Esperimenti di follow-up hanno mostrato che CCDC6-RET lega entrambi i nucleotidi e può usare l’uno o l’altro come donatore di fosfato, sebbene lavori più rapidamente con l’ATP. A livelli moderati di ADP la fusione rimane attiva, ma concentrazioni molto alte di ADP cominciano a interferire con l’attività guidata dall’ATP, suggerendo che l’ADP può sia alimentare sia regolare questa chinasi tumorale a seconda della sua abbondanza.
Interruttori finemente regolati sulla superficie della proteina
Il gruppo ha quindi mappato esattamente dove CCDC6-RET si fosforila. Hanno trovato molteplici siti non solo nel nucleo catalitico di RET ma anche nella porzione CCDC6, inclusi siti precedentemente sconosciuti. Due tirosine adiacenti in un segmento flessibile chiamato loop di attivazione svolgevano ruoli distinti. Un sito (Tyr 900) sembra cruciale per il corretto ripiegamento e la stabilità della proteina di fusione, mentre l’altro (Tyr 905) è essenziale per una fosforilazione efficiente di altre proteine. La mutazione di Tyr 905 ha sostanzialmente risparmiato la capacità della proteina di modificare se stessa ma ha compromesso la sua abilità di agire su un peptide substrato aggiunto, rivelando che «auto-attivazione» e «segnalazione verso l’esterno» sono controllate in parte separatamente. Questo controllo sfumato può aiutare la proteina di fusione a restare attiva senza perdere integrità strutturale.
Rivelare le parti mobili della proteina in 3D
Per comprendere come questi cambiamenti chimici si traducano in variazioni conformazionali, i ricercatori hanno ricostruito un’immagine tridimensionale usando modelli predittivi di intelligenza artificiale, microscopia elettronica, scattering di raggi X a piccolo angolo e spettrometria di massa con cross-linking. Nel suo stato di riposo, il dimero CCDC6-RET adotta una configurazione «faccia a faccia»: i due domini chinasi stanno vicini alla base di un gambo coiled-coil condiviso formato dai segmenti CCDC6, con i loro loop di attivazione a contatto. Al legarsi di ATP o ADP, quei lobi della chinasi si aprono come le punte di un paio di bacchette. Le simulazioni al computer suggeriscono che in questo stato più aperto ciascuna chinasi può raggiungere e fosforilare il proprio loop di attivazione («in cis»), predisponendo il dimero per una rapida segnalazione verso altri bersagli cellulari.
Cosa significa per il cancro e le terapie future
Le cellule tumorali spesso vivono al limite di una crisi energetica, con livelli di ATP più bassi e di ADP più alti rispetto alle cellule sane. Una chinasi di fusione in grado di funzionare sia con ATP sia con ADP—e persino di modificare la preferenza per diversi aminoacidi in condizioni ricche di ADP—potrebbe dunque avere un vantaggio di sopravvivenza nei microambienti ostili dei tumori solidi. Chiarendo come CCDC6-RET è costruita, come si dimerizza, come utilizza entrambe le forme di carburante cellulare e quali siti di fosforilazione sono più importanti, questo lavoro offre un progetto dettagliato per progettare farmaci di nuova generazione. Tali farmaci potrebbero mirare non solo a bloccare il sito attivo, ma anche a disturbare il dimero, interferire con lo switching del loop di attivazione o sfruttare l’insolita dipendenza dell’enzima dal bilancio energetico cellulare.
Citazione: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Parole chiave: fusione RET, carcinoma papillare della tiroide, adenocarcinoma polmonare, attivazione delle proteine chinasi, metabolismo ATP ADP