Clear Sky Science · tr
Onkogenik CCDC6-RET füzyon proteini, hem ATP hem de ADP bağımlı bir kinazdır
Bu kanser çalışması neden önemli
Akciğer ve tiroid kanserleri sıklıkla kinaz adı verilen hücre iletişim proteinlerinin bozuk biçimleri tarafından yönlendirilir. Bu bozuk versiyonlardan biri olan CCDC6-RET füzyon proteini, papiller tiroid kanserinde ve özellikle radyasyona maruz kalma sonrası bazı akciğer kanserlerinde sıkça görülür. Bu çalışma, söz konusu füzyon proteinin nasıl etkinleştiğini ve tümör içindeki stresli, enerji açısından fakir ortama neden olağanüstü biçimde uyum sağlamış olabileceğini ortaya koyuyor; bu da hedefe yönelik tedaviler için yeni yaklaşımların kapısını açıyor.
Tümörleri besleyen genetik bir karışım
Sağlıklı hücrelerde RET proteini hücre zarında yer alır ve büyüme sinyallerinin iletilmesine yardımcı olur. Birçok tiroid kanserinde ve bazı akciğer kanserleri alt grubunda DNA kırıkları yanlış yerlerde yeniden birleşerek CCDC6 proteininin bir bölümünü RET’in işleyici kısmına bağlayan hibrit bir gen oluşturur. Ortaya çıkan CCDC6-RET, normal dış uyaranlara ihtiyaç duymayan bağımsız bir sinyal motorudur. Yazarlar bu füzyon proteinini böcek hücreleri kullanarak bol miktarda üretmiş ve çözeltide çok sağlam çiftler (dimerler) oluşturduğunu göstermişlerdir. Bu dimerler oldukça aktiftir; kendilerine birçok yerde fosfat grubu eklemekte ve bilinen RET engelleyici ilaçlara güçlü yanıt vermektedir; bu da laboratuvarda üretilen proteinin kanser sürükleyici muadili gibi davrandığını doğrular.
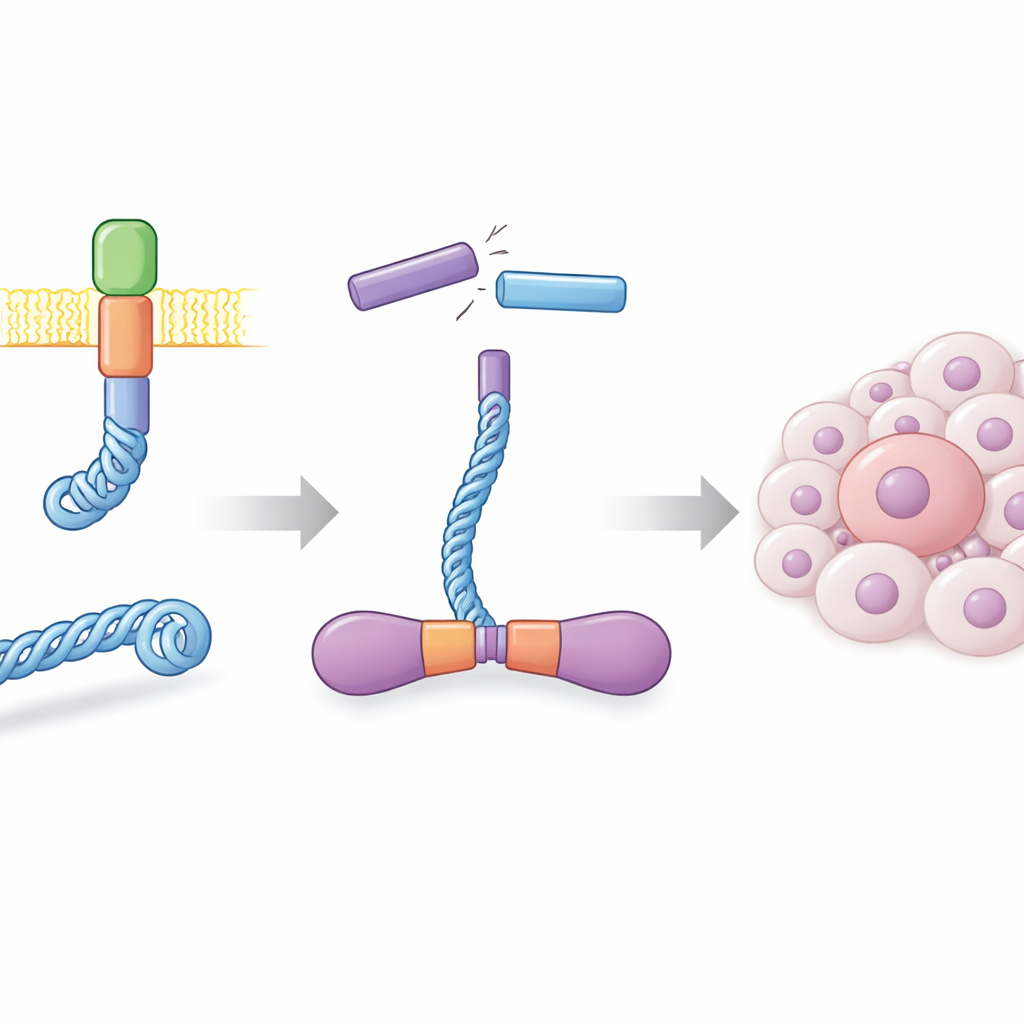
İki tür yakıtla çalışan bir kinaz
Çoğu kinaz tepkileri için fosfat kaynağı olarak hücrenin birincil enerji parası ATP’yi kullanır. Yazarlar CCDC6-RET’in aktivitesini biyokimyasal testler ve zaman çözünür kütle spektrometrisi ile analiz ettiğinde şaşırtıcı bir şey fark ettiler: proteinin fosforilasyonu yalnızca ATP ile değil, aynı zamanda ATP tüketildikten sonra kalan düşük enerjili ürün olan ADP ile de artıyordu. Takip deneyleri CCDC6-RET’in her iki nükleotidi de bağladığını ve her birini fosfat bağışı için kullanabildiğini gösterdi; ancak ATP ile daha hızlı çalışıyordu. Orta düzey ADP konsantrasyonlarında füzyon aktifliğini korurken, çok yüksek ADP seviyeleri ATP kaynaklı aktiviteyi bozmayı başlattı; bu da ADP’nin bolluğuna bağlı olarak hem bu kanser enzimini besleyebileceğini hem de düzenleyebileceğini düşündürür.
Yüzeyde ince ayarlı kontrol anahtarları
Araştırma ekibi CCDC6-RET’in kendini tam olarak nerelere fosforiladığını haritalamaya devam etti. RET’in katalitik çekirdeğinde olduğu kadar CCDC6 bölümünde de daha önce bilinmeyenlerin de aralarında bulunduğu çok sayıda site buldular. Aktivasyon halkası olarak adlandırılan esnek bir segmentteki birbirine yakın iki tirozin farklı roller oynuyordu. Bir bölge (Tyr 900) füzyon proteininin uygun katlanması ve stabilitesi için hayati görünürken, diğeri (Tyr 905) diğer proteinlerin etkin fosforilasyonu için şarttı. Tyr 905’in mutasyonu proteinin kendini modifiye etme yeteneğini büyük ölçüde etkilemezken, ilave bir peptid altstrata etki etme kapasitesini bozdu; bu da “kendini aktive etme” ile “dışa sinyal verme” işlevlerinin bir ölçüde ayrı kontrol edildiğini ortaya koyuyor. Bu ince ayarlı kontrol, füzyon proteinin yapısal bütünlüğünü kaybetmeden sürekli aktif kalmasına yardımcı olabilir.
Proteinin hareketli parçalarını 3B olarak açığa çıkarmak
Bu kimyasal değişikliklerin şekille nasıl ilişkili olduğunu anlamak için araştırmacılar, yapay zeka öngörü modelleri, elektron mikroskobu, küçük açılı X-ışını saçılması ve çapraz bağlama kütle spektrometrisini bir araya getirerek üç boyutlu bir resim oluşturdular. Dinlenme durumunda CCDC6-RET dimeri “yüz yüze” konfigürasyonunu benimser: iki kinaz domaı, CCDC6 segmentleri tarafından oluşturulan ortak bir koil-çubuk gövdesinin tabanında birbirine yakın oturur ve aktivasyon halkaları temas halindedir. ATP veya ADP bağlandığında bu kinaz lobları bir çift yemek çubuğunun uçları gibi açılır. Bilgisayar simülasyonları bu daha açık durumda her bir kinazın kendi aktivasyon halkasını “in cis” yani kendi üzerinde fosforile edebileceğini ve dimeri diğer hücresel hedeflere hızlı sinyal göndermeye hazırlayabileceğini öne sürer.
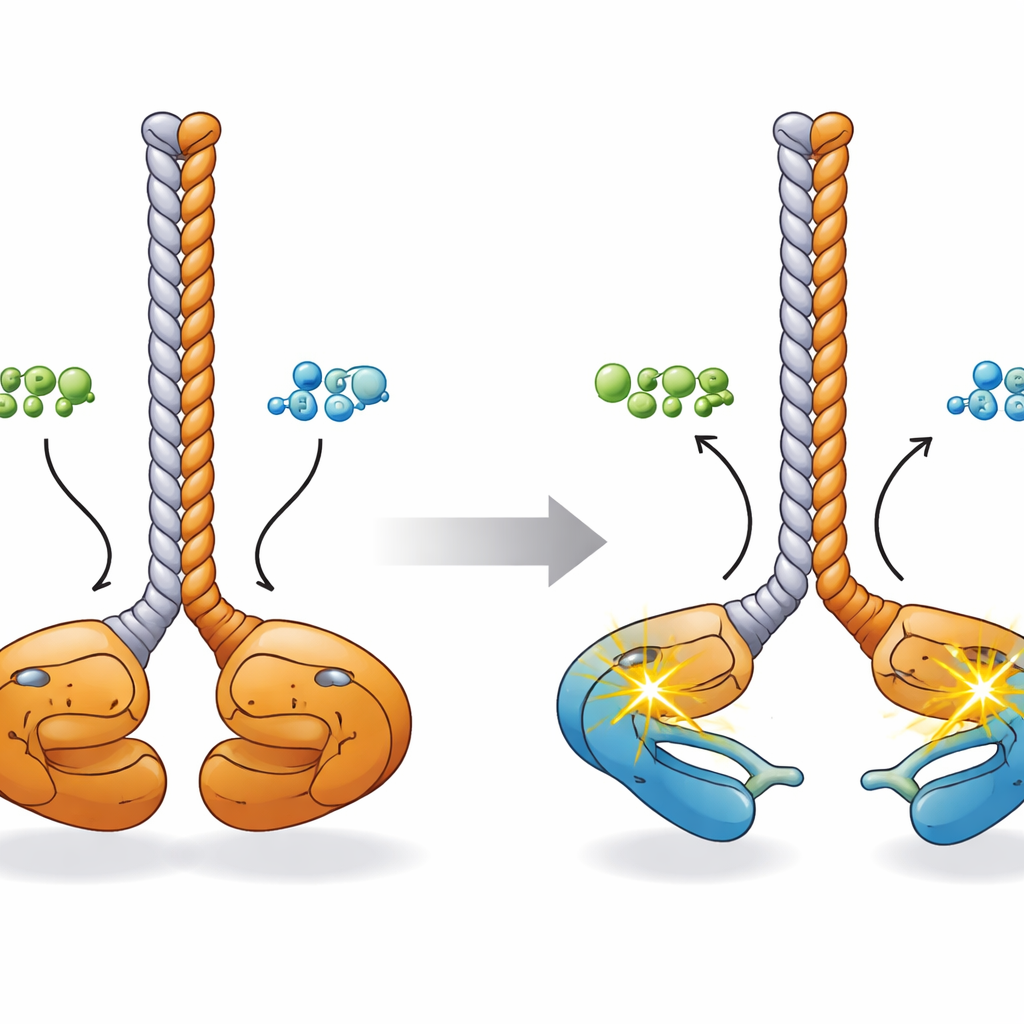
Bu bulguların kanser ve gelecekteki tedaviler için anlamı
Tümör hücreleri genellikle enerji krizinin eşiğinde yaşar; sağlıklı hücrelere kıyasla daha düşük ATP ve daha yüksek ADP seviyelerine sahiptir. Hem ATP hem ADP ile işleyebilen—hatta ADP açısından zengin koşullarda hedef tercihlerini farklı aminoasitlere kaydırabilen—bir füzyon kinaz, katı tümörlerin sert mikroortamında hayatta kalma avantajına sahip olabilir. CCDC6-RET’in nasıl inşa edildiğini, nasıl dimerleştiğini, her iki hücresel yakıt biçimini nasıl kullandığını ve hangi fosforilasyon bölgelerinin en önemli olduğunu açıklayarak bu çalışma, yeni nesil ilaçlar tasarlamak için ayrıntılı bir plan sunuyor. Bu tür ilaçlar yalnızca aktif bölgeyi engellemeyi değil, aynı zamanda dimeri bozmayı, aktivasyon-halkası geçişini müdahale etmeyi veya enzimin hücrenin enerji dengesine olan alışılmadık bağımlılığını kullanmayı hedefleyebilir.
Atıf: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Anahtar kelimeler: RET füzyonu, papiller tiroid kanseri, akciğer adenokarsinomu, protein kinaz aktivasyonu, ATP ADP metabolizması