Clear Sky Science · pl
Onkogenny białkowy fuzyjny CCDC6-RET jest kinazą zależną od ATP i ADP
Dlaczego to badanie raka ma znaczenie
Raki płuc i tarczycy często są napędzane przez wadliwe wersje białek komunikacji komórkowej zwanych kinazami. Jedna z takich wadliwych form, białko fuzyjne CCDC6-RET, pojawia się często w raku brodawkowatym tarczycy i w niektórych nowotworach płuc, zwłaszcza po narażeniu na promieniowanie. Badanie to ujawnia, jak to białko fuzyjne się włącza i dlaczego może być wyjątkowo dobrze przystosowane do zestresowanego, ubogiego energetycznie środowiska w obrębie guzów, otwierając nowe możliwości ukierunkowanych terapii.
Genetyczne połączenie, które napędza guzy
W zdrowych komórkach białko RET znajduje się w błonie komórkowej i pomaga przekazywać sygnały wzrostu. W wielu rakach tarczycy i w części raków płuc dochodzi do przerwań i nieprawidłowych połączeń DNA, tworząc hybrydowy gen, który łączy fragment białka CCDC6 z aktywną częścią RET. Powstający w ten sposób CCDC6-RET jest samodzielnym silnikiem sygnalizacyjnym, który nie potrzebuje normalnych zewnętrznych sygnałów. Autorzy wyprodukowali to białko fuzyjne w dużych ilościach w komórkach owadzich i wykazali, że w roztworze tworzy bardzo stabilne pary, czyli dimery. Te dimery były wysoce aktywne, fosforylowały się w wielu miejscach i silnie reagowały na znane leki hamujące RET, potwierdzając, że białko wytworzone w laboratorium zachowuje się jak jego nowotworowy odpowiednik.
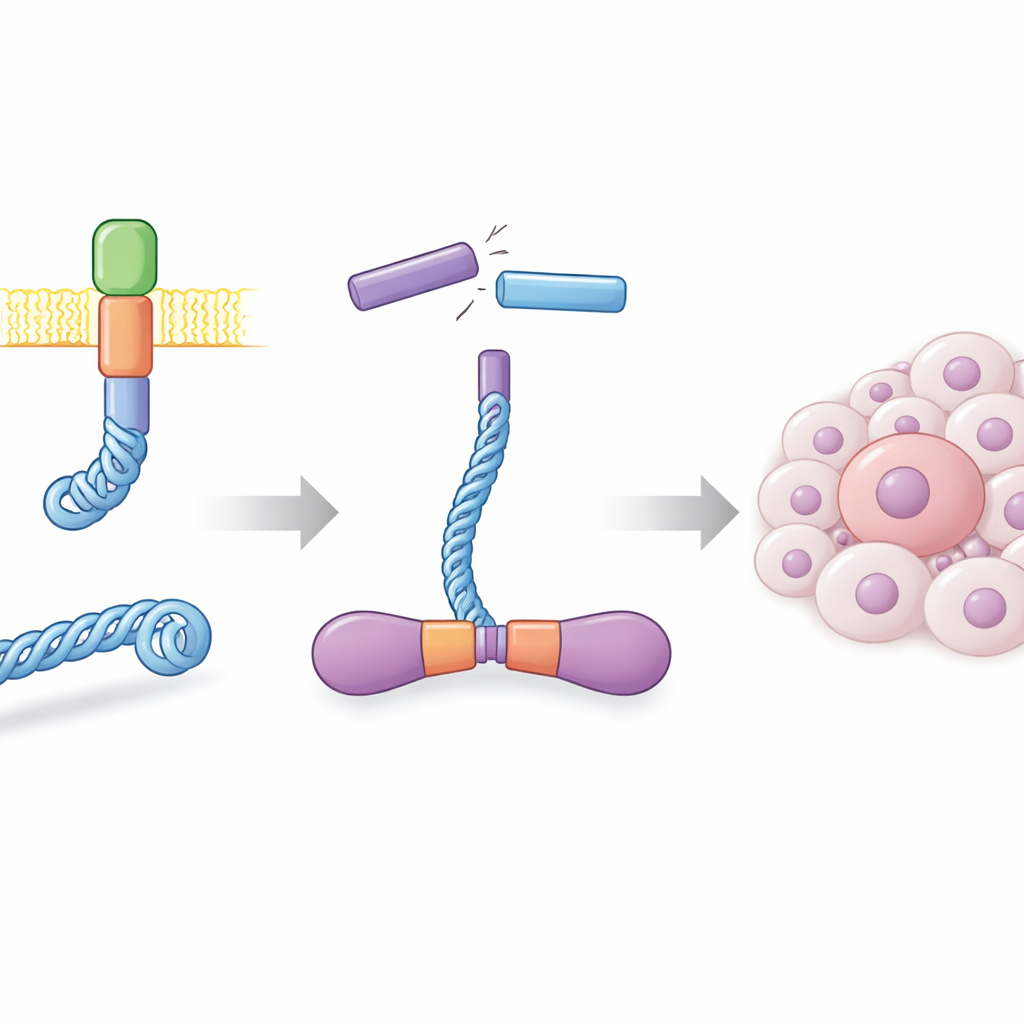
Kinaza zasilana dwoma rodzajami paliwa
Większość kinaz wykorzystuje ATP, podstawową walutę energetyczną komórki, jako źródło fosforu w reakcjach. Kiedy autorzy analizowali aktywność CCDC6-RET za pomocą testów biochemicznych i spektrometrii mas z rozdziałem czasowym, zauważyli coś zaskakującego: fosforylacja białka rosła nie tylko w obecności ATP, lecz także ADP, produktu o niższej energii powstającego po wykorzystaniu ATP. Kolejne eksperymenty wykazały, że CCDC6-RET wiąże oba nukleotydy i może używać każdego z nich jako dawcy fosforu, chociaż z ATP działa szybciej. Przy umiarkowanych stężeniach ADP fuzja pozostaje aktywna, ale bardzo wysokie stężenia ADP zaczynają zakłócać aktywność zależną od ATP, co sugeruje, że ADP może zarówno zasilać, jak i regulować tę onkogenną kinazę w zależności od swojej obfitości.
Wyrafinowane przełączniki kontroli na powierzchni białka
Zespół zmapował dokładnie miejsca, w których CCDC6-RET fosforyluje sam siebie. Znaleziono wiele miejsc nie tylko w centrum katalitycznym RET, lecz także w części CCDC6, w tym wcześniej nieznane. Dwa sąsiednie tyrozyny w giętkim odcinku zwanym pętlą aktywacyjną pełniły odrębne role. Jedno miejsce (Tyr 900) wydaje się kluczowe dla prawidłowego fałdowania i stabilności fuzji, podczas gdy drugie (Tyr 905) jest niezbędne dla efektywnej fosforylacji innych białek. Mutacja Tyr 905 w dużym stopniu oszczędzała zdolność białka do modyfikowania siebie, ale uniemożliwiała jego działanie na dodany peptydowy substrat, ujawniając, że „autoaktywacja” i „sygnalizacja na zewnątrz” są sterowane częściowo oddzielnie. Ta subtelna kontrola może pomóc białku fuzyjnemu pozostać aktywnym bez utraty integralności strukturalnej.
Ujawnianie ruchomych elementów białka w 3D
Aby zrozumieć, jak te chemiczne zmiany przekładają się na kształt, badacze złożyli trójwymiarowy obraz używając przewidywań opartych na sztucznej inteligencji, mikroskopii elektronowej, rozpraszania promieni X małego kąta oraz spektrometrii mas połączonej z utrwalaniem przekątnie (cross-linking). W stanie spoczynkowym dimer CCDC6-RET przyjmuje konfigurację „twarzą do twarzy”: dwie domeny kinazowe leżą blisko siebie u podstawy wspólnego pręta skręconej spirali tworzonego przez segmenty CCDC6, z dotykającymi się pętlami aktywacyjnymi. Po związaniu ATP lub ADP płaty kinaz rozchodzą się jak końcówki pałeczek do jedzenia. Symulacje komputerowe sugerują, że w tym bardziej otwartym stanie każda kinaza może sięgnąć i fosforylować własną pętlę aktywacyjną („in cis”), przygotowując dimer do szybkiej sygnalizacji wobec innych celów komórkowych.
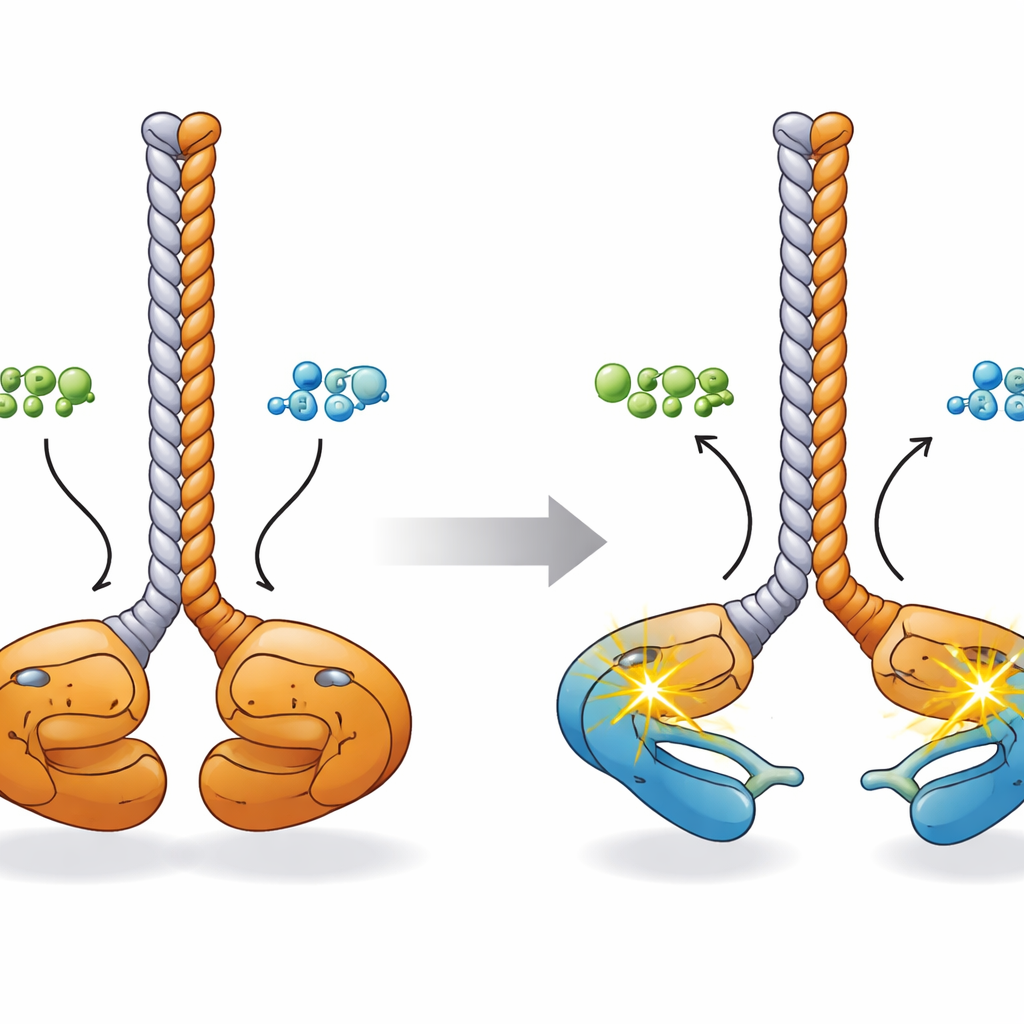
Co to oznacza dla raka i przyszłych terapii
Komórki nowotworowe często żyją na krawędzi kryzysu energetycznego, z niższymi poziomami ATP i wyższymi poziomami ADP niż komórki zdrowe. Kinaza fuzyjna, która może funkcjonować z ATP lub ADP — a nawet zmieniać preferencje substratowe w warunkach bogatych w ADP — może mieć w takich warunkach przewagę przetrwania w surowym mikrośrodowisku guzów litych. Dzięki wyjaśnieniu, jak zbudowany jest CCDC6-RET, jak dimeruje, w jaki sposób zużywa obie formy paliwa komórkowego i które miejsca fosforylacji są najważniejsze, praca ta dostarcza szczegółowego planu do projektowania leków następnej generacji. Takie leki mogłyby nie tylko blokować miejsce aktywne, lecz także rozbijać dimer, zakłócać przełączanie pętli aktywacyjnej lub wykorzystywać nietypowe uzależnienie enzymu od bilansu energetycznego komórki.
Cytowanie: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Słowa kluczowe: fuzja RET, rak brodawkowaty tarczycy, gruczolakorak płuca, aktywacja kinazy białkowej, metabolizm ATP i ADP