Clear Sky Science · zh
真菌肌醇磷酸化鞘磷脂合成的分子见解及抗真菌药物黑曲霉素A对其的抑制作用
为何这个真菌故事很重要
侵袭性真菌感染每年悄然夺去数百万人生命,尤其是在免疫受损者中。然而医生手头只有少数几种抗真菌药物,且许多真菌正在进化出耐药性。本研究关注的是一种在人类细胞中不存在的真菌过程,使其成为开发新药的理想靶点。通过揭示一个关键真菌酶的工作机制——以及一种强效药物如何堵塞它——研究者为更安全、更有效的抗真菌疗法奠定了基础。
真菌防御中的独特点
真菌细胞依赖一类特殊脂类,称为鞘磷脂,来构建和组织它们的膜。其中一种——肌醇磷酸化鞘磷脂(IPC)——存在于真菌中但在人哺乳动物中不存在。IPC由一个名为IPC合酶的双组分酶复合体合成。一方Aur1负责化学反应;另一方Kei1帮助将复合体定位并稳定于膜中。因为真菌无法在没有IPC合酶的情况下存活,而人类根本不具备该酶,长期以来该酶被视为极具吸引力的药物靶点。
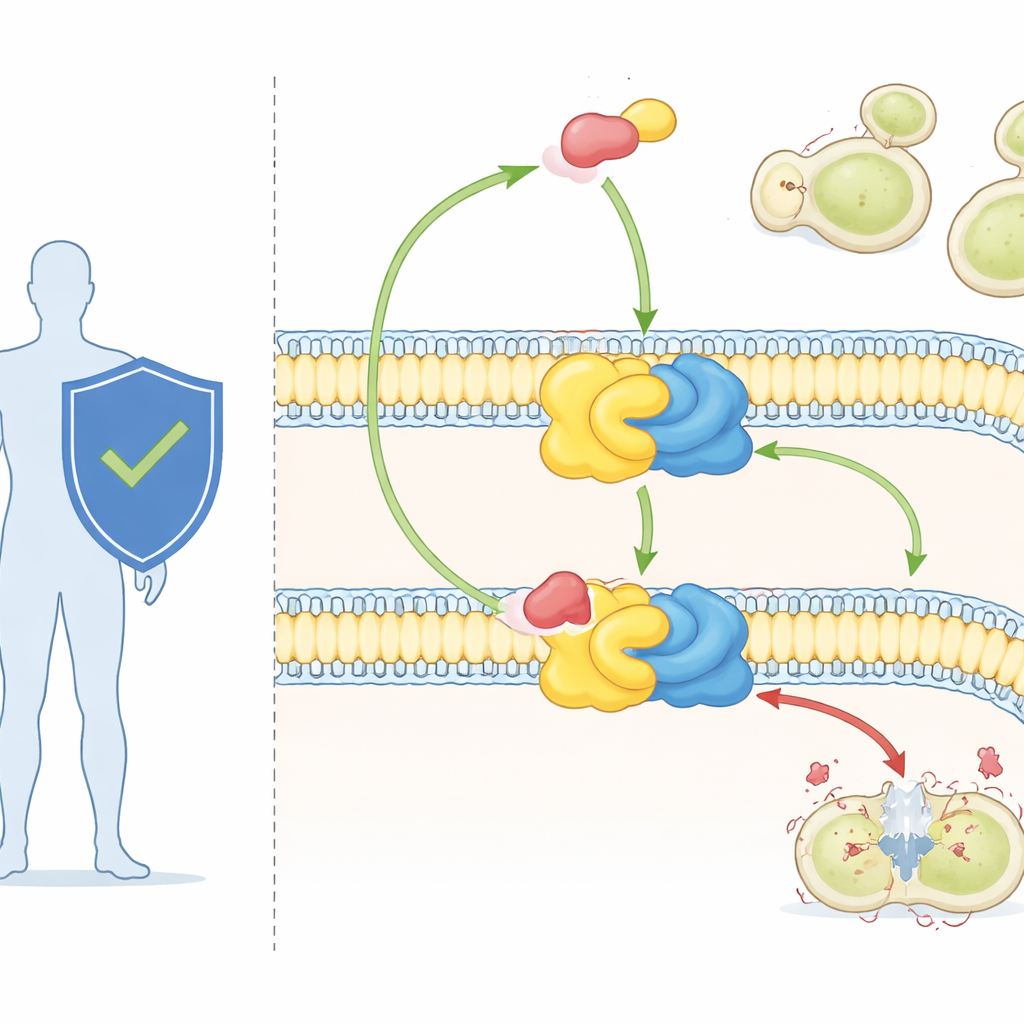
一种强效抗真菌药与神秘靶点
黑曲霉素A(aureobasidin A)目前主要作为研究用药,是已知最强效的抗真菌剂之一。它能以极低剂量杀死主要的真菌病原体,并对哺乳动物细胞显示出较低毒性。遗传学研究已表明,Aur1蛋白的改变可使真菌对该药产生抗性,证实IPC合酶是其靶点。但在没有高分辨率酶结构的情况下,科学家无法确切看清它如何识别其天然脂质底物,或黑曲霉素A如何嵌入并关闭反应。
将酶在工作状态下“冷冻”
为了解决这一问题,研究者使用了冷冻电子显微镜(cryo–EM),这项技术可在近原子分辨率下成像闪速冷冻的分子。IPC合酶体积小且大部分埋入膜中,这使得可视化变得困难。研究团队通过连接一个微小的蛋白标签以及配套的纳米抗体“手柄”来克服这一难题,该策略在不破坏酶活性或其对药物敏感性的前提下改善了图像对齐。随后他们解析了酵母IPC合酶在两种关键状态下的结构:与其脂质底物鞘氨醇(ceramide)结合的状态,以及与黑曲霉素A结合的状态。
酶的工作腔与控制伙伴
结构显示Aur1和Kei1形成一个紧密配对,跨越膜层。Aur1含有一个沟槽状的反应腔,侧向向周围脂质开放。鞘氨醇嵌入这个沟槽,其一条尾链沿着一列疏油性的氨基酸深埋,反应性头部则朝向位于腔底的三个关键残基——两个组氨酸和一个天冬氨酸。改变该“H–H–D三联”中任一残基会完全消除酶活性,表明它们共同完成将带磷酸基团从一种脂质转移到另一种脂质的两步反应。
曾被认为是被动助剂的Kei1被证明是必不可少的。它与Aur1的一个环形成广泛接触,并包裹住一个共同的口袋,该口袋紧密结合着一分子磷脂。当保持该磷脂位置的关键残基被突变时,Aur1–Kei1的组装解体并失去活性。这表明天然膜脂作为结构性的楔子来稳定酶复合体,提示还有其他方式可以用药物来破坏其功能。
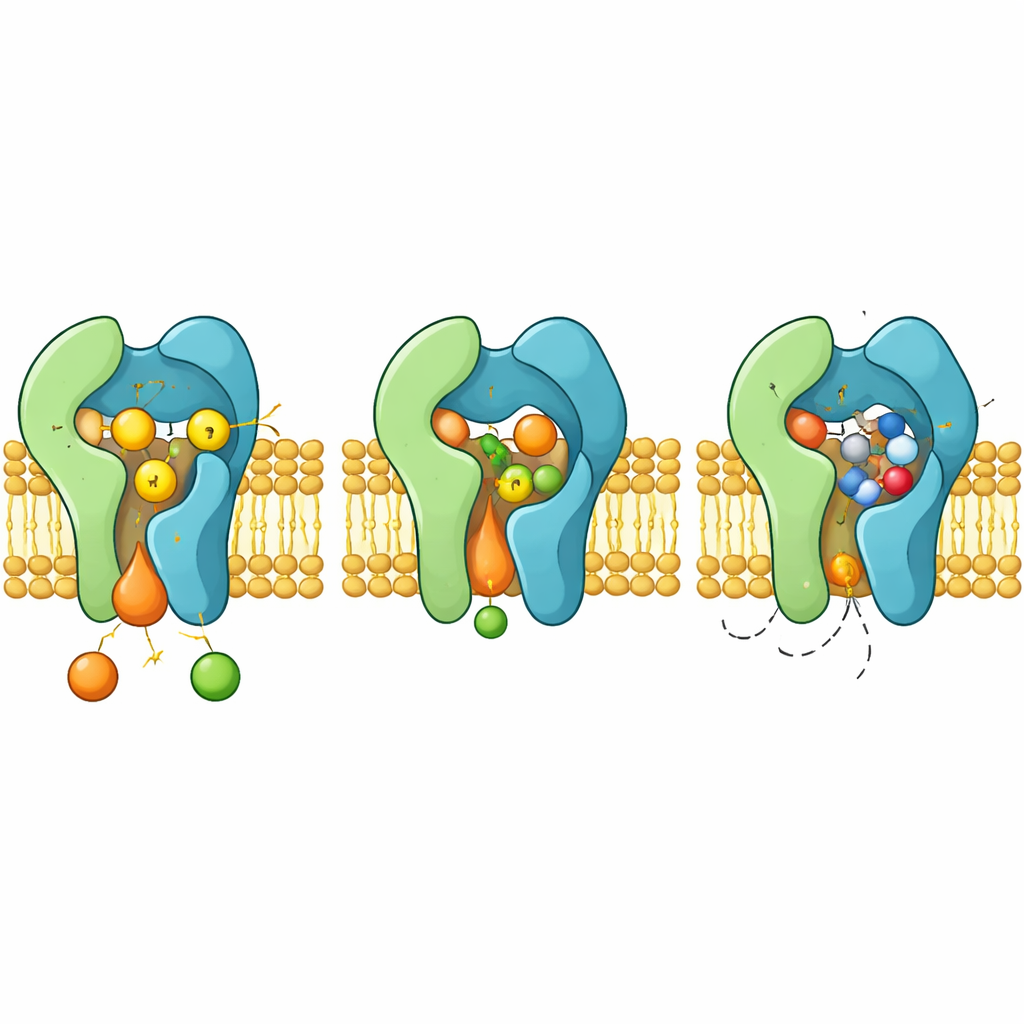
药物如何阻断以及抗性如何产生
当黑曲霉素A结合时,它占据了通常容纳鞘氨醇的同一反应腔。该环状分子被夹入位于灵活环和螺旋之间,推动芳香侧链重排以形成一个贴合的口袋。在这种构型下,药物遮蔽了H–H–D三联并在空间上排斥鞘氨醇,起到经典的竞争性抑制剂作用。结构也解释了为何Aur1中特定的突变,例如靠近口袋的H157或F158的改变,会削弱药物结合而保留催化功能,从而产生耐药真菌。
对未来抗真菌药物的意义
总体而言,这些发现提供了对一种真菌不可或缺而人类不具备的酶的详细地图。通过准确展示IPC合酶如何组装、如何识别其脂质底物以及黑曲霉素A如何塞入其反应腔,研究为设计能选择性破坏真菌膜的新药提供了蓝图。这样的结构指导化合物有望扩展有限的抗真菌武器库,并帮助赶超日益严重的药物耐受性真菌感染问题。
引用: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
关键词: 抗真菌药物, 真菌细胞膜, 鞘磷脂, 药物抗性, 冷冻电子显微镜