Clear Sky Science · pl
Wnikliwość molekularna syntezy inozytolofosforylowanego ceramidu u grzybów i jej zahamowanie przez antygrzybiczny aureobasydyn A
Dlaczego ta historia o grzybach ma znaczenie
Nawracające zakażenia inwazyjne wywołane przez grzyby zabijają po cichu miliony ludzi rocznie, zwłaszcza osoby z osłabionym układem odpornościowym. Tymczasem lekarze dysponują tylko kilkoma klasami leków przeciwgrzybiczych, a wiele gatunków grzybów rozwija oporność. W tej pracy skoncentrowano się na procesie występującym wyłącznie w komórkach grzybów, nieobecnym u ludzi, co czyni go doskonałym celem dla nowych leków. Odkrywając, jak działa kluczowy enzym grzybowy — i jak potężny związek go blokuje — autorzy kładą podwaliny pod bezpieczniejsze i skuteczniejsze terapie przeciwgrzybicze.
Unikalna słabość pancerza grzyba
Komórki grzybów polegają na specjalnej klasie lipidów, zwanych sfingolipidami, do budowy i organizacji swoich błon. Jednym z nich jest inozytolofosforylowany ceramid (IPC), obecny u grzybów, a nieobecny u ssaków. IPC syntetyzowany jest przez dwu‑składnikowy kompleks enzymatyczny znany jako syntaza IPC. Jeden element, Aur1, przeprowadza reakcję chemiczną; drugi, Kei1, pomaga umiejscowić i ustabilizować kompleks w membranie. Ponieważ grzyby nie mogą przeżyć bez syntazy IPC, a ludzie jej nie posiadają, enzym ten od dawna postrzegany jest jako atrakcyjny cel farmakologiczny.
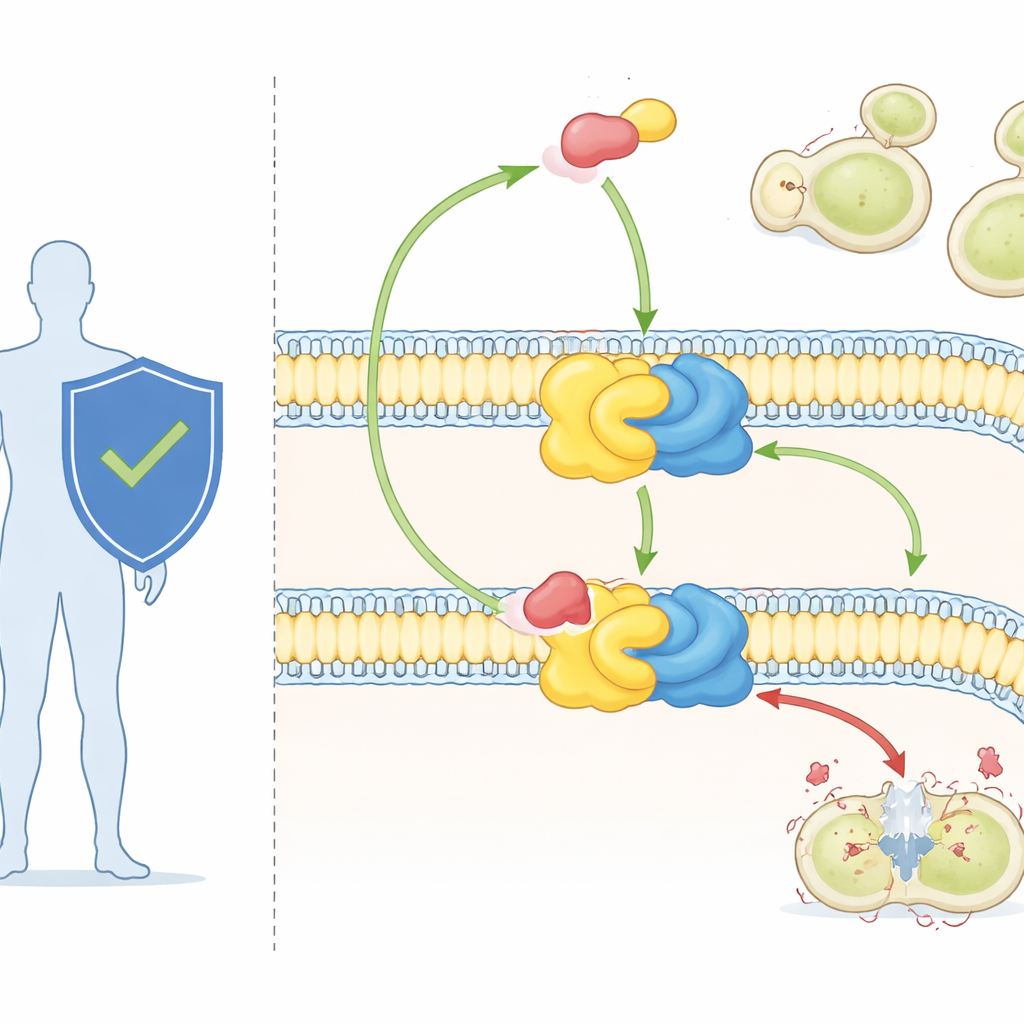
Potężny antygrzybiczy i tajemniczy cel
Aureobasydyn A, stosowany dotąd przede wszystkim w badaniach, jest jednym z najsilniejszych znanych antygrzybiczych związków. Może zabijać istotne patogeny grzybicze w bardzo małych dawkach i wykazuje niewielką toksyczność wobec komórek ssaków. Prace genetyczne wykazały już, że zmiany w białku Aur1 mogą uczynić grzyby odpornymi na związek, potwierdzając, że syntaza IPC jest jego celem. Bez wysokorozdzielczego obrazu enzymu naukowcy jednak nie mogli zobaczyć, jak dokładnie rozpoznaje on swoje naturalne lipidowe substraty ani jak aureobasydyn A klinuje się w nim, by zahamować reakcję.
Zamrażanie enzymu w akcji
Aby rozwiązać ten problem, autorzy zastosowali kriomikroskopię elektronową, technikę obrazowania błyskowo zamrożonych cząsteczek z niemal atomową szczegółowością. Syntaza IPC jest niewielka i w przeważającej części zanurzona w błonie, co utrudnia jej wizualizację. Zespół poradził sobie z tym, dołączając małą etykietę białkową i dopasowaną nanoprzetwornicę („nanobody”) jako uchwyt, co poprawiło wyrównanie obrazów nie zaburzając aktywności enzymu ani jego wrażliwości na lek. Wyznaczyli następnie struktury syntazy drożdżowej IPC w dwóch kluczowych stanach: związanej z jej lipidowym substratem — ceramidem, oraz związanej z aureobasydyną A.
Komora reakcyjna enzymu i partner kontrolny
Struktury ujawniają, że Aur1 i Kei1 tworzą ciasną parę rozpiętą przez błonę. Aur1 zawiera szczelinowatą komorę reakcyjną, która otwiera się bocznie do otaczających lipidów. Ceramid mieści się w tej szczelinie, z jednym łańcuchem zanurzonym głęboko wzdłuż szeregu tłustych reszt aminokwasowych, a jego reaktywna głowa skierowana jest w stronę trzech kluczowych reszt — dwóch histydyn i jednej asparaginianu — umieszczonych u podstawy komory. Mutacje dowolnego członka tej „triady H–H–D” całkowicie eliminują aktywność enzymu, co pokazuje, że współdziałają one przy dwuetapowym przeniesieniu grupy fosforowej między lipidami.
Kei1, wcześniej uważany za biernego pomocnika, okazuje się niezbędny. Tworzy obszerne kontakty z pętlą Aur1 i obejmuje wspólną kieszeń, która mocno wiąże cząsteczkę fosfolipidu. Kiedy kluczowe reszty utrzymujące ten lipid są zmutowane, kompleks Aur1–Kei1 rozpada się i tracona jest aktywność. Sugeruje to, że natywne lipidy błonowe działają jako strukturalne kliny stabilizujące kompleks enzymatyczny, wskazując na dodatkowe sposoby, w jakie leki mogłyby zaburzać jego funkcję.
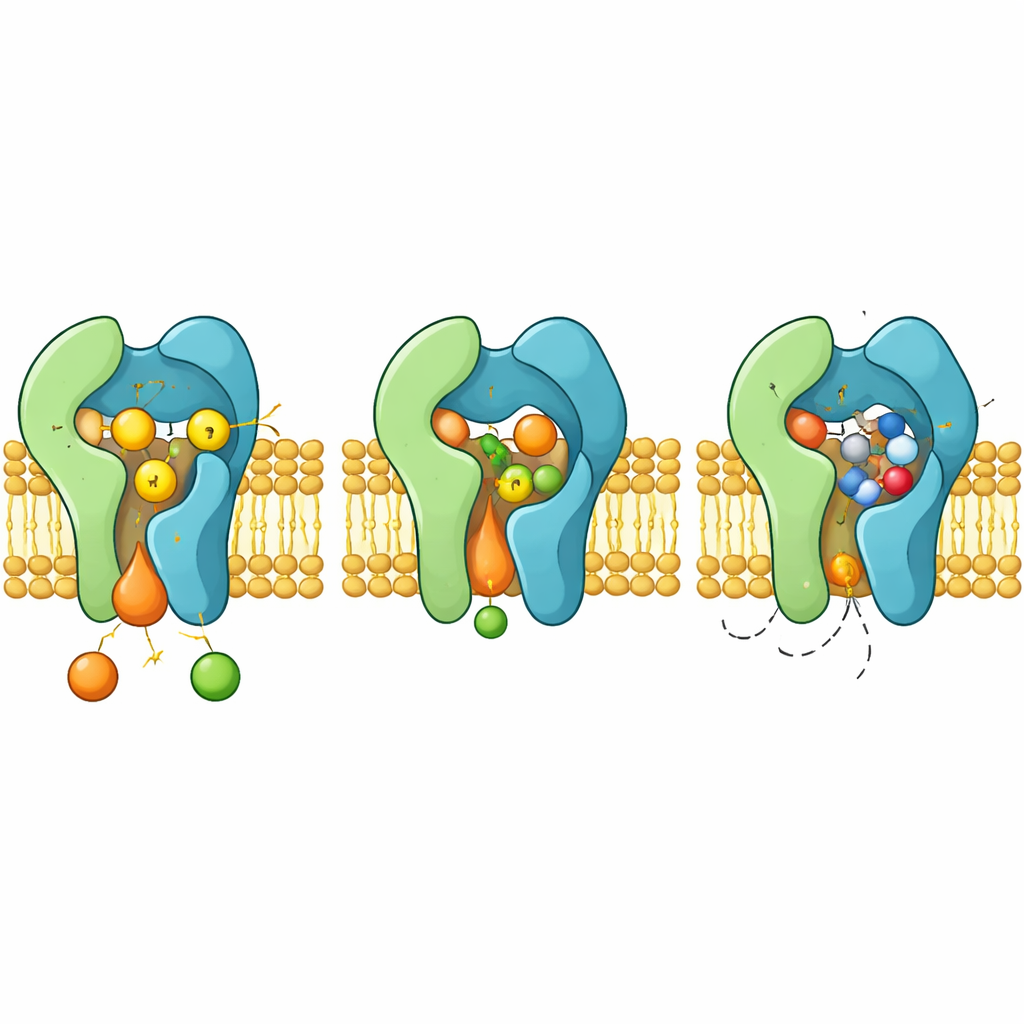
Jak lek blokuje i skąd bierze się oporność
Gdy aureobasydyn A wiąże się z enzymem, zajmuje tę samą komorę reakcyjną, w której normalnie gości ceramid. Cząsteczka cykliczna zaciska się między elastycznymi pętlami i helisami, odsuwając aromatyczne łańcuchy boczne, które przeorientowują się, tworząc ciasną kieszeń. W tej konfiguracji lek zasłania triadę H–H–D i sterycznie wyklucza ceramid, działając jako klasyczny inhibitor kompetycyjny. Struktury wyjaśniają też, jak konkretne mutacje w Aur1, takie jak zmiany reszt H157 czy F158 w pobliżu kieszeni, osłabiają wiązanie leku przy zachowaniu aktywności katalitycznej, prowadząc do powstania opornych grzybów.
Co to oznacza dla przyszłych leków przeciwgrzybiczych
W sumie te odkrycia dostarczają szczegółowej mapy enzymu, bez którego grzyby nie mogą żyć, a którego ludzie nie posiadają. Pokazując, jak syntaza IPC się składa, jak rozpoznaje swoje lipidowe substraty i jak aureobasydyn A klinuje się w jej komorze reakcyjnej, badanie oferuje plan działania dla projektowania nowych leków, które selektywnie osłabią błony grzybów. Związki projektowane w oparciu o strukturę mogłyby rozszerzyć ograniczony arsenał antygrzybiczy i pomóc wyprzedzić narastający problem opornych na leki zakażeń grzybiczych.
Cytowanie: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Słowa kluczowe: leki przeciwgrzybicze, błona komórkowa grzybów, sfingolipidy, oporność na leki, kriomikroskopia elektronowa