Clear Sky Science · ar
رؤى جزيئية في تخليق الفسفاتيديل سيراميد الإينوزيتول الفطري وتثبيطه بالمضاد الفطري أوريوبيسيدين A
لماذا هذه القصة الفطرية مهمة
تقتل العدوى الفطرية الغازية ملايين الأشخاص كل عام بصمت، خصوصًا من لديهم أجهزة مناعية ضعيفة. ومع ذلك يمتلك الأطباء فقط عددًا محدودًا من الأدوية المضادة للفطريات، والعديد من الفطريات تطور مقاومة. تركز هذه الدراسة على عملية فطرية غير موجودة في الخلايا البشرية، ما يجعلها هدفًا مثاليًا للأدوية الجديدة. من خلال كشف كيفية عمل إنزيم فطري رئيسي — وكيف يقوم دواء قوي بتعطيله — يمهد الباحثون الطريق لعلاجات مضادة للفطريات أكثر أمانًا وفعالية.
نقطة ضعف فريدة في درع الفطريات
تعتمد الخلايا الفطرية على فئة خاصة من الدهون تسمى السفينجوليبيدات لبناء وتنظيم أغشيتها. أحد هذه المركبات، فسفاتيديل سيراميد الإينوزيتول (IPC)، يوجد في الفطريات لكنه غائب في الثدييات. يُصنع IPC بواسطة مركب إنزيمي مكوّن من جزأين يعرف باسم سينثاز IPC. أحد الشريكين، Aur1، يقوم بالتفاعل الكيميائي؛ والآخر، Kei1، يساعد في وضع وتثبيت المركب في الغشاء. لأن الفطريات لا تستطيع العيش بدون سينثاز IPC، بينما لا يملكه البشر على الإطلاق، فقد اعتُبر هذا الإنزيم هدفًا دوائيًا جذابًا منذ زمن.
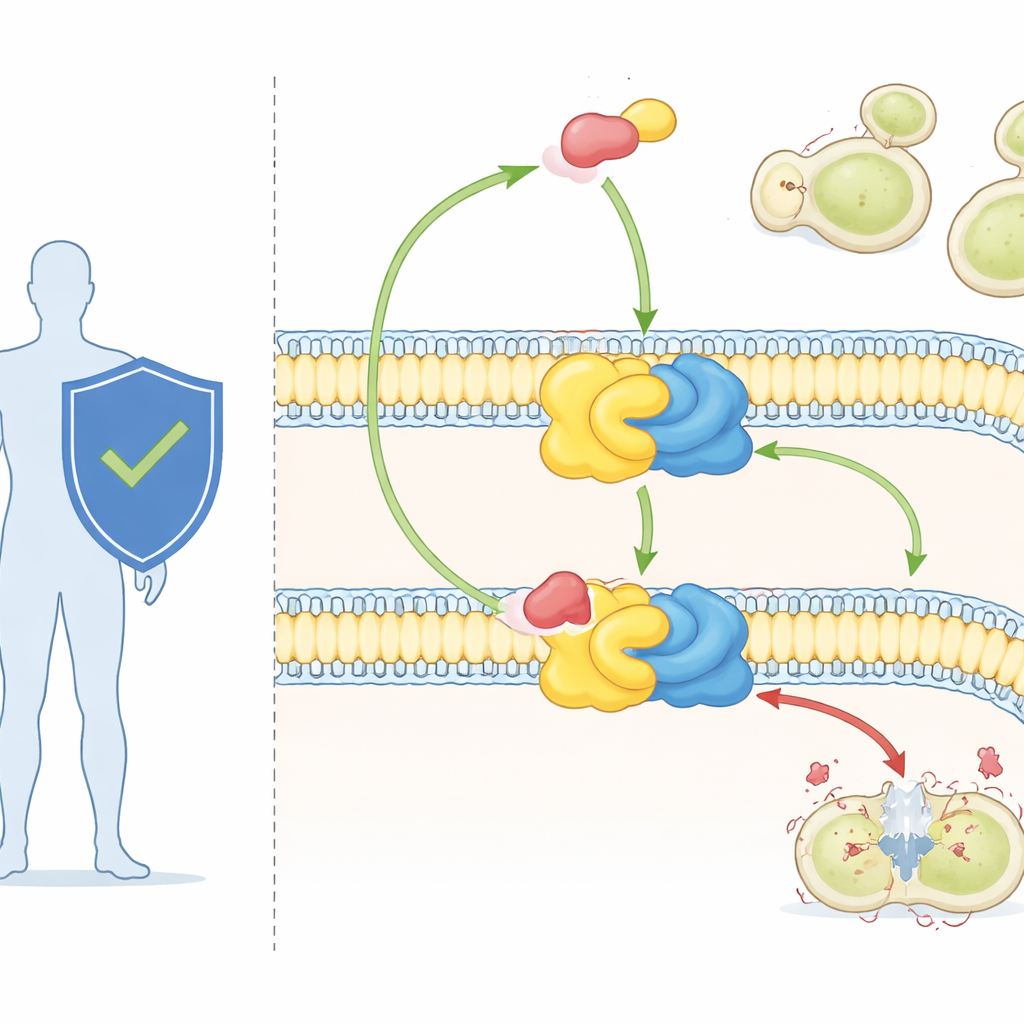
مضاد فطري قوي وهدف غامض
الدواء أوريوبيسيدين A، المستخدم حتى الآن أساسًا في البحث، هو أحد أقوى المضادات الفطرية المعروفة. يمكنه قتل مسببات الأمراض الفطرية الكبرى بجرعات ضئيلة ويظهر سمية منخفضة للخلايا الثديية. أظهرت دراسات وراثية مسبقًا أن تغييرات في بروتين Aur1 قد تجعل الفطريات مقاومة للدواء، ما أكد أن سينثاز IPC هو هدفه. لكن من دون رؤية ذات دقة عالية للإنزيم، لم يستطع العلماء أن يروا بالضبط كيف يتعرف على ركائزه الدهنية الطبيعية أو كيف يندس أوريوبيسيدين A لإيقاف التفاعل.
تجميد الإنزيم أثناء العمل
لحل هذه المسألة، استخدم الباحثون المجهر الإلكتروني بالتبريد، وهي تقنية تظهر جزيئات مُجمّدة فوريًا بتفاصيل قريبة من الذرية. سينثاز IPC صغير ومحمور في الغشاء في الغالب، ما يجعل رؤيته صعبة. تغلب الفريق على ذلك عبر إرفاق وسم بروتيني صغير ومضاد جسم نانوي ملائم كـ"مقبض" حسن من محاذاة الصور من دون أن يعيق نشاط الإنزيم أو حساسيته للدواء. ثم حددوا تراكيب سينثاز IPC من الخميرة في حالتين رئيسيتين: مربوطًا بركيزة الدهن سيراميد، ومربوطًا بأوريوبيسيدين A.
حجرة عمل الإنزيم والشريك المسيطر
تكشف التراكيب عن Aur1 وKei1 يشكلان زوجًا محكمًا يعبر الغشاء. يحتوي Aur1 على أخدود شبيه بحجرة تفاعل تفتح جانبًا إلى الدهون المحيطة. يستقر السيراميد داخل هذا الأخدود، بذيل واحد مدفون عميقًا بمحاذاة سلسلة من الأحماض الأمينية الزيتية ورأسه التفاعلي متجهًا نحو ثلاث بقايا حاسمة — اثنتان من الهيستيدين والبِقْيَة أسْبارتيك — تقعان في قاعدة الحجرة. تؤدي طفرات في أي عضو من هذا "الثلاثي H–H–D" إلى إلغاء نشاط الإنزيم تمامًا، مما يدل على أن هذه البقايا تعمل معًا لإجراء نقل من خطوتين لمجموعة حاملة للفوسفات من دهن إلى آخر.
يتبين أن Kei1، الذي كان يُعتقد سابقًا أنه مساعد سلبي، أساسي فعليًا. فهو يشكل اتصالات واسعة مع حلقة من Aur1 ويحتضن جيبًا مشتركًا يرتبط بإحكام بجزيء فوسفوليبيد. عند إدخال طفرات في البقايا الأساسية التي تثبّت هذا الدهن في مكانه، تنهار مجموعة Aur1–Kei1 وتفقد نشاطها. هذا يوحي بأن دهون الغشاء الأصلية تعمل كوتدات هيكلية تثبت المركب الإنزيمي، مما يشير إلى طرق إضافية قد يمكن للأدوية من خلالها تعطيل وظيفته.
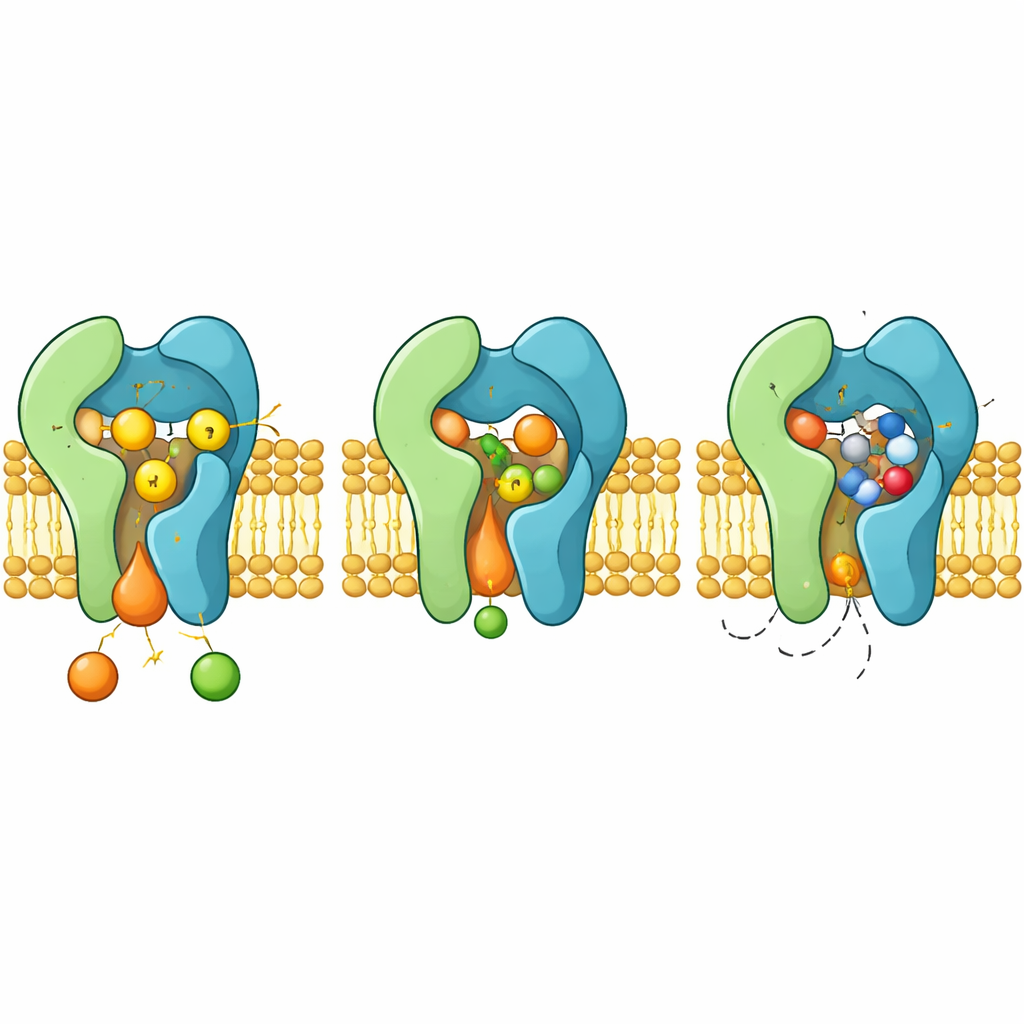
كيف يعيق الدواء وكيف تنشأ المقاومة
عندما يرتبط أوريوبيسيدين A، يشغل نفس حجرة التفاعل التي يستضيف عادة السيراميد. تثبت الجزيئة الحلقية في مكانها بين حلقات ومحاور مرنة، داعية سلاسل جانبية عطرية لتتحرك وتُعيد توجيه نفسها لتكوّن جيبًا محكمًا. في هذا الترتيب، يحجب الدواء الثلاثي H–H–D ويمنع السيراميد ستريريًا، ليعمل كمثبط تنافسي كلاسيكي. تشرح التراكيب أيضًا كيف تؤدي طفرات محددة في Aur1، مثل تغيير البقايا H157 أو F158 قرب الجيب، إلى إضعاف ارتباط الدواء مع الحفاظ على التحفيز، مما يؤدي إلى ظهور فطريات مقاومة.
ما يعنيه هذا لأدوية مضادة للفطريات في المستقبل
توفر هذه النتائج معًا خارطة مفصلة لإنزيم لا تستطيع الفطريات العيش بدونه ولا يمتلكه البشر. من خلال إظهار كيفية تجمّع سينثاز IPC، وكيف يتعرف على ركائزه الدهنية، وكيف يندس أوريوبيسيدين A في حجرة تفاعله، تقدم الدراسة مخططًا لتصميم أدوية جديدة تعطل أغشية الفطريات بشكل انتقائي. مثل هذه المركبات الموجَّهة بالبنية قد توسع ترسانة الأدوية المحدودة المتاحة وتساعد في مجاراة مشكلة تزايد العدوى الفطرية المقاومة للأدوية.
الاستشهاد: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
الكلمات المفتاحية: أدوية مضادة للفطريات, غشاء الخلية الفطري, الدهون الشبيهة بالسفينجوليبيد, مقاومة الأدوية, المجهر الإلكتروني بالتبريد