Clear Sky Science · he
תובנות מולקולריות על סינתזת אינוזיטול פוספורילצרמיד פטרייתית ועיכובה על‑ידי האנטיפונגי Aureobasidin A
מדוע הסיפור הזה של פטריות חשוב
זיהומים פטרייתיים חודרניים הורגים בחשאי מיליונים של אנשים בכל שנה, במיוחד כאלה עם מערכת חיסון מוחלשת. יחד עם זאת, לרופאים יש רק מספר מצומצם של תרופות אנטיפונגיות, ורבים מן המינים הפטרייתיים מתפתחים לעמידות. המחקר הזה מתמקד בתהליך פטרייתי שאינו קיים בתאי אדם, מה שהופך אותו למטרה אידיאלית לתרופות חדשות. על ידי גילוי האופן שבו אנזים פטרייתי מרכזי פועל — ואיך תרופה חזקה חוסמת אותו — החוקרים מספקים בסיס לפיתוח טיפולים אנטיפונגיים בטוחים ויעילים יותר.
נקודת תורפה ייחודית בחזות הפטרייה
תאי פטרייה נשענים על קבוצת שומנים מיוחדת, שנקראת ספינגוליפידים, כדי לבנות ולארגן את ממברנותיהם. אחד מהשומנים האלה, אינוזיטול פוספורילצרמיד (IPC), נמצא בפטריות אך נעדר ביונקים. IPC מיוצר על‑ידי קומפלקס אנזימטי דו‑חלקי המכונה IPC synthase. שותף אחד, Aur1, מבצע את התגובה הכימית; השני, Kei1, מסייע במיקום ויציבות הקומפלקס בממברנה. מאחר שפטריות לא יכולות להתקיים ללא IPC synthase, בעוד שבני אדם לא מכילים אנזים זה כלל, נחשב האנזים זה זמן רב למטרה מבטיחה לתרופות.
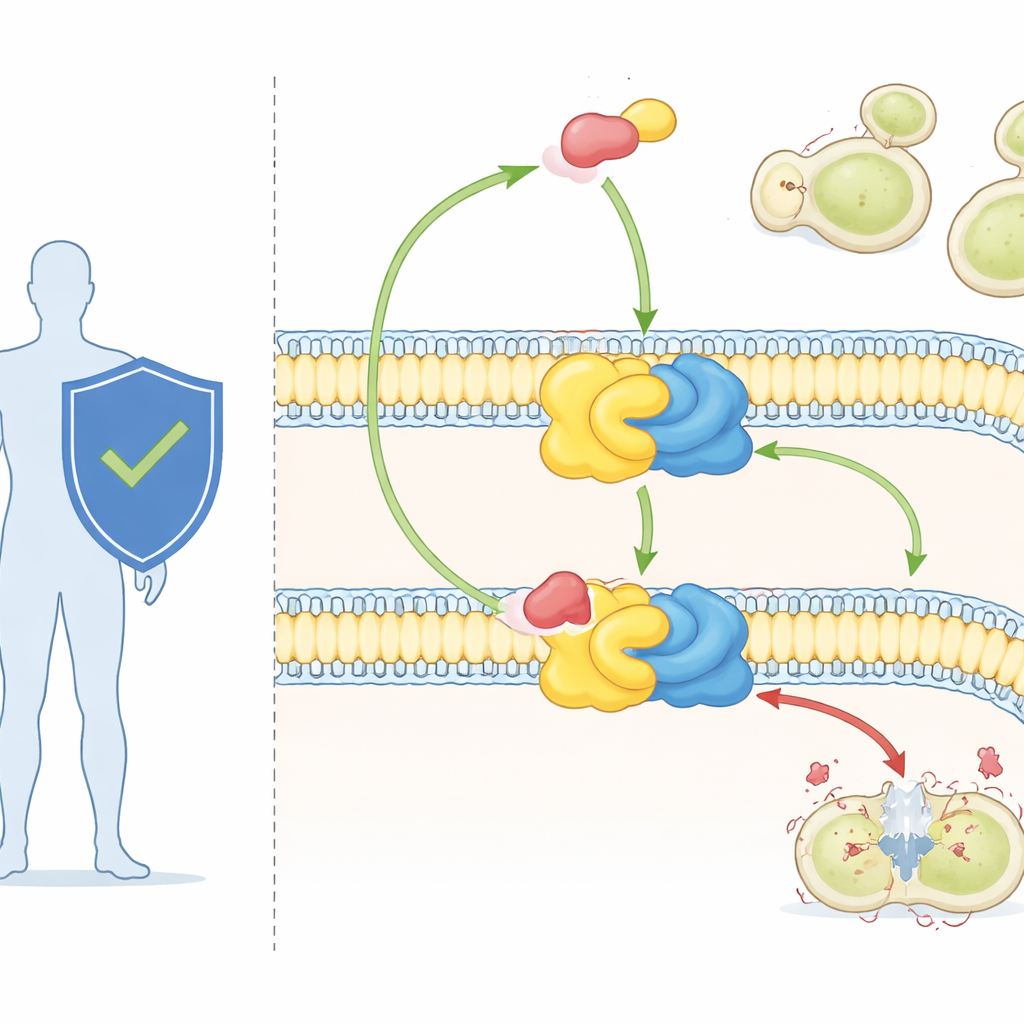
אנטיפונגי עוצמתי ומטרה מסתורית
התרופה aureobasidin A, שמשמשת עד כה בעיקר במחקר, היא אחת התרופות האנטיפונגיות הפעילות הידועות. היא יכולה להרוג פתוגנים פטרייתיים משמעותיים במינונים זעירים ומראה רעילות מועטה לתאים יונקיים. עבודות גנטיות הראו כבר ששינויים בחלבון Aur1 יכולים להפוך פטריות לעמידות כלפי התרופה, מה שאישר כי IPC synthase הוא היעד שלה. אך ללא מבט ברזולוציה גבוהה על האנזים, לא היה ניתן לראות בדיוק כיצד הוא מזהה את תת‑המוליכים הליפידיים הטבעיים שלו או כיצד aureobasidin A משתבצת ומכבידה על התגובה.
הקפאת האנזים בפעולה
כדי לפתור בעיה זו השתמשו החוקרים במיקרוסקופיית אלקטרונים מוקפאת (cryo–EM), טכניקה שממפה מולקולות מוקפאות במהירות ברזולוציה כמעט אטומית. IPC synthase קטן ורובו שקוע בממברנה, מה שמקשה על הדמייתו. הצוות התגבר על כך על‑ידי הצמדה של תגוני חלבון זעיר ותמיכה בננובודי מתאים ששיפרו יישור תמונות מבלי להפריע לפעילות האנזימטית או לרגישותו לתרופה. לאחר מכן קבעו מבנים של ה‑IPC synthase של שמרים בשני מצבים מרכזיים: קשור לתת‑המוליך הליפידי שלו, סרמיד, וקשור ל‑aureobasidin A.
חלל הפעולה של האנזים ושותפו השולט
המבנים מגלהים כי Aur1 ו‑Kei1 יוצרים זוג הדוק השוזר את הממברנה. Aur1 מכיל תעלה דמוית חריץ שמשמשת כחדר תגובה שנפתח הצידה אל נוסחאות השומן הסובבות. סרמיד נשאב לתוך החריץ הזה, עם זנב אחד שקוע עמוק לאורך שרשרת חומצות אמינו שומניות וראש ריאקטיבי שמצביע לכיוון שלוש שיירות חיוניות — שתי היסטידינים ואספרטאט אחד — אשר יושבות בבסיס החדר. שינוי גנטי של כל אחד מרכיבי "הטריאדה H–H–D" הזו מבטל לחלוטין את הפעילות האנזימטית, מה שמראה כי הן יחד מבצעות את העברה דו‑שלבית של קבוצת פוספט בין ליפידים.
Kei1, שלפני כן נחשבה לעוזרת פסיבית, מתבררת כחיונית. היא יוצרת מגעים נרחבים עם לולאה של Aur1 ומחבקת כיס משותף שקושר בריתותית מולקולת פוספוליפיד. כאשר משנים שיירים מרכזיים שמחזיקים את הליפיד הזה במקום, הקומפלקס Aur1–Kei1 מתפרק והפעילות אובדת. ממצא זה מרמז שליפידים מקוריים בממברנה פועלים כיסות מבניות שמייצבות את הקומפלקס האנזימטי, ומצביע על דרכים נוספות בהן תרופות עשויות להפריע לתפקודו.
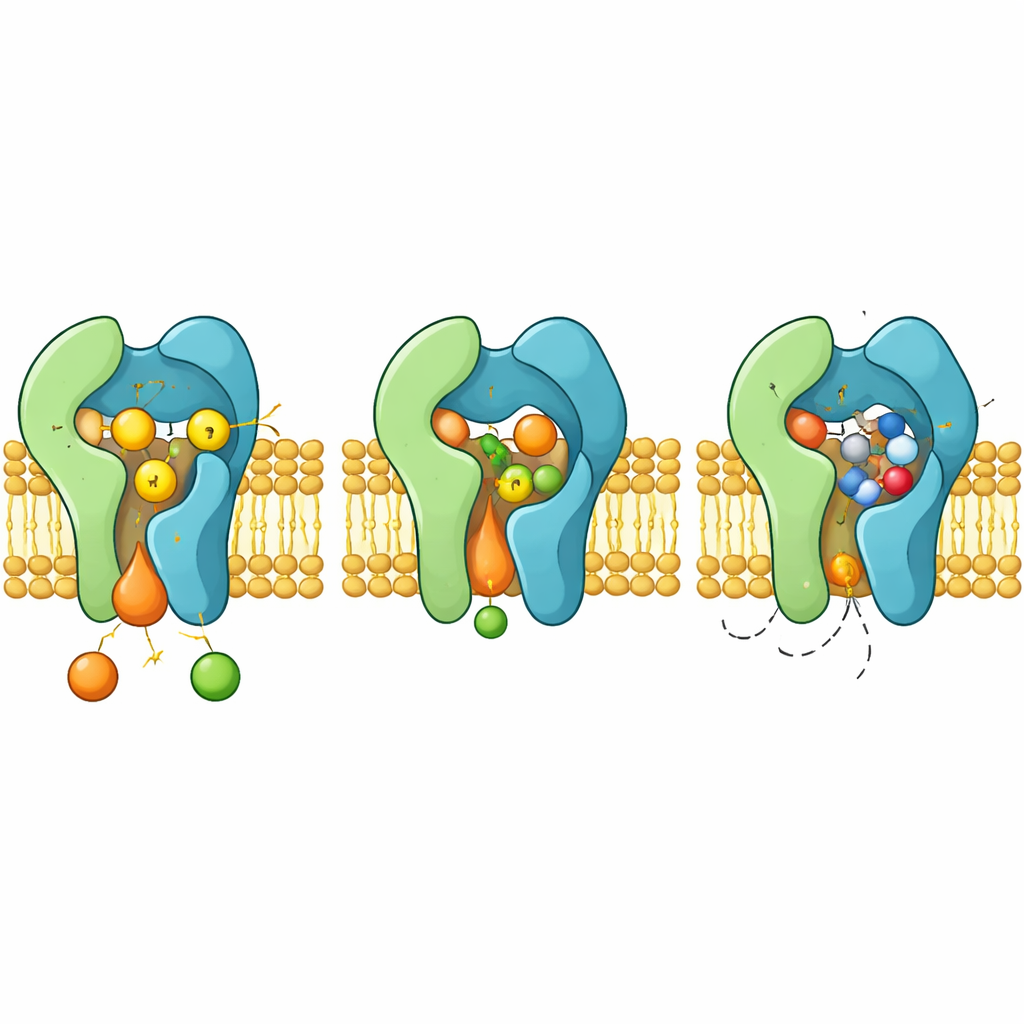
כיצד התרופה חוסמת וכיצד מתפתחת העמידות
כאשר aureobasidin A נקשרת, היא תופסת את אותו חדר תגובה שבו בדרך‑כלל מתמקם הסרמיד. המולקולה המחזורית ננעלת בין לולאות וגבעולי אלפא גמישים, דוחקת שיירים ארומטיים שמסתדרים מחדש כדי ליצור כיס צמוד. בתצורה זו, התרופה חוסמת את הטריאדה H–H–D ומונעת סטראית כניסת סרמיד, ותפקוד כמעכב תחרותי קלאסי. המבנים גם מסבירים כיצד מוטציות ספציפיות ב‑Aur1, כגון שינוי השיירים H157 או F158 הסמוכים לכיס, מחלישות את קשירת התרופה בזמן ששומרות על הקטליזה, ומובילות להופעת פטריות עמידות.
ממצא המשמעותי לפיתוח תרופות אנטיפונגיות עתידיות
ביחד, ממצאים אלה מספקים מפת מבנה מפורטת של אנזים שפטריות לא יכולות בלעדיו ובני אדם אינם מחזיקים בו כלל. על‑ידי הצגה מדויקת של האופן שבו IPC synthase מתרכב, כיצד הוא מזהה את תת‑המוליכים הליפידיים שלו, וכיצד aureobasidin A משתבצת בחדר התגובה שלו, המחקר מציע תבנית לעיצוב תרופות חדשות שיפגעו באופן סלקטיבי בממברנות פטרייתיות. תרכובות המונחות על־ידי מבנה כזו עשויות להרחיב את ארסנל התרופות המצומצם הקיים ולעזור להקדים את הבעיה ההולכת וגדלה של זיהומים פטרייתיים עמידים לתרופות.
ציטוט: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
מילות מפתח: תרופות אנטיפונגיות, ממברנת תא פטרייתית, ספינגוליפידים, עמידות לתרופות, מיקרוסקופיית אלקטרונים מוקפאת (cryo‑EM)