Clear Sky Science · sv
Molekylära insikter i svampens inositolfosforylceramid-syntes och dess hämning av det antifungala ämnet aureobasidin A
Varför den här svamphistorien är viktig
Invasiva svampinfektioner dödar tyst miljontals människor varje år, särskilt personer med försvagat immunsystem. Läkare har ändå bara ett fåtal antifungala läkemedel, och många svampar utvecklar resistens. Den här studien fokuserar på en svampprocess som inte finns i mänskliga celler, vilket gör den till ett idealiskt mål för nya läkemedel. Genom att avslöja hur ett nyckelenzym i svampen fungerar — och hur ett potent läkemedel blockerar det — lägger forskarna grunden för säkrare och mer effektiva antifungala terapier.
En unik svag punkt i svampens rustning
Svampceller är beroende av en särskild klass fetter, så kallade sfingolipider, för att bygga upp och organisera sina membran. En av dessa, inositolfosforylceramid (IPC), finns i svampar men saknas hos däggdjur. IPC tillverkas av ett tvådelat enzymkomplex känt som IPC-syntas. Den ena partnern, Aur1, utför den kemiska reaktionen; den andra, Kei1, hjälper till att positionera och stabilisera komplexet i membranet. Eftersom svampar inte kan leva utan IPC-syntas, medan människor inte har det alls, har detta enzym länge setts som ett attraktivt läkemedelsmål.
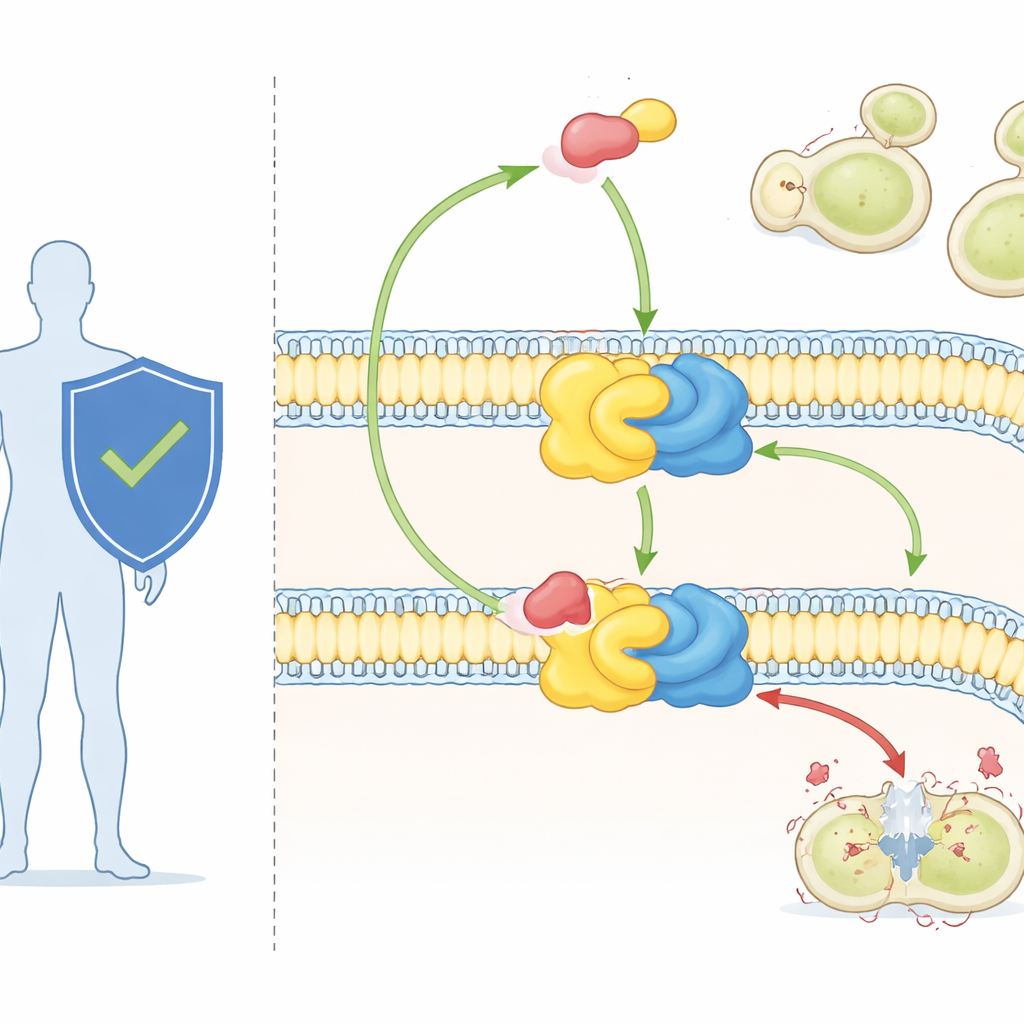
Ett kraftfullt antifungalt medel och ett mystiskt mål
Läkemedlet aureobasidin A, hittills främst använt i forskning, är ett av de mest potenta kända antifungalerna. Det kan döda stora svamppatogener vid mycket små doser och visar låg toxicitet mot däggdjursceller. Genetiska studier hade redan visat att förändringar i Aur1-proteinet kan göra svampar resistenta mot läkemedlet, vilket bekräftar att IPC-syntas är dess mål. Men utan en högupplöst bild av enzymet kunde forskarna inte se exakt hur det känner igen sina naturliga lipidsubstrat eller hur aureobasidin A kilas in för att stoppa reaktionen.
Frysa enzymet i arbete
För att lösa detta problem använde forskarna kryoelektronmikroskopi, en teknik som avbildar snabbfrysta molekyler i närapå atomdetalj. IPC-syntas är litet och till största delen begravt i membranet, vilket gör det svårt att visualisera. Gruppen övervann detta genom att fästa en liten proteintagg och en matchande nanobindande ”handtag” som förbättrade bildinriktningen utan att störa enzymets aktivitet eller dess känslighet för läkemedlet. De bestämde sedan strukturerna för jästens IPC-syntas i två viktiga tillstånd: bundet till sitt lipidsubstrat ceramid och bundet till aureobasidin A.
Enzymets arbetskammare och kontrollpartnern
Strukturerna visar Aur1 och Kei1 som en tät duo som spänner över membranet. Aur1 innehåller en spårliknande reaktionskammare som öppnar sig i sidled mot de omgivande lipiderna. Ceramid vilar i denna fåra, med ett svansparti djupt begravt längs en rad oljiga aminosyror och sin reaktiva huvudgrupp pekande mot tre avgörande rester — två histidiner och en aspartat — som sitter vid kammarens botten. Att mutera någon medlem i denna ”H–H–D-triad” eliminerar helt enzymaktiviteten, vilket visar att de tillsammans utför den tvåstegsöverföring av en fosfatbärande grupp från en lipid till en annan.
Kei1, som tidigare antagits vara en passiv hjälpare, visar sig vara essentiell. Det bildar omfattande kontakter med en loop från Aur1 och omfamnar en delad ficka som hårt binder en fosfolipidmolekyl. När nyckelrester som håller denna lipid på plats muteras faller Aur1–Kei1-assemblén sönder och aktiviteten går förlorad. Detta antyder att native membranlipider fungerar som strukturella kilar som stabiliserar enzymkomplexet, vilket pekar på ytterligare sätt att läkemedel kan störa dess funktion.
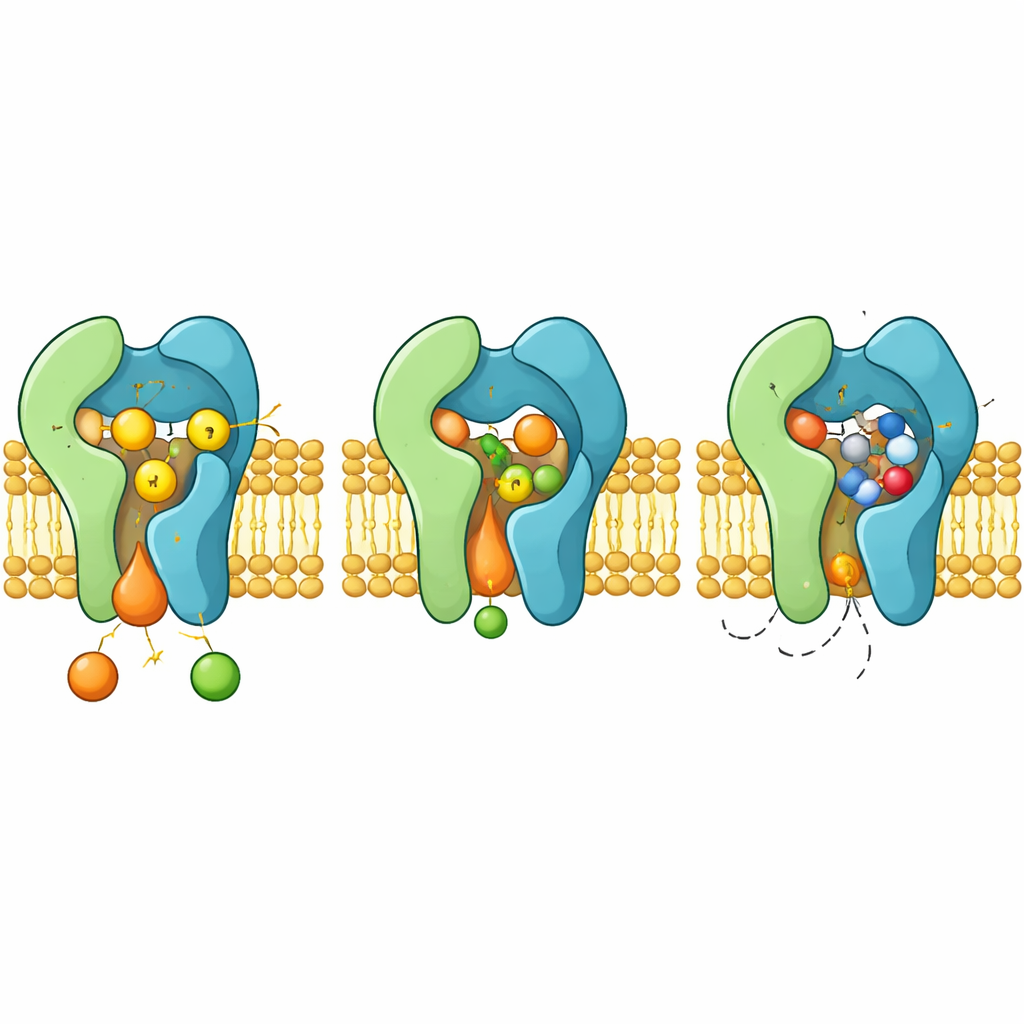
Hur läkemedlet blockerar och hur resistens uppstår
När aureobasidin A binder upptar det samma reaktionskammare som normalt hyser ceramid. Den cykliska molekylen klämmer fast mellan flexibla loopar och helixar, och tränger undan aromatiska sidokedjor som omorienteras för att skapa en tät ficka. I denna konfiguration blockerar läkemedlet H–H–D-triaden och utestänger ceramid steriskt, vilket fungerar som en klassisk konkurrerande hämmare. Strukturerna förklarar också hur specifika mutationer i Aur1, såsom förändringar i resterna H157 eller F158 nära fickan, försvagar läkemedlets bindning samtidigt som katalysen bevaras, vilket ger upphov till resistenta svampar.
Vad detta betyder för framtida antifungala läkemedel
Tillsammans ger dessa fynd en detaljerad karta över ett enzym som svampar inte kan leva utan och som människor inte har. Genom att visa exakt hur IPC-syntas monteras, hur det känner igen sina lipidsubstrat och hur aureobasidin A kilas in i dess reaktionskammare, erbjuder studien en ritning för att designa nya läkemedel som selektivt förlamar svampmembran. Sådana strukturstyrda föreningar kan utöka den begränsade antifungala arsenalen och hjälpa till att förhala det växande problemet med läkemedelsresistenta svampinfektioner.
Citering: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Nyckelord: antifungala läkemedel, svampens cellmembran, sfingolipider, läkemedelsresistens, kryoelektronmikroskopi