Clear Sky Science · tr
Mantar inositol fosforilseramid sentezi ve antifungal aureobasidin A tarafından inhibisyonuna ilişkin moleküler içgörüler
Bu mantar hikâyesi neden önemli
İnvazif mantar enfeksiyonları, özellikle bağışıklığı zayıf kişilerde, her yıl sessizce milyonlarca insanın ölümüne yol açıyor. Buna rağmen hekimlerin kullanabileceği antifungal ilaç sayısı sınırlı ve birçok mantar türü direnç geliştirmeye devam ediyor. Bu çalışma, insan hücrelerinde bulunmayan bir mantar sürecine odaklanıyor; bu da yeni ilaçlar için ideal bir hedef noktası oluşturuyor. Araştırmacılar, anahtar bir mantar enziminin nasıl çalıştığını ve güçlü bir ilacın onu nasıl kilitlediğini ortaya koyarak daha güvenli ve etkili antifungal tedaviler için zemin hazırlıyor.
Mantarda benzersiz bir zayıf nokta
Mantar hücreleri zarlarını oluşturmak ve düzenlemek için sfinolipitler adı verilen özel bir yağ sınıfına dayanır. Bunlardan biri olan inositol fosforilseramid (IPC), mantarlarda bulunur ancak memelilerde yoktur. IPC, IPC sentaz olarak bilinen iki parçalı bir enzim kompleksince üretilir. Ortaklardan biri, Aur1, kimyayı gerçekleştirir; diğeri Kei1 ise kompleksi zar içinde konumlandırıp stabilize etmeye yardımcı olur. Mantarlar IPC sentaz olmadan yaşayamadığı için ve insanların bu enzime sahip olmaması nedeniyle, bu enzim uzun zamandır çekici bir ilaç hedefi olarak görülüyor.
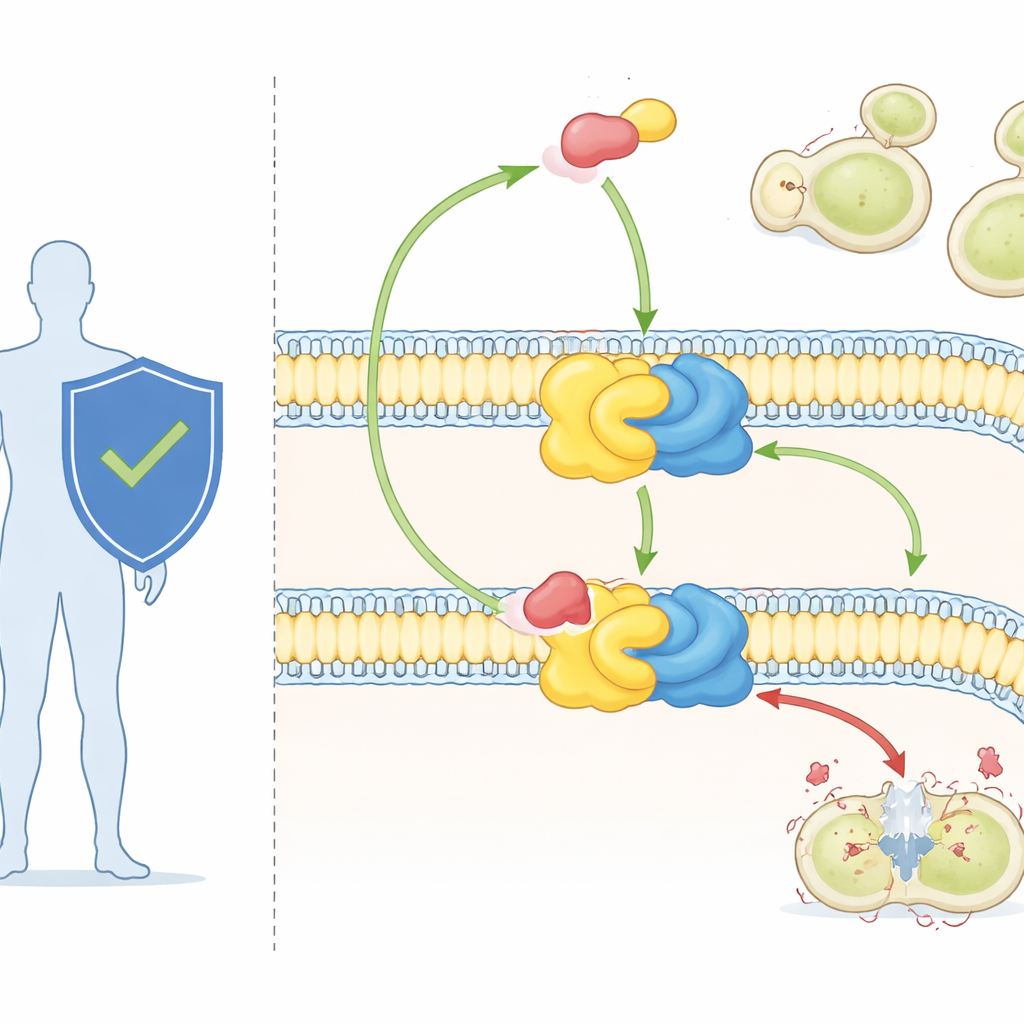
Güçlü bir antifungal ve gizemli hedef
Şimdiye dek çoğunlukla araştırmalarda kullanılan aureobasidin A, bilinen en güçlü antifungallerden biridir. Çok küçük dozlarda büyük mantar patojenlerini öldürebilir ve memeli hücreleri üzerinde düşük toksisite gösterir. Genetik çalışmalar, Aur1 proteinindeki değişikliklerin mantarları ilaca dirençli hale getirebildiğini göstermiş; bu da IPC sentazın ilacın hedefi olduğunu doğrulamıştır. Ancak enzimin yüksek çözünürlüklü bir görünümü olmadan, bilim insanları doğal lipid substratları nasıl tanıdığını veya aureobasidin A’nın reaksiyonu nasıl bloke etmek için kendisini nasıl taktırdığını tam olarak göremiyordu.
Enzimi hareket halinde dondurmak
Bu sorunu çözmek için araştırmacılar, molekülleri neredeyse atomik ayrıntıda görüntüleyen kriyo–elektron mikroskobu tekniğini kullandılar. IPC sentaz küçük ve büyük ölçüde zar içine gömülü olduğundan görüntülenmesi zordur. Ekip, enzimin aktivitesini veya ilaca duyarlılığını bozmadan görüntü hizalamasını iyileştiren küçük bir protein etiketi ve eşleşen bir nanobody “tutuşu” ekleyerek bu sorunun üstesinden geldi. Ardından maya IPC sentazının iki önemli durumunun yapısını belirlediler: lipid substratı seramidine bağlı hâli ve aureobasidin A’ya bağlı hâli.
Enzimin çalışma boşluğu ve kontrol ortağı
Yapılar, Aur1 ve Kei1’in zar boyunca sıkı bir çift oluşturduğunu ortaya koyuyor. Aur1, çevreleyen lipidlere yana doğru açılan oluk benzeri bir reaksiyon odacığı içerir. Seramid bu oluğa yerleşir; bir kuyruğu yağlı amino asitlerden oluşan bir hat boyunca derinlere gömülürken reaktif başı odacığın tabanında yer alan iki histidin ve bir apartat olmak üzere üç kritik kalıntıya doğru yönelir. Bu “H–H–D triadı”nın herhangi bir üyesinin mutasyona uğraması, enzim aktivitesini tamamen ortadan kaldırır; bu da birlikte fosfat taşıyan bir grubun bir lipidden diğerine iki adımlı transferini gerçekleştirdiklerini gösterir.
Kei1, bir zamanlar pasif bir yardımcı olarak düşünüldüğünden, aslında vazgeçilmezdir. Aur1’den bir döngü ile geniş temaslar kurar ve bir fosfolipit molekülünü sıkıca bağlayan paylaşılan bir cebi kavrar. Bu lipidi yerinde tutan kilit kalıntılar mutasyona uğradığında, Aur1–Kei1 birikimi parçalanır ve aktivite kaybolur. Bu durum, doğal zar lipidlerinin enzim kompleksini stabilize eden yapısal kama görevi gördüğünü ve ilaçların işlevini bozmasının ek yollarını işaret ediyor.
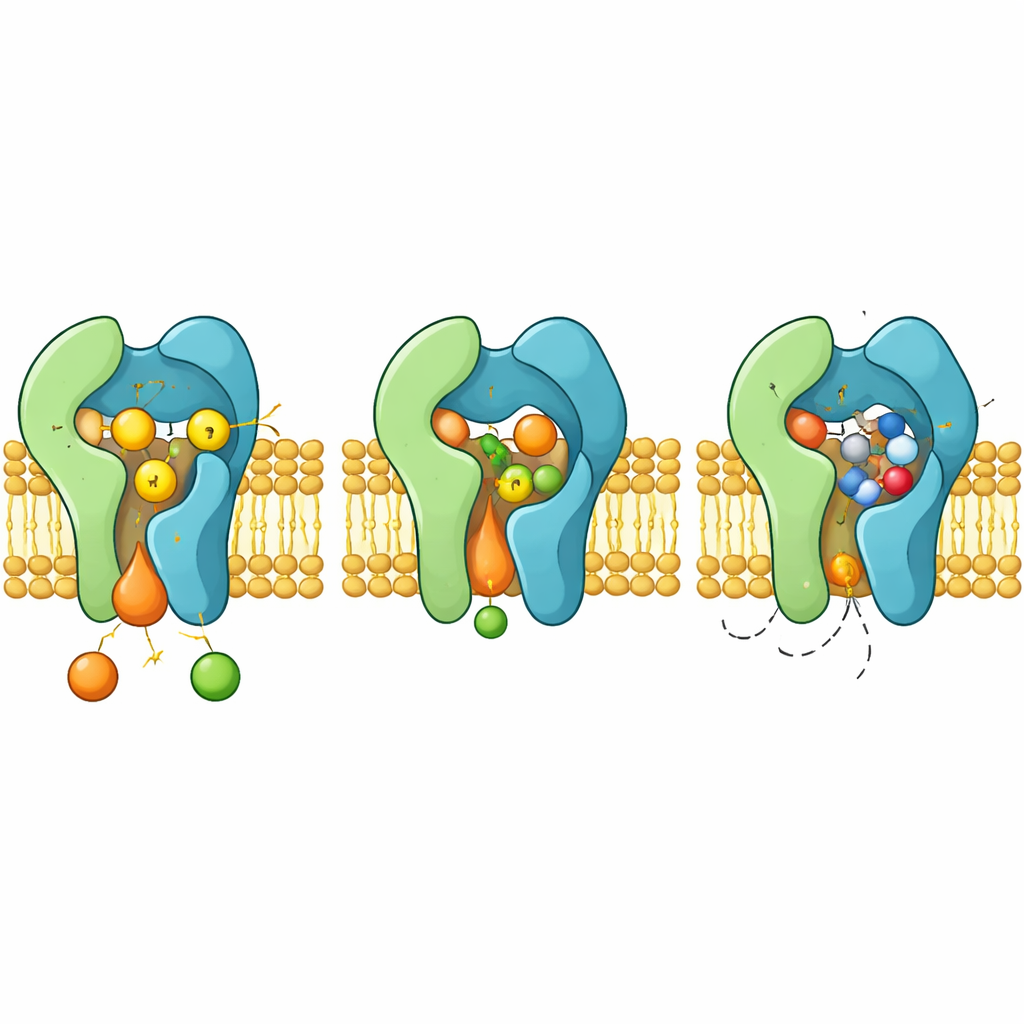
İlacın nasıl bloke ettiği ve direnç nasıl ortaya çıkıyor
Aureobasidin A bağlandığında, normalde seramidi barındıran aynı reaksiyon odacığını işgal eder. Siklik molekül, esnek döngüler ve heliksler arasında yerine oturur, aromatik yan zincirleri iterek sıkı bir cep oluşturmak üzere yeniden yönlendirir. Bu konfigürasyonda ilaç H–H–D triadını örter ve sterik olarak seramidi dışlar; klasik bir rekabetçi inhibitör gibi davranır. Yapılar ayrıca Aur1’deki belirli mutasyonların, örneğin ceple yakın H157 veya F158 kalıntılarının değiştirilmesinin, katalizi korurken ilaç bağlanmasını zayıflatıp dirençli mantarların ortaya çıkmasına nasıl yol açtığını açıklıyor.
Gelecek antifungal ilaçlar için ne anlama geliyor
Birlikte ele alındığında bu bulgular, mantarların onsuz yaşayamayacağı ve insanların sahip olmadığı bir enzimin ayrıntılı haritasını sunuyor. IPC sentazın nasıl bir araya geldiğini, lipid substratlarını nasıl tanıdığını ve aureobasidin A’nın reaksiyon odacığına nasıl yerleştiğini göstererek çalışma, mantar zarlarını seçici şekilde çökerten yeni ilaçların tasarımı için bir plan sunuyor. Yapı yönlendirmeli bileşikler, sınırlı antifungal cephanesini genişletebilir ve artan ilaç dirençli mantar enfeksiyonları sorununun önüne geçmeye yardımcı olabilir.
Atıf: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Anahtar kelimeler: antifungal ilaçlar, mantar hücre zarı, sfinolipitler, ilaç direnci, kriyoyalın elektron mikroskobu