Clear Sky Science · ja
真菌のイノシトールリン酸化セリミド合成の分子機構と抗真菌薬オーレオバシジンAによる阻害
この真菌研究が重要な理由
侵襲性真菌感染症は毎年ひっそりと数百万人を死に至らしめており、特に免疫力が低下した人々で深刻です。それでも利用できる抗真菌薬はごく限られており、多くの真菌が耐性を獲得しつつあります。本研究はヒト細胞には存在しない真菌特有の過程に焦点を当てており、新薬の理想的な標的になり得ます。主要な真菌酵素の働きと強力な薬剤がそれをどのように妨げるかを明らかにすることで、安全で有効な新しい抗真菌療法の基盤を築きます。
真菌の盾にある独自の弱点
真菌細胞は膜の構築と組織化に、スフィンゴ脂質と呼ばれる特殊な脂質群を必要とします。そのうちイノシトールリン酸化セリミド(IPC)は真菌に見られ、哺乳類には存在しません。IPCはIPC合成酵素として知られる二成分の酵素複合体によって作られます。一方のパートナーであるAur1が化学反応を担い、もう一方のKei1は複合体を膜内で位置決めし安定化させます。真菌はIPC合成酵素がなければ生存できず、ヒトにはまったく存在しないことから、この酵素は長く有望な薬剤標的と考えられてきました。
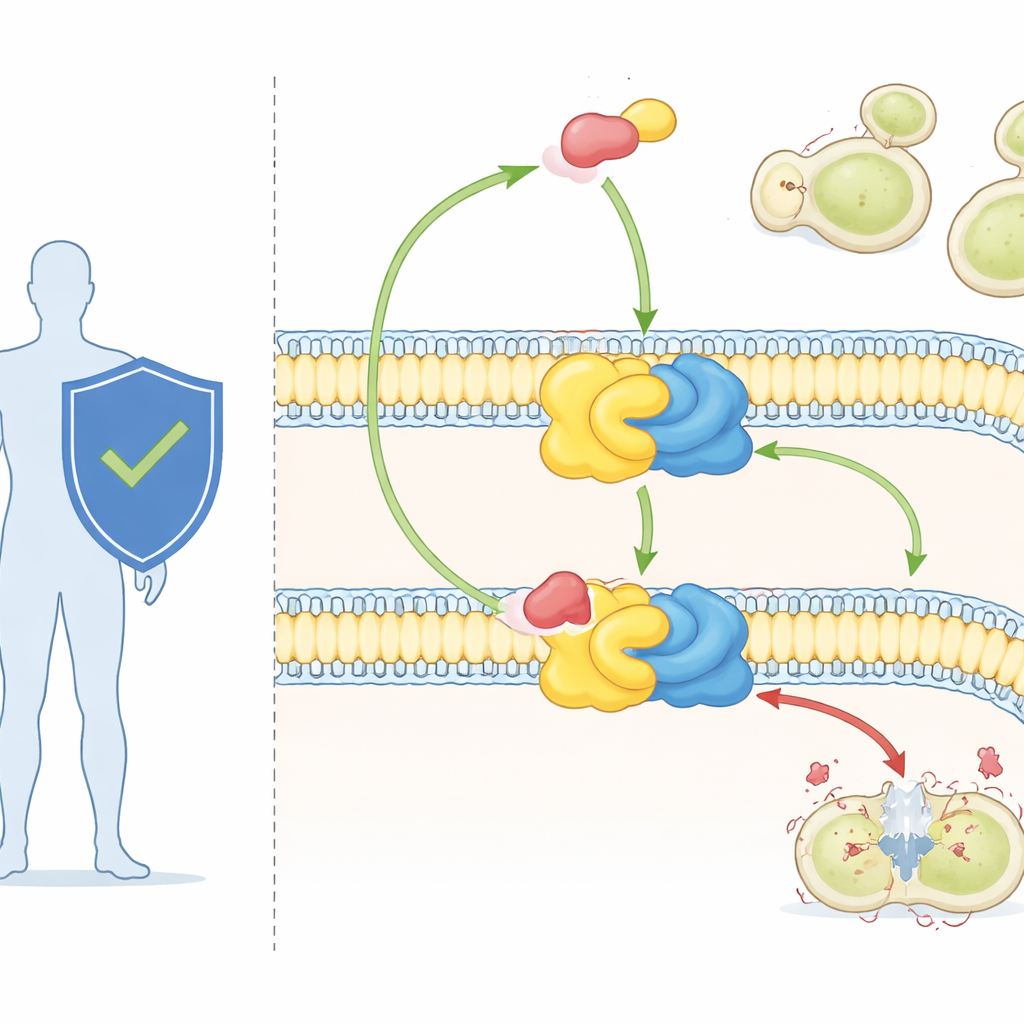
強力な抗真菌薬と謎の標的
オーレオバシジンAは、これまで主に研究用途で用いられてきたものの、知られている中で最も強力な抗真菌薬の一つです。極微量で主要な病原真菌を殺すことができ、哺乳類細胞への毒性は低いとされます。遺伝学的研究により、Aur1タンパク質の変化が真菌に薬剤耐性をもたらすことが示されており、IPC合成酵素が標的であることが確認されていました。しかし高解像度の酵素構造がなければ、自然の脂質基質をどのように認識するかや、オーレオバシジンAがどのように反応を停止させるために噛み込むかを正確に見ることはできませんでした。
反応中の酵素を凍結する
この問題を解決するため、研究者らはクライオ電子顕微鏡(クライオEM)を用い、フラッシュ冷凍した分子を原子近傍の詳細で撮像しました。IPC合成酵素は小さく、膜中に埋もれている部分が多いため可視化が困難です。研究チームは、酵素の活性や薬剤感受性を損なわずに画像の整列を向上させる小さなタンパク質タグと、それに結合するナノボディ“ハンドル”を付加することでこの困難を克服しました。こうして酵母のIPC合成酵素について、脂質基質セリミド結合状態とオーレオバシジンA結合状態という二つの重要な構造を決定しました。
酵素の作動空洞と制御パートナー
構造は、Aur1とKei1が膜を横切る緊密なペアを形成していることを明らかにします。Aur1には溝状の反応チャンバーがあり、側方から周囲の脂質に開いています。セリミドはこの溝に収まり、その片方の尾部は脂溶性アミノ酸列に沿って深く埋まり、反応性の頭部はチャンバー底部に位置する三つの重要残基—二つのヒスチジンと一つのアスパラギン酸—に向いています。この「H–H–D三連」いずれかを変異させると酵素活性が完全に失われ、これらが協働してリン酸基を伴う基の脂質間転移という二段階の反応を担っていることが示されます。
かつて受動的な補助因子と考えられていたKei1は、実は不可欠であることが分かりました。Kei1はAur1のループと広範な接触を形成し、共有のポケットを抱え込んでリン脂質分子を強く結合します。この脂質を保持する重要残基を変異させると、Aur1–Kei1複合体は崩壊し活性を失います。これは、天然の膜脂質が酵素複合体を安定化する構造的な楔(ウェッジ)として働くことを示唆しており、薬剤がその機能を妨げる別の手段を示しています。
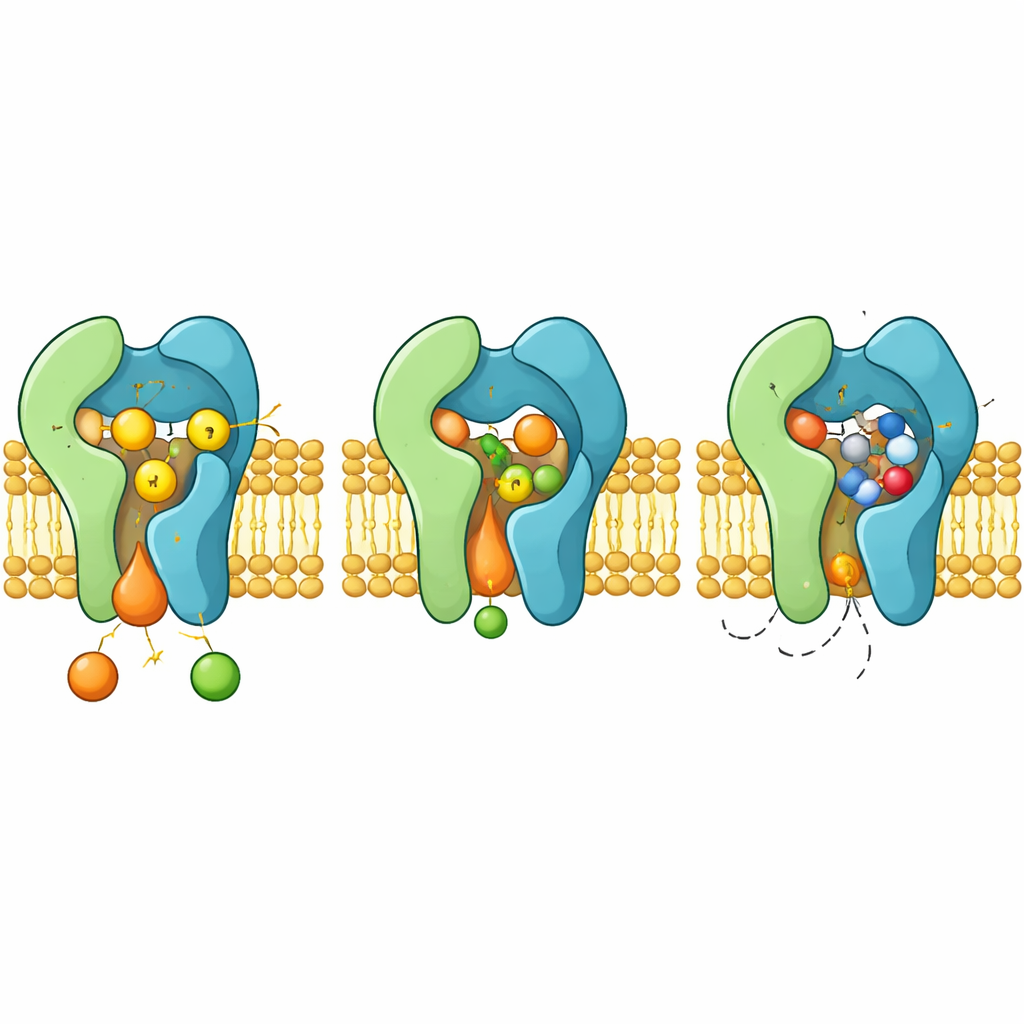
薬剤の遮断機構と耐性の由来
オーレオバシジンAが結合すると、通常セリミドが収まる反応チャンバーを占有します。環状分子は可動性の高いループやヘリックスの間にしっかりとはまり込み、芳香族側鎖を押しのけて再配向させ、ぴったりのポケットを形成させます。この配置では薬剤がH–H–D三連を覆い、立体的にセリミドを排除するため古典的な競合阻害剤として働きます。構造はまた、ポケット近傍の残基(例えばH157やF158)のような特定のAur1変異が触媒作用を維持しつつ薬剤結合を弱め、耐性菌を生じさせる仕組みも説明します。
将来の抗真菌薬への示唆
これらの発見は、真菌が必須とする一方でヒトには存在しない酵素の詳細な地図を提供します。IPC合成酵素がどのように組み立てられ、脂質基質をどのように認識し、オーレオバシジンAがどのように反応チャンバーに噛み込むかを正確に示すことで、本研究は真菌の膜を選択的に障害する新薬設計の青写真を提示します。こうした構造に基づく化合物は、限られた抗真菌薬の選択肢を広げ、薬剤耐性真菌感染症の増大に対抗する助けとなる可能性があります。
引用: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
キーワード: 抗真菌薬, 真菌の細胞膜, スフィンゴ脂質, 薬剤耐性, クライオ電子顕微鏡法