Clear Sky Science · ru
Молекулярные сведения о синтезе инозитолфосфорилцерамидов у грибов и его ингибировании противогрибковым ауребазидином A
Почему эта история о грибах важна
Инвазивные грибковые инфекции тихо уносят жизни миллионов людей каждый год, особенно у тех, у кого ослаблен иммунитет. Однако у врачей в распоряжении всего несколько противогрибковых средств, и многие грибы приобретают устойчивость. В этом исследовании рассматривается грибковой процесс, отсутствующий в клетках человека, что делает его идеальной мишенью для новых лекарств. Раскрывая, как работает ключевой грибковый фермент и как мощный препарат его блокирует, исследователи закладывают основу для более безопасных и эффективных противогрибковых терапий.
Уникальная слабая точка грибковой брони
Грибковые клетки зависят от особого класса жиров — сфинголипидов — для построения и организации своих мембран. Один из них, инозитолфосфорилцерамид (IPC), встречается у грибов, но отсутствует у млекопитающих. IPC синтезируется двухкомпонентным ферментным комплексом, известным как IPC-синтаза. Одна часть, Aur1, осуществляет химическую реакцию; другая, Kei1, помогает позиционировать и стабилизировать комплекс в мембране. Поскольку грибы не могут существовать без IPC-синтазы, а у людей такого фермента вообще нет, длительное время его рассматривали как перспективную мишень для лекарств.
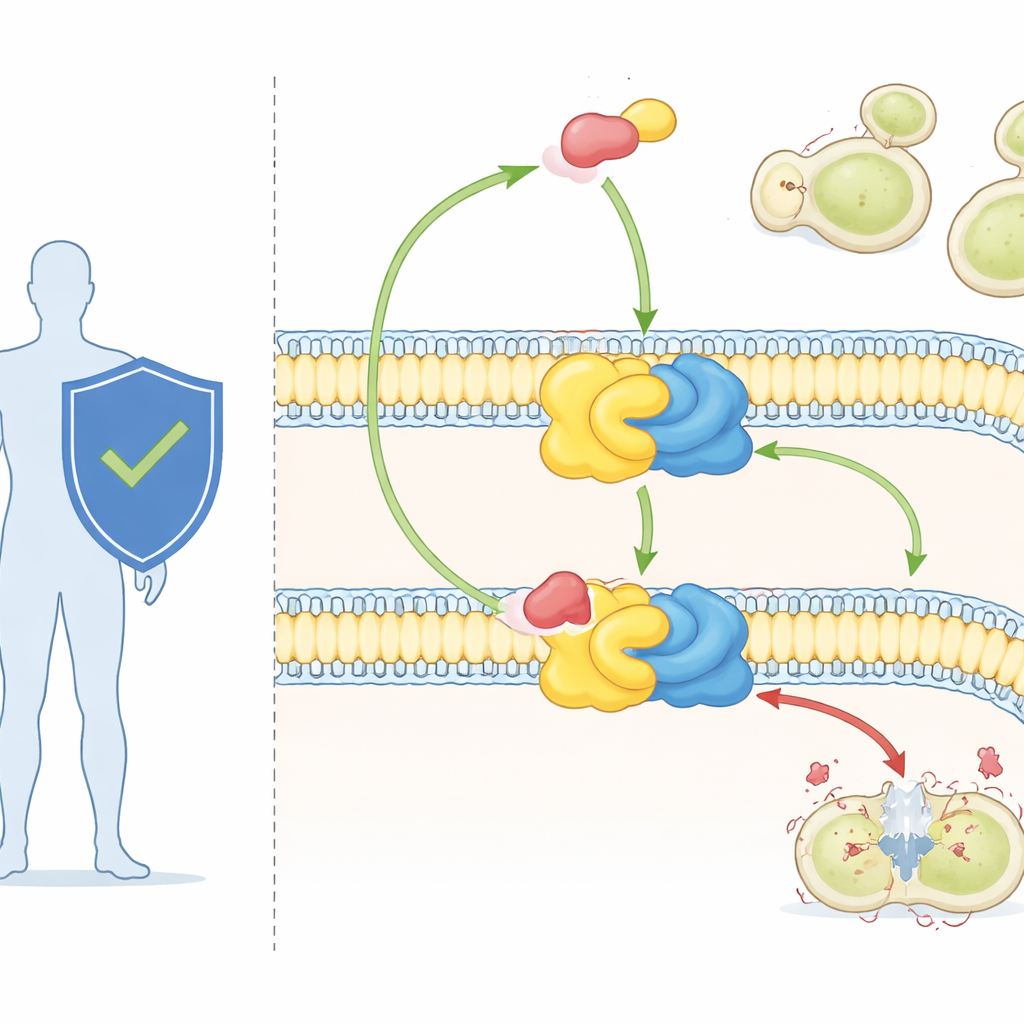
Мощное противогрибковое средство и загадочная мишень
Ауребазидин A, препарат, пока в основном используемый в исследованиях, является одним из наиболее мощных известных противогрибковых средств. Он убивает главные грибковые патогены в крошечных дозах и почти не токсичен для клеток млекопитающих. Генетические данные уже показали, что изменения в белке Aur1 могут делать грибы устойчивыми к препарату, подтверждая, что IPC-синтаза является его мишенью. Но без высокоразрешающего вида фермента учёные не могли точно увидеть, как он распознаёт свои природные липидные субстраты и как ауребазидин A вклинивается в структуру, чтобы остановить реакцию.
Замораживая фермент «в действии»
Чтобы решить эту проблему, исследователи использовали криоэлектронную микроскопию — метод, который позволяет получить изображение быстро замороженных молекул с почти атомарной детальностью. IPC-синтаза мала и преимущественно спрятана в мембране, что затрудняет её визуализацию. Команда преодолела это, присоединив к ферменту крошечную метку белка и соответствующую нанотелесную «ручку», что улучшило выравнивание изображений, не нарушая активности фермента и его чувствительности к препарату. Затем они определили структуры дрожжевой IPC-синтазы в двух ключевых состояниях: связанной с липидным субстратом церамида и связанной с ауребазидином A.
Рабочая полость фермента и регуляторный партнёр
Структуры показывают, что Aur1 и Kei1 образуют плотную пару, проходящую через мембрану. Aur1 содержит желобообразную реакционную камеру, которая открывается боком в сторону окружающих липидов. Церамид располагается в этом желобе: один хвост глубоко погружён вдоль ряда «жирных» аминокислот, а реактивная голова направлена к трём критическим остаткам — двум гистидинам и одной аспарагиновой кислоте — расположенным у основания камеры. Замена любого из членов этой «H–H–D триады» полностью уничтожает активность фермента, показывая, что вместе они осуществляют двухступенчатую передачу фосфорсодержащей группы от одного липида к другому.
Kei1, считавшийся пассивным помощником, оказывается необходимым. Он устанавливает обширные контакты с петлёй Aur1 и охватывает общий карман, который прочно связывает молекулу фосфолипида. Когда ключевые остатки, удерживающие этот липид на месте, мутируют, комплекс Aur1–Kei1 распадается и теряет активность. Это указывает на то, что нативные мембранные липиды действуют как структурные клинья, стабилизирующие ферментный комплекс, и открывает дополнительные пути, которыми препараты могут нарушать его функцию.
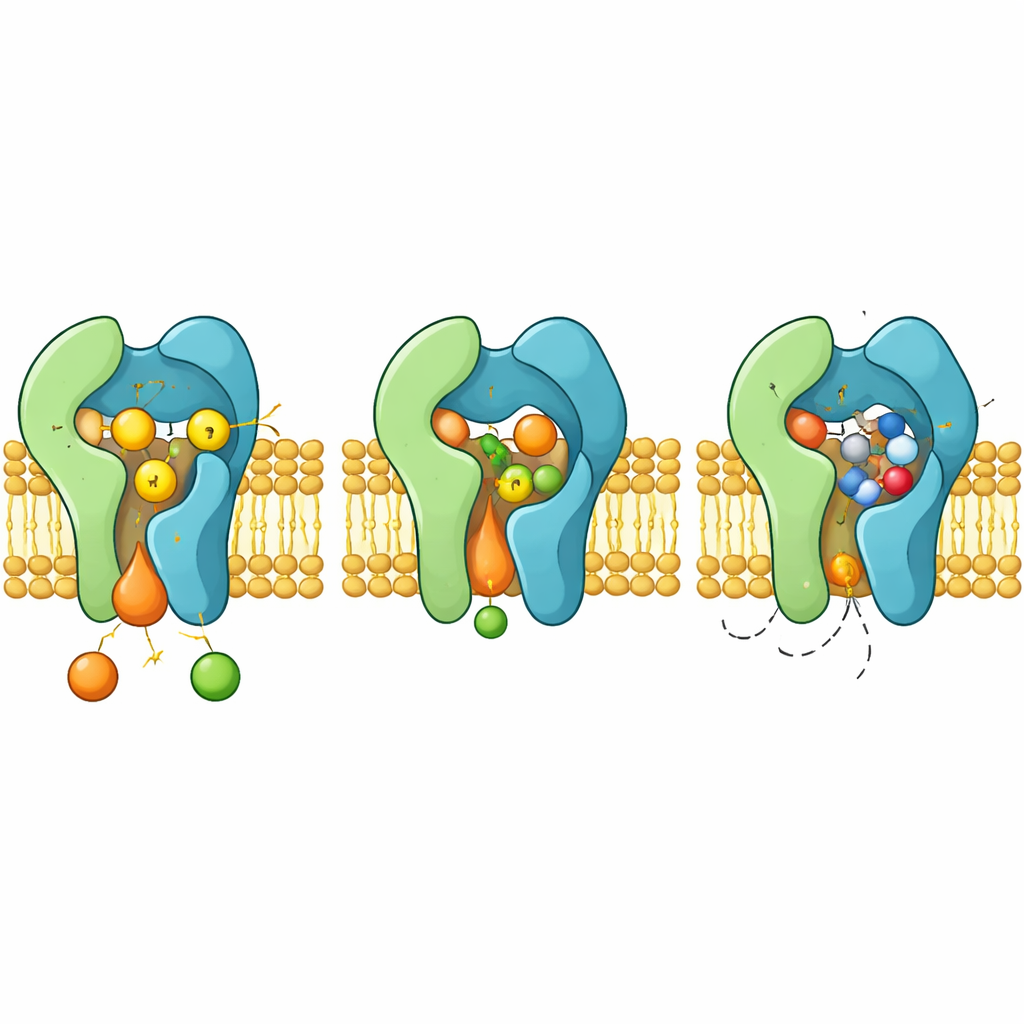
Как препарат блокирует фермент и как возникает устойчивость
Когда связывается ауребазидин A, он занимает ту же реакционную камеру, в которой обычно располагается церамид. Циклическая молекула зажимается между гибкими петлями и спиралями, отталкивая ароматические боковые цепи, которые перенастраиваются, чтобы создать плотный карман. В такой конфигурации препарат закрывает доступ к H–H–D триаде и стерически исключает церамид, действуя как классический конкурентный ингибитор. Структуры также объясняют, как конкретные мутации в Aur1, например изменение остатков H157 или F158 рядом с карманом, ослабляют связывание препарата, при этом сохраняя каталитическую активность, что приводит к появлению устойчивых грибов.
Что это значит для будущих противогрибковых препаратов
Вместе эти результаты дают детальную карту фермента, без которого грибы не могут жить, а у человека его нет. Показывая, как собирается IPC-синтаза, как она распознаёт свои липидные субстраты и как ауребазидин A вклинивается в её реакционную камеру, исследование предоставляет план для разработки новых препаратов, которые селективно нарушают целостность грибковых мембран. Такие препараты, созданные на основе структурной информации, могут расширить ограниченный набор противогрибковых средств и помочь опережать растущую проблему лекарственно‑резистентных грибковых инфекций.
Цитирование: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Ключевые слова: противогрибковые препараты, клеточная мембрана грибов, сфинголипиды, устойчивость к препаратам, криоэлектронная микроскопия