Clear Sky Science · fr
Aperçus moléculaires de la synthèse fongique de l’inositol phosphorylceramide et de son inhibition par l’antifongique aureobasidine A
Pourquoi cette histoire de champignon compte
Les infections fongiques invasives tuent discrètement des millions de personnes chaque année, en particulier celles dont le système immunitaire est affaibli. Pourtant, les médecins ne disposent que d’un nombre limité d’antifongiques, et de nombreux champignons développent une résistance. Cette étude se concentre sur un processus fongique absent des cellules humaines, ce qui en fait une cible idéale pour de nouveaux médicaments. En révélant comment une enzyme fongique clé fonctionne — et comment un puissant composé l’enrayé — les chercheurs posent les bases de thérapies antifongiques plus sûres et plus efficaces.
Une faiblesse unique de l’armure fongique
Les cellules fongiques s’appuient sur une classe particulière de lipides, appelés sphingolipides, pour construire et organiser leurs membranes. L’un d’eux, l’inositol phosphorylceramide (IPC), se trouve chez les champignons mais est absent chez les mammifères. L’IPC est synthétisé par un complexe enzymatique à deux sous‑unités connu sous le nom d’IPC synthase. L’une des sous‑unités, Aur1, réalise la chimie ; l’autre, Kei1, aide à positionner et stabiliser le complexe dans la membrane. Parce que les champignons ne peuvent pas vivre sans l’IPC synthase, alors que les humains ne possèdent pas cette enzyme, celle‑ci est depuis longtemps considérée comme une cible médicamenteuse attrayante.
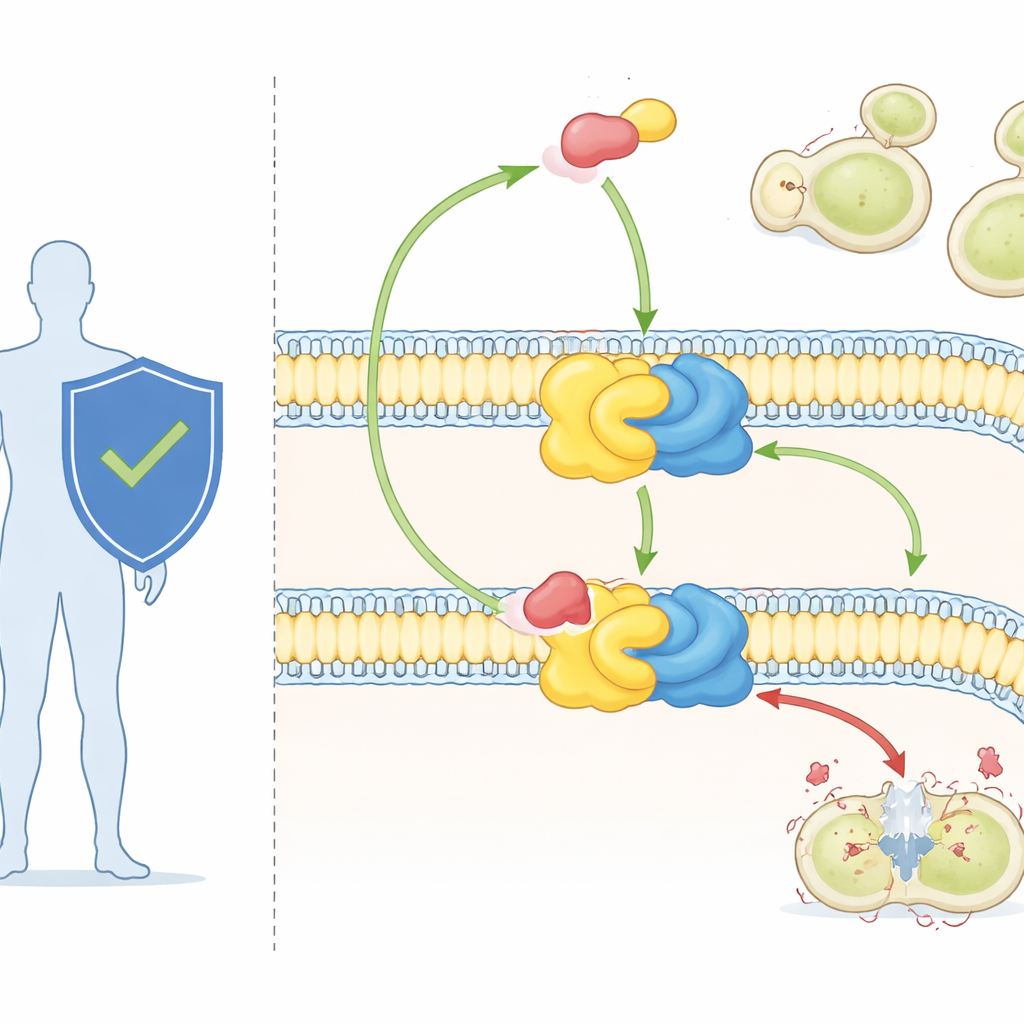
Un antifongique puissant et une cible mystérieuse
L’aureobasidine A, utilisée principalement en recherche jusqu’à présent, est l’un des antifongiques les plus puissants connus. Elle peut tuer d’importants agents pathogènes fongiques à de très faibles doses et présente peu de toxicité pour les cellules de mammifères. Des travaux génétiques avaient déjà montré que des modifications de la protéine Aur1 peuvent rendre les champignons résistants au composé, confirmant que l’IPC synthase en est la cible. Mais sans vue à haute résolution de l’enzyme, les scientifiques ne pouvaient pas voir exactement comment elle reconnaît ses substrats lipidiques naturels ni comment l’aureobasidine A s’insère pour interrompre la réaction.
Geler l’enzyme en action
Pour résoudre ce problème, les chercheurs ont utilisé la cryo‑microscopie électronique, une technique qui image des molécules vitrifiées à une résolution proche de l’atome. L’IPC synthase est petite et majoritairement enfouie dans la membrane, ce qui la rend difficile à visualiser. L’équipe a contourné cet obstacle en ajoutant une minuscule étiquette protéique et un nanocorps « poignée » correspondant qui ont amélioré l’alignement des images sans perturber l’activité de l’enzyme ni sa sensibilité au médicament. Ils ont ensuite déterminé les structures de l’IPC synthase de levure dans deux états clés : liée à son substrat lipidique céramide, et liée à l’aureobasidine A.
La cavité de travail de l’enzyme et son partenaire de contrôle
Les structures révèlent Aur1 et Kei1 formant une paire serrée traversant la membrane. Aur1 contient une chambre de réaction en forme de sillon qui s’ouvre latéralement vers les lipides environnants. Le céramide s’insère dans ce sillon, une de ses chaînes enfouie profondément le long d’une ligne d’acides aminés hydrophobes et sa tête réactive orientée vers trois résidus cruciaux — deux histidines et un aspartate — situés à la base de la chambre. La mutation de n’importe quel membre de cette « triade H–H–D » abolît complètement l’activité enzymatique, démontrant qu’ensemble ils réalisent le transfert en deux étapes d’un groupe phosphorylé d’un lipide à un autre.
Kei1, jadis considéré comme un aide‑passif, s’avère essentiel. Il établit des contacts étendus avec une boucle d’Aur1 et embrasse une poche partagée qui lie fermement une molécule de phospholipide. Lorsque des résidus clés qui retiennent ce lipide en place sont mutés, l’assemblage Aur1–Kei1 se désagrège et l’activité disparaît. Cela suggère que des lipides membranaires natifs agissent comme des cales structurelles stabilisant le complexe enzymatique, indiquant des voies supplémentaires par lesquelles des médicaments pourraient perturber sa fonction.
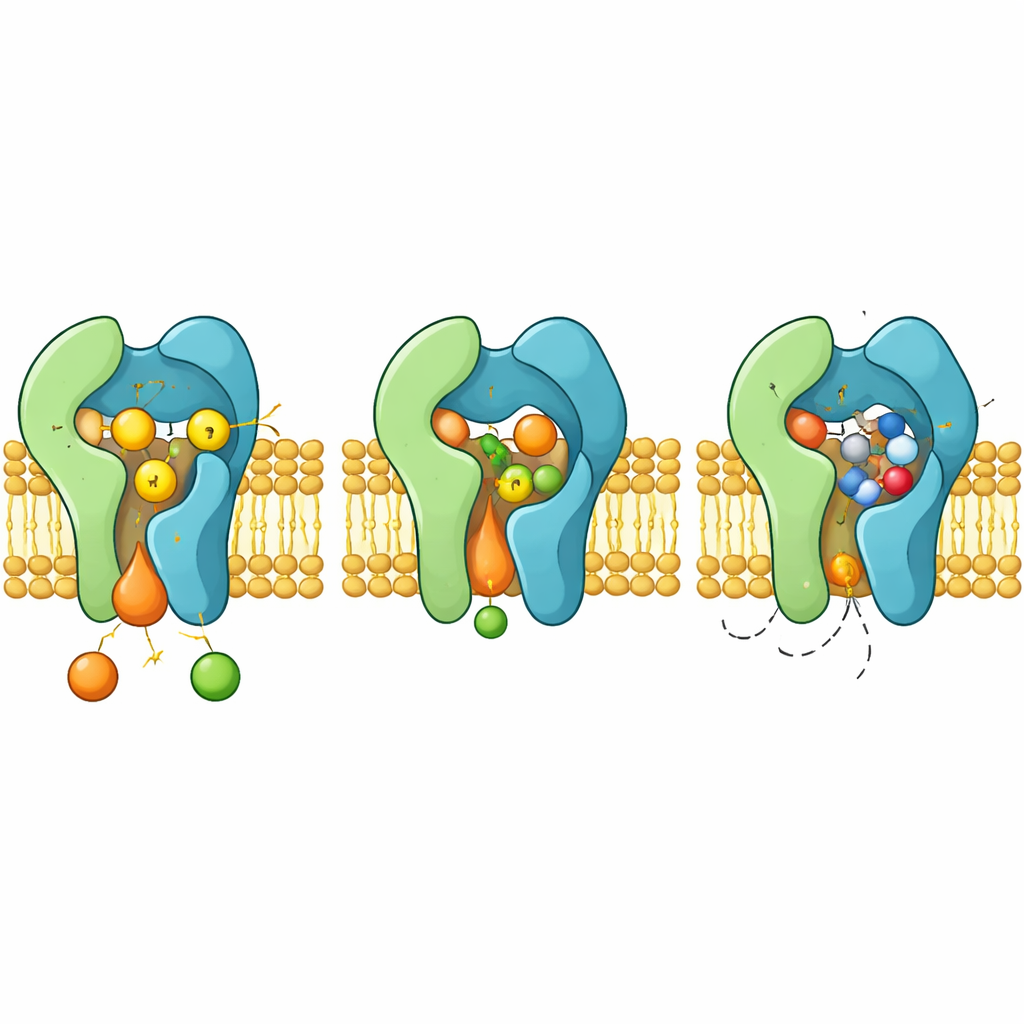
Comment le médicament bloque et comment la résistance émerge
Lorsque l’aureobasidine A se lie, elle occupe la même chambre de réaction qui accueille normalement le céramide. La molécule cyclique se verrouille entre des boucles et des hélices flexibles, repoussant des chaînes latérales aromatiques qui se réorientent pour créer une poche bien ajustée. Dans cette configuration, le médicament occlut la triade H–H–D et exclut stériquement le céramide, agissant comme un inhibiteur compétitif classique. Les structures expliquent aussi comment des mutations spécifiques dans Aur1, comme l’altération des résidus H157 ou F158 près de la poche, affaiblissent la liaison du médicament tout en préservant la catalyse, entraînant l’apparition de champignons résistants.
Ce que cela signifie pour les futurs antifongiques
Ensemble, ces découvertes fournissent une carte détaillée d’une enzyme indispensable aux champignons et absente chez l’homme. En montrant exactement comment l’IPC synthase s’assemble, comment elle reconnaît ses substrats lipidiques et comment l’aureobasidine A s’insère dans sa chambre de réaction, l’étude offre un plan pour concevoir de nouveaux médicaments qui affaiblissent sélectivement les membranes fongiques. De tels composés guidés par la structure pourraient élargir l’arsenal antifongique limité et aider à devancer le problème croissant des infections fongiques résistantes aux traitements.
Citation: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Mots-clés: médicaments antifongiques, membrane cellulaire fongique, sphingolipides, résistance aux médicaments, cryo‑microscopie électronique