Clear Sky Science · nl
Moleculaire inzichten in de synthese van schimmel-inositolgefosforylceramide en de remming ervan door het antifungale aureobasidine A
Waarom dit schimmelverhaal ertoe doet
Invasieve schimmelinfecties doden stilletjes miljoenen mensen per jaar, vooral personen met een verzwakt immuunsysteem. Artsen hebben echter maar een handvol antifungale middelen en veel schimmels ontwikkelen resistentie. Deze studie richt zich op een schimmelproces dat niet in menselijke cellen voorkomt, waardoor het een ideaal mikpunt is voor nieuwe geneesmiddelen. Door te onthullen hoe een sleutelenzym van schimmels werkt — en hoe een krachtig middel het blokkeert — leggen de onderzoekers de basis voor veiligere, effectievere antifungale therapieën.
Een unieke zwakke plek in het schimmelvezet
Schimmelcellen vertrouwen op een speciale klasse vetten, sphingolipiden genaamd, om hun membranen op te bouwen en te organiseren. Een daarvan, inositolgefosforylceramide (IPC), komt voor in schimmels maar ontbreekt bij zoogdieren. IPC wordt gemaakt door een tweedelig enzymcomplex dat bekendstaat als IPC-synthase. De ene partner, Aur1, voert de chemische reactie uit; de andere, Kei1, helpt het complex in het membraan te positioneren en te stabiliseren. Omdat schimmels niet zonder IPC-synthase kunnen leven, terwijl mensen het helemaal niet hebben, wordt dit enzym al lang gezien als een aantrekkelijk doelwit voor geneesmiddelen.
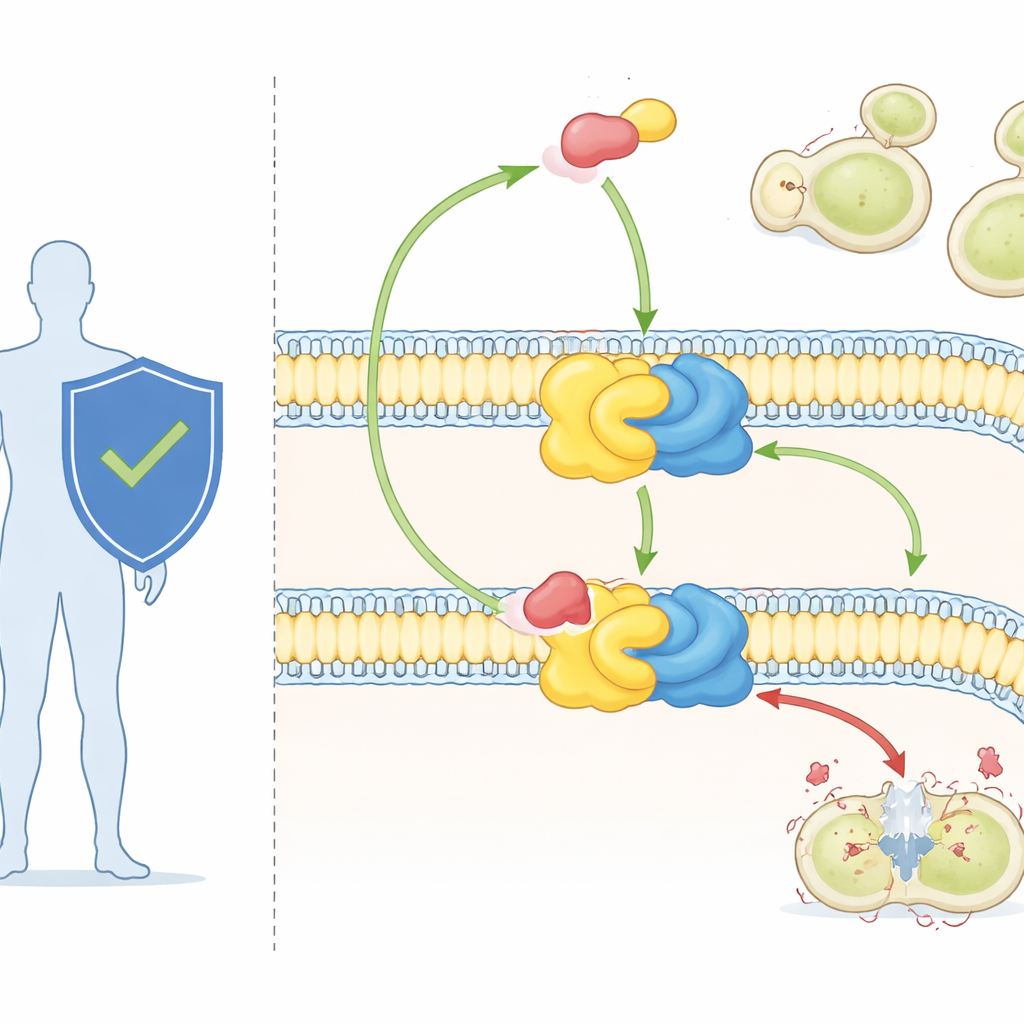
Een krachtig antifungaal en een mysterieus doelwit
Het middel aureobasidine A, tot dusver vooral in onderzoek gebruikt, is een van de meest krachtige bekende antifungale stoffen. Het kan belangrijke schimmelpathogenen doden in zeer kleine doses en vertoont weinig toxiciteit voor zoogdiercellen. Genetisch onderzoek had al aangetoond dat veranderingen in het Aur1-eiwit schimmels resistent kunnen maken tegen het middel, wat bevestigt dat IPC-synthase het doelwit is. Maar zonder een hoogresolutieweergave van het enzym konden wetenschappers niet precies zien hoe het zijn natuurlijke lipidesubstraten herkent of hoe aureobasidine A zich in het enzym klemt om de reactie te blokkeren.
Het enzym in actie bevriezen
Om dit probleem op te lossen gebruikten de onderzoekers cryo-elektronenmicroscopie, een techniek die bevriende moleculen afbeeldt met bijna-atomair detail. IPC-synthase is klein en grotendeels in het membraan ingebed, wat visualisatie bemoeilijkt. Het team omzeilde dit door een klein proteinetiket en een bijpassende nanobody "greep" te bevestigen die de beelduitlijning verbeterde zonder de activiteit van het enzym of de gevoeligheid voor het middel te verstoren. Vervolgens bepaalden ze structuren van de gist-IPC-synthase in twee sleuteltoestanden: gebonden aan zijn lipidesubstraat ceramide, en gebonden aan aureobasidine A.
De werkzame holte van het enzym en de controlerende partner
De structuren tonen Aur1 en Kei1 die een strak paar vormen dat het membraan overspant. Aur1 bevat een groefachtige reactiekamer die zijwaarts uitmondt in de omringende lipiden. Ceramide nestelt zich in deze groef, met één staart diep begraven langs een rij olierijke aminozuren en de reactieve kop gericht naar drie cruciale residuen — twee histidines en één asparaginezuur — die onder in de kamer zitten. Het muteren van elk lid van deze "H–H–D triade" schakelt de enzymactiviteit volledig uit, wat aantoont dat zij samen de twee-stappenoverdracht van een fosfaatdragende groep van het ene lipide naar het andere uitvoeren.
Kei1, ooit gedacht een passieve helper te zijn, blijkt essentieel. Het maakt uitgebreide contacten met een lus van Aur1 en omvat een gedeelde pocket die strak een fosfolipidemolecuul bindt. Wanneer sleutelresiduen die dit lipide op zijn plaats houden gemuteerd worden, valt het Aur1–Kei1-complex uiteen en gaat de activiteit verloren. Dit suggereert dat native membraannoten als structurele wiggen werken die het enzymcomplex stabiliseren, wat wijst op extra manieren waarop geneesmiddelen zijn functie kunnen verstoren.
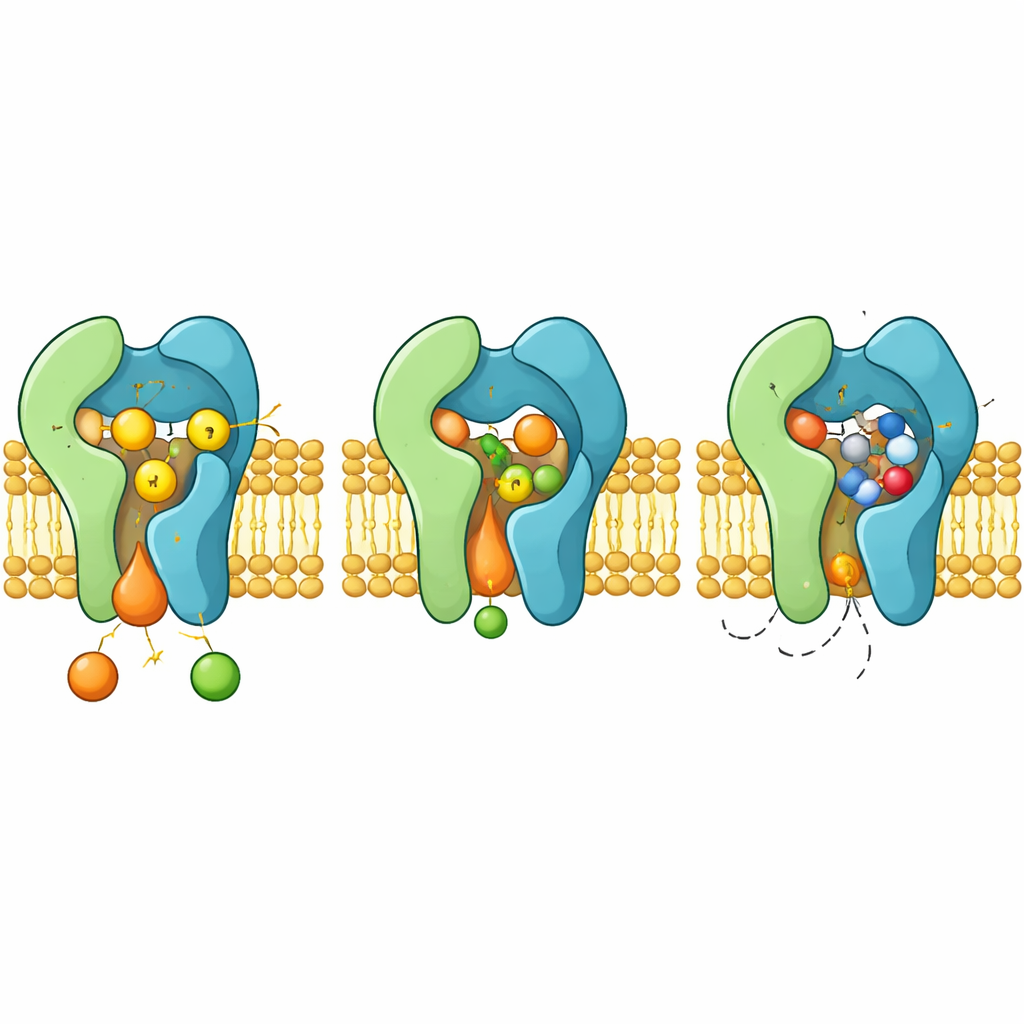
Hoe het middel blokkeert en hoe resistentie ontstaat
Wanneer aureobasidine A bindt, neemt het dezelfde reactiekamer in die normaal ceramide huisvest. Het cyclische molecuul klemt zich vast tussen flexibele lussen en helixen en duwt aromatische zijketens opzij die zich heroriënteren om een nauw gepaste pocket te vormen. In deze configuratie blokkeert het middel de H–H–D triade en sluit ceramide sterisch uit, werkend als een klassieke competitieve remmer. De structuren verklaren ook hoe specifieke mutaties in Aur1, zoals veranderingen in residuen H157 of F158 nabij de pocket, de geneesmiddelbinding verzwakken terwijl de katalyse behouden blijft, wat leidt tot resistente schimmels.
Wat dit betekent voor toekomstige antifungale middelen
Gezamenlijk bieden deze bevindingen een gedetailleerde kaart van een enzym waar schimmels niet zonder kunnen en dat mensen niet bezitten. Door precies te laten zien hoe IPC-synthase assembleert, hoe het zijn lipidesubstraten herkent en hoe aureobasidine A zich in zijn reactiekamer klemt, biedt de studie een blauwdruk voor het ontwerpen van nieuwe middelen die selectief schimmelmembraan verzwakken. Dergelijke op structuur geleide verbindingen zouden het beperkte antifungale arsenaal kunnen uitbreiden en kunnen helpen de groeiende problematiek van medicijnresistente schimmelinfecties voor te blijven.
Bronvermelding: Chen, J., Ke, Y., Zhang, M. et al. Molecular insights into fungal inositol phosphorylceramide synthesis and its inhibition by antifungal aureobasidin A. Nat Commun 17, 3951 (2026). https://doi.org/10.1038/s41467-026-69777-3
Trefwoorden: antifungale middelen, schimmelcelmembraan, sphingolipiden, middelenresistentie, kryo-elektronenmicroscopie