Clear Sky Science · zh
营养瓶颈控制结构化细菌群体中抗生素的疗效
这对感染的意义
抗生素通常在充分混合的试管中进行测试,然而许多真实的感染涉及附着在组织或医疗器械上的致密细菌群落。在这些拥挤的环境中,营养和药物从外部渗入,形成尖锐的化学梯度,而实验室测试很少能再现这种情况。本研究提出了一个简单但有力的问题:营养在这些结构化细菌群体中的流动方式,是否能控制抗生素的有效性——甚至帮助某些细菌口袋存活并复苏?
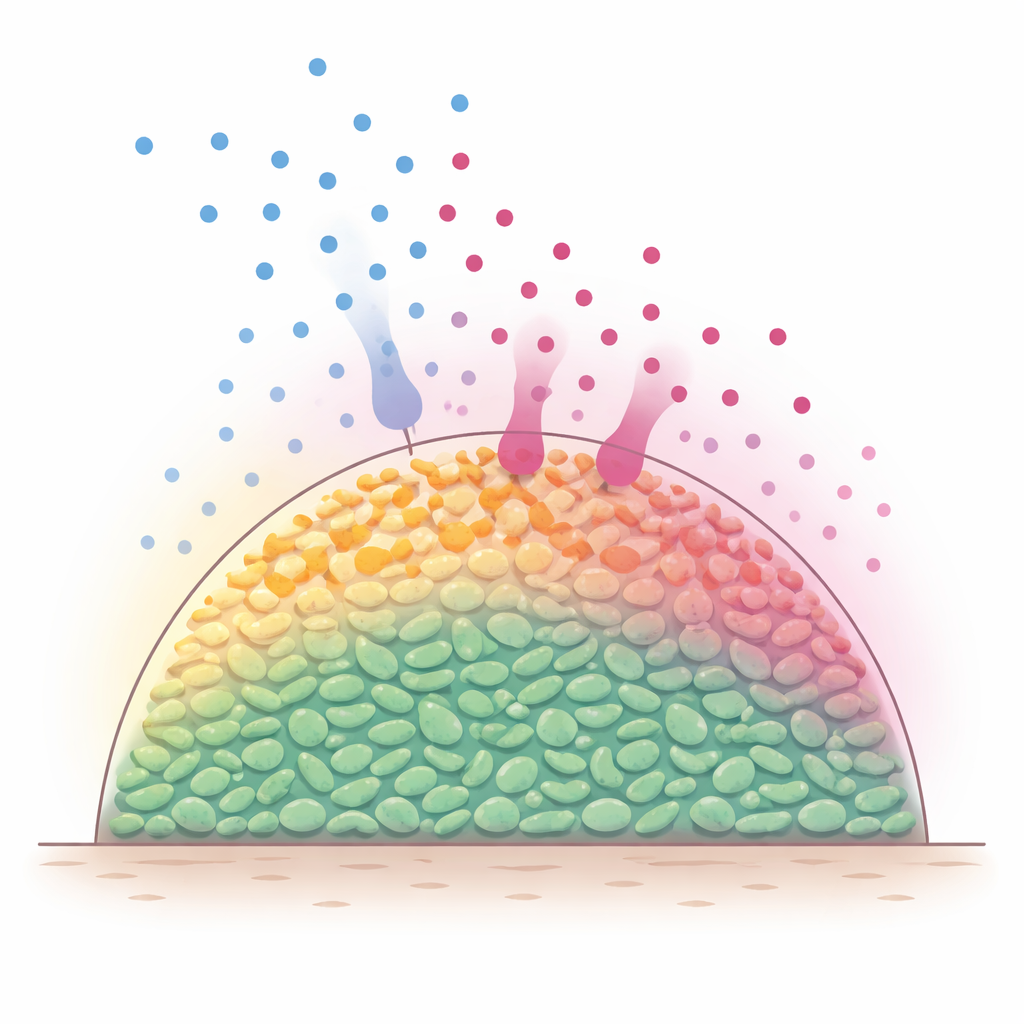
细菌群落内的隐蔽层
在自然环境中,细菌常以多细胞组装体的形式生活,有时称为生物膜,细胞在三维空间中紧密堆积。营养分子(例如糖类)自外部扩散进入,却被最外层的细胞迅速消耗。因此,表层保持较高的代谢活性,而更深的细胞则饥饿且代谢迟缓。由于许多抗生素对活跃生长的细菌最为有效,科学家长期以来怀疑这些内在的营养梯度会形成更难以杀死的受保护内部。然而,在致密群体中直接观察营养和抗生素随时间移动和反应时发生的事情一直很困难。
构建可控的微型生物膜
为了解决这一挑战,研究者将大肠杆菌(E. coli)困在透明水凝胶基质中——这是一种柔软、充水的材料,其孔隙将细胞固定同时允许小分子扩散。每个凝胶块的一侧含有细菌但不含营养物或药物;另一侧则含有糖(葡萄糖)、抗生素(磷霉素)或两者兼有。通过移除两半之间的隔板,团队可以让分子缓慢扩散,同时用荧光显微镜区分活细胞与死细胞。该装置模拟了生物膜的横截面,一侧是外部世界,另一侧是受保护的内部,但比自然样本具有更严格的实验可控性。
当食物解锁致死作用时
令人惊讶的是,当仅有抗生素扩散进入细菌区域时——即使在远高于标准抑制浓度的剂量下——大多数细胞在整整一天内仍保持存活。情形在加入适量葡萄糖与抗生素共同扩散时发生了显著改变。在这种情况下,团队观察到一个异常锋利的“死亡前线”从暴露一侧向内部推进:一个活细胞骤然被死亡细胞取代的推进层。该前线的速度强烈依赖于营养供应与消耗,但对提高抗生素剂量在超过某一阈值后的变化不太敏感。更多的糖会加速前线;更多的细胞(总体上更快地消耗糖)则会减慢它。用其它几种营养和抗生素也出现了类似行为,表明这是一种普遍原理,而非某种药物的特例。
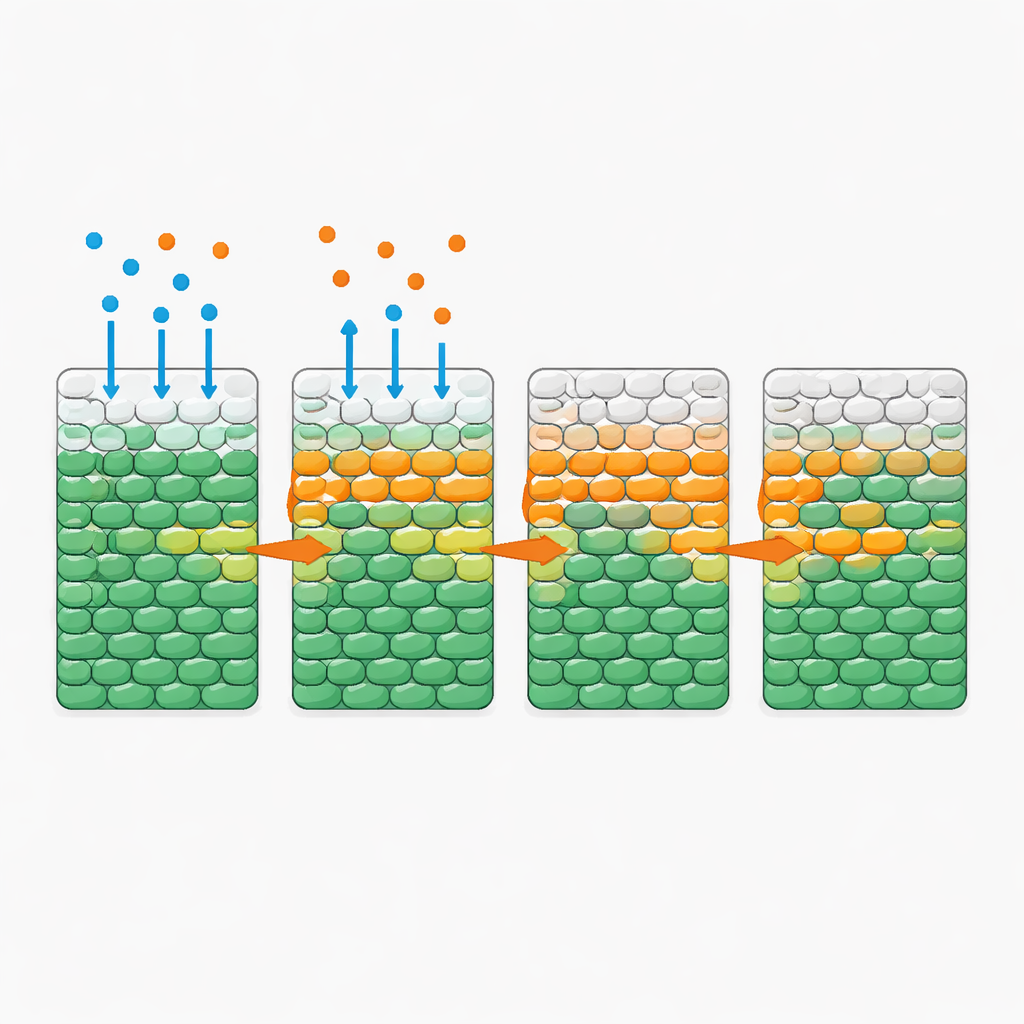
复杂模式背后的简单规则
为定量理解这些动力学,作者建立了一个数学模型,追踪三种要素:细菌、营养和抗生素。在模型中,营养和抗生素在群体中扩散;细胞消耗营养以生长;一旦在足够的营养和抗生素暴露下持续足够长时间,细胞先增殖随后死亡。所有参数均在充分混合的培养物中独立测量,因此模型在空间实验中不需调参。尽管如此,模拟仍再现了观察到的死亡前线及其对营养水平、细胞密度和消耗速率的依赖性。模型分析揭示了一个关键的无量纲量,比较了细胞在抗生素暴露下生长并死亡所需的时间与耗尽其局部营养供应所需的时间。当营养被迅速耗尽时,内层细胞保持饥饿因而在很大程度上受到保护;当消耗较慢时,营养可深入渗透,前线便能横扫整个群体。
生存与再生长如何出现
即便细胞具有相同遗传背景,细菌群体对药物的敏感性也很少是均一的。团队利用其平台探究当部分细胞比其他细胞更耐药时会发生什么。在中等剂量的抗生素下,死亡前线仍然形成并向内推进,但前线通过后,零散的更耐药细胞微菌落开始在其后方重新生长,利用释放到更空旷区域的营养。降低抗生素剂量或增加初始细胞密度会放大这种再生。在结构化群体中,许多此类耐药口袋可以并存,这与通常在充分混合培养物中由单一优势株占据主导的情况形成对比。这种格局可能增加感染进化出更高耐药性或在治疗后反弹的机会。
这对治疗感染的启示
这项工作表明,营养可用性不仅是背景细节,而是在结构化细菌群体中决定抗生素杀灭效果的核心瓶颈。临床医生和研究者除了询问药物是否能到达感染部位外,可能还需考虑食物源如何穿过群落以及细胞消耗它们的速度。该研究的框架,包括其关于何时营养消耗超过杀灭速度的简单量度,提供了一种预测抗生素治疗何时可能在保护性的外壳处停滞的方法。它还表明,将抗生素与改变营养渗透或破坏空间结构的策略结合,可能使现有药物更有效,并解释了为何致密、生物膜样感染即便在实验室测试显示药物应当有效时也能如此顽固。
引用: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
关键词: 抗生素耐药性, 细菌生物膜, 营养梯度, 磷霉素, 微生物群体动力学