Clear Sky Science · ru
Узкое место в питании контролирует эффективность антибиотиков в структурированных бактериальных популяциях
Почему это важно для инфекций
Антибиотики часто испытывают в хорошо перемешанных пробирках, тогда как многие реальные инфекции связаны с плотными сообществами бактерий, прикреплёнными к тканям или медицинским устройствам. В таких тесных условиях питание и лекарства проникают снаружи, создавая резкие химические градиенты, которые редко учитываются в лабораторных тестах. В этом исследовании ставится простой, но мощный вопрос: может ли способ распространения питательных веществ через структурированные бактериальные популяции определять эффективность антибиотиков — и даже позволять участкам бактерий выживать и восстанавливаться?
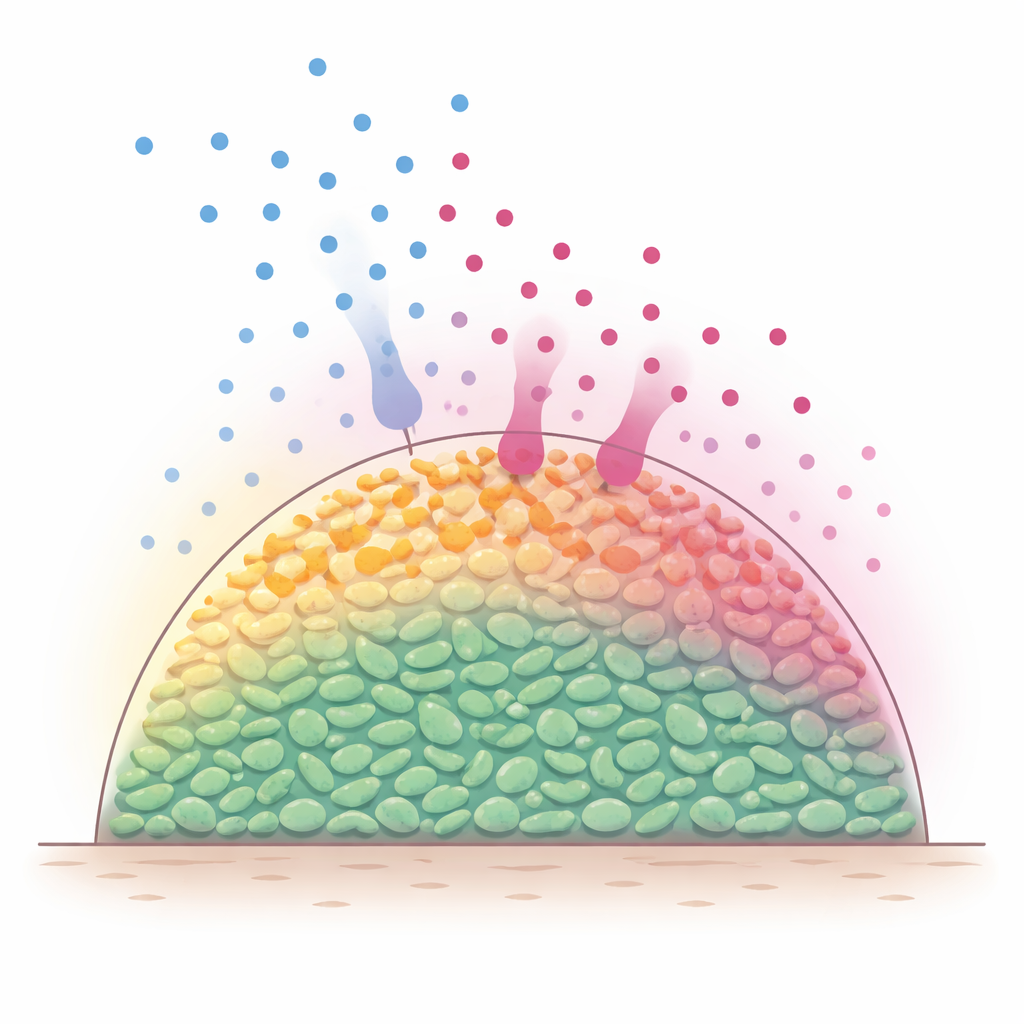
Скрытые слои внутри бактериальных сообществ
В природных условиях бактерии часто живут в многоклеточных образованиях, иногда называемых биопленками, где клетки упакованы в трёх измерениях. Молекулы питательных веществ, например сахара, диффундируют снаружи и быстро поедаются внешними клетками. В результате поверхностные слои остаются метаболически активными, тогда как более глубокие клетки испытывают голод и становятся вялыми. Поскольку многие антибиотики наиболее эффективны против активно растущих бактерий, учёные давно подозревали, что такие встроенные градиенты питательных веществ создают защищённую внутреннюю зону, которую труднее уничтожить. Тем не менее было сложно напрямую наблюдать, что происходит внутри таких плотных популяций по мере перемещения и реакции питательных веществ и антибиотиков во времени.
Создание управляемой мини-биопленки
Чтобы решить эту задачу, исследователи поместили бактерии E. coli в прозрачные гидрогелевые матрицы — мягкие, заполненные водой материалы с порами, которые фиксируют клетки, но пропускают диффузию малых молекул. С одной стороны каждого гелевого блока находились бактерии, но не было ни питательных веществ, ни лекарств; с другой стороны располагался резервуар с сахаром (глюкозой), антибиотиком (фосфомицином) или обоими веществами. Устранив перегородку между половинами, команда позволяла молекулам медленно диффундировать и с помощью флуоресцентной микроскопии различала живые и мёртвые клетки. Эта установка имитирует поперечное сечение биопленки, с внешним миром с одной стороны и защищённым интерьером с другой, но обеспечивает гораздо более строгий экспериментальный контроль, чем природные образцы.
Когда еда включает смертельное действие
Удивительно, но когда антибиотик один диффундировал в область с бактериями — даже в дозах значительно выше стандартных ингибирующих уровней — большинство клеток оставались живыми в течение полного дня. Ситуация кардинально менялась, когда вместе с антибиотиком добавляли небольшое количество глюкозы. В этом случае исследователи наблюдали заметный «фронт смерти», быстро продвигающийся внутрь от открытой стороны: передовая полоса, где живые клетки резко уступали место мёртвым. Скорость этого фронта сильно зависела от подачи и потребления питательных веществ, но в значительной степени была нечувствительна к увеличению дозы антибиотика после достижения определённого порога. Большее количество сахара ускоряло фронт; больше клеток, которые коллективно поедали сахар быстрее, замедляло его. Похожее поведение наблюдалось с несколькими другими питательными веществами и антибиотиками, что указывает на общее правило, а не на частный случай одного препарата.
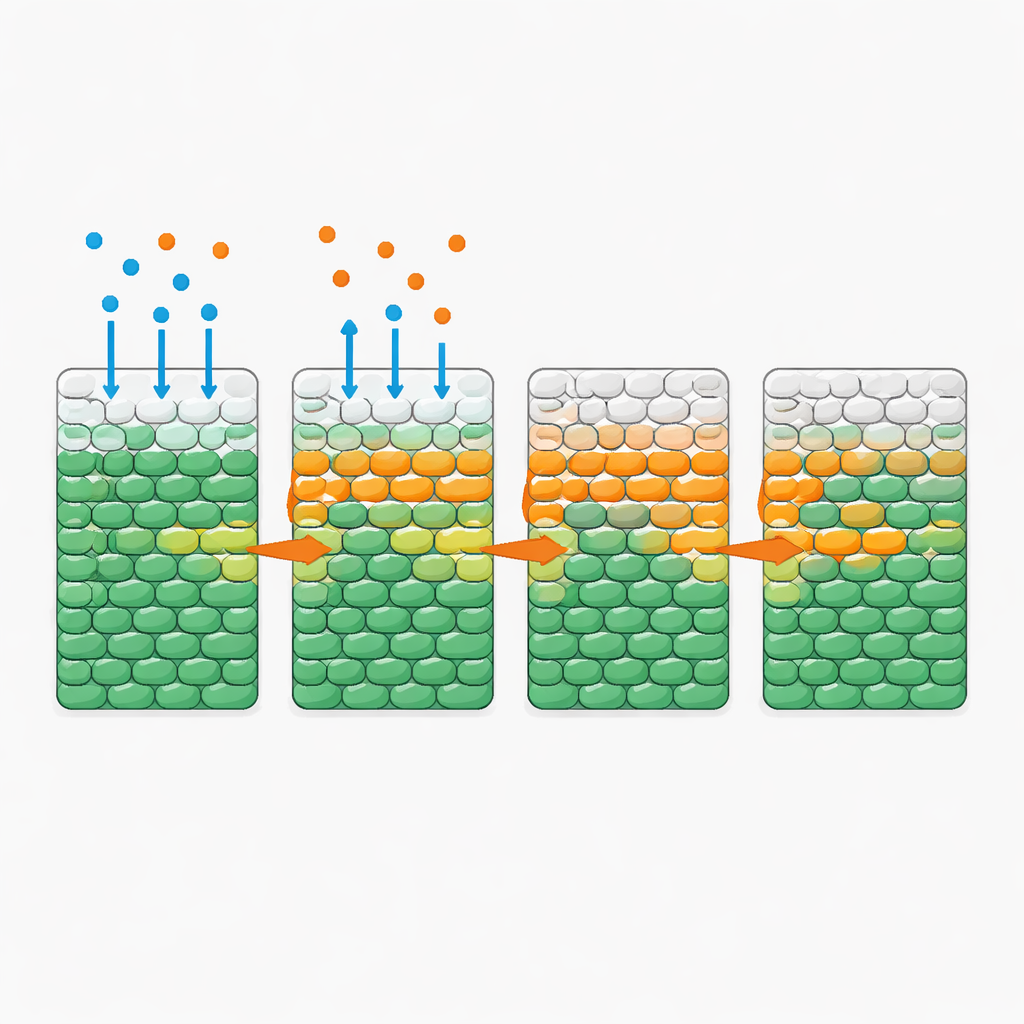
Простые правила за сложным рисунком
Чтобы количественно понять эту динамику, авторы создали математическую модель, отслеживающую три компонента: бактерии, питательное вещество и антибиотик. В модели питательное вещество и антибиотик диффундируют через популяцию; клетки потребляют питательное вещество для роста; и при достаточной экспозиции антибиотика и наличии питательного вещества в течение определённого времени они сначала размножаются, а затем погибают. Все параметры были измерены независимо в хорошо перемешанных культурах, поэтому модель не требовала подстройки для пространственных экспериментов. Тем не менее её симуляции воспроизвели наблюдаемые фронты смерти и их зависимость от уровня питательных веществ, плотности клеток и скорости потребления. Анализ модели выявил ключевую безразмерную величину, сравнивающую время, за которое клетки растут и умирают под действием антибиотика, со временем, за которое они истощают местный запас питательных веществ. Когда питательные вещества исчерпываются быстро, внутренние клетки остаются голодными и поэтому в значительной степени защищены; когда потребление медленное, питательные вещества проникают глубоко, и фронт может пройти через всю популяцию.
Как возникают выживание и восстановление
Бактериальные популяции редко бывают однородны по своей чувствительности к препаратам, даже при одинаковом генетическом фоне клеток. Команда использовала свою платформу, чтобы изучить, что происходит, когда некоторые клетки более резистентны, чем другие. При промежуточных дозах антибиотика фронт смерти всё ещё формировался и продвигался внутрь, но после его прохождения разбросанные микроколонии более устойчивых клеток начинали восстанавливаться в его тылу, питаясь питательными веществами, высвободившимися в теперь более пустых областях. Снижение дозы антибиотика или увеличение начальной плотности клеток усиливало это восстановление. В структурированных популяциях многие такие устойчивые очаги могут сосуществовать бок о бок, в отличие от хорошо перемешанных культур, где обычно доминирует единственный победитель. Такая картина может дать инфекциям больше шансов эволюционировать повышенную устойчивость или восстановиться после лечения.
Что это значит для лечения инфекций
Эта работа показывает, что доступность питательных веществ — это не просто фоновая деталь, а центральное узкое место, которое может либо обеспечивать, либо ограничивать убивающее действие антибиотиков в структурированных бактериальных популяциях. Вместо того чтобы просто выяснять, достигает ли препарат места инфекции, клиницисты и исследователи также должны учитывать, как источники питания проникают через сообщество и как быстро клетки их потребляют. Рамки исследования, включая простую метрику для оценки, когда потребление питательных веществ опережает действие антибиотика, предлагают способ предсказать, когда лечение, вероятно, остановится на защитной оболочке. Это также указывает, что сочетание антибиотиков со стратегиями, изменяющими проникновение питательных веществ или нарушающими пространственную структуру, может повысить эффективность существующих препаратов, и поясняет, почему плотные, подобные биоплёнкам инфекции могут быть столь упорными даже при положительных лабораторных тестах препарата.
Цитирование: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Ключевые слова: устойчивость к антибиотикам, бактериальные биопленки, градиенты питательных веществ, фосфомицин, динамика микробных популяций