Clear Sky Science · ar
عنق زجاجة غذائي يتحكّم في فعالية المضاد الحيوي في تجمعات بكتيرية منظمة
لماذا هذا مهم في العدوى
غالباً ما تُختبر المضادات الحيوية في أنابيب اختبار مختلطة جيدًا، بينما تتضمن العديد من العدوى الحقيقية مجتمعات بكتيرية كثيفة ملتصقة بالأنسجة أو الأجهزة الطبية. في هذه البيئات المزدحمة، تتسرب المواد الغذائية والأدوية من الخارج مكوّنة تدرجات كيميائية حادة لا تلتقطها اختبارات المختبر عادة. يطرح هذا العمل سؤالاً بسيطًا لكنه قويًا: هل يمكن لطريقة تدفق المغذّيات عبر هذه التجمعات البكتيرية المنظمة أن تتحكم في مدى فعالية المضادات الحيوية—وحتى تساعد جيوبًا من البكتيريا على النجاة والعودة إلى النمو؟
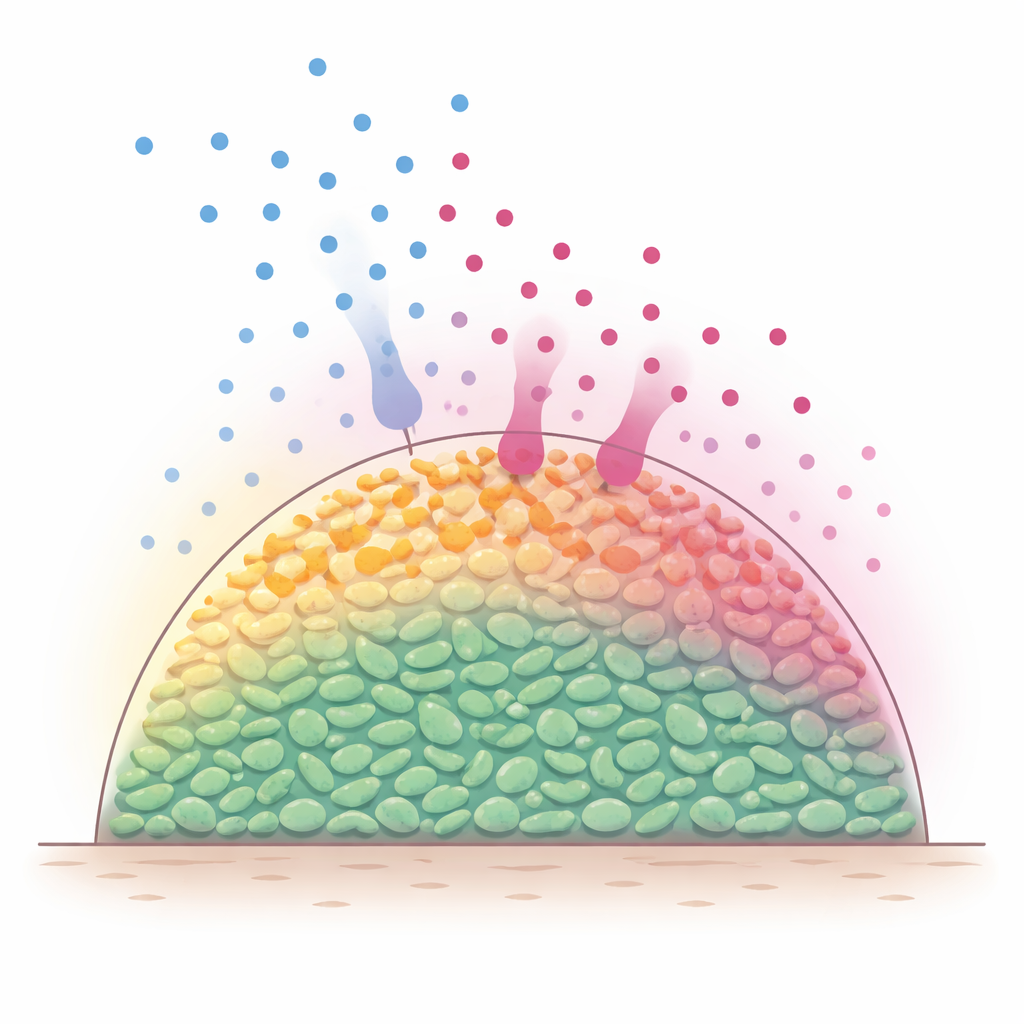
طبقات مخفية داخل المجتمعات البكتيرية
في البيئات الطبيعية، تعيش البكتيريا كثيرًا في تجمعات متعددة الخلايا، تُعرف أحيانًا بالطبقات الحيوية (biofilms)، حيث تتكدّس الخلايا ثلاثية الأبعاد. تتوغّل جزيئات المغذّيات، مثل السكريات، من الخارج وتُستهلك سريعًا بواسطة الخلايا السطحية. ونتيجة لذلك تظل الطبقات السطحية نشطة أيضيًا، بينما تصبح الخلايا الأعمق مجوعة وبطيئة الأيض. وبما أن العديد من المضادات الحيوية تكون أكثر فعالية ضد البكتيريا النامية بنشاط، فقد اشتبه العلماء منذ زمن طويل أن هذه التدرجات المتأصلة في المغذّيات تخلق باطنًا محميًا يصعب قتله. ومع ذلك، كان من الصعب مراقبة ما يحدث داخل مثل هذه التجمعات الكثيفة بينما تتحرك المغذّيات والمضادات الحيوية وتتفاعل مع الزمن.
بناء «طبقة حيوية مصغرة» قابلة للتحكم
لمعالجة هذا التحدي، حبَس الباحثون بكتيريا E. coli داخل مصفوفات هلامية شفافة—مواد طرية مملوءة بالماء تُثبّت الخلايا في مكانها لكنها تسمح للجزيئات الصغيرة بالانتشار. كان أحد جانبي كل كتلة هلامية يحتوي على بكتيريا لكن بدون مغذّيات أو أدوية؛ بينما احتوى الجانب الآخر على خزان من السكر (الجلوكوز)، أو المضاد الحيوي (الفوسفوميسين)، أو كليهما. بفتح فاصلة بين النصفين، سمح الفريق للجزيئات بالانتشار ببطء مع استخدام المجهر الوميضي لتمييز الخلايا الحية عن الميتة. تحاكي هذه البنية مقطعًا عرضيًا لطبقة حيوية، مع العالم الخارجي على جانب والداخل المحمي على الجانب الآخر، لكنها تمنح تحكمًا تجريبيًا أكثر إحكامًا بكثير من العينات الطبيعية.
عندما يفتح الطعام الفعل القاتل
بشكل مفاجئ، عندما تسرب المضاد الحيوي بمفرده إلى منطقة البكتيريا—حتى بجرعات تفوق بكثير مستويات التثبيط القياسية—بقيت معظم الخلايا حية طوال يوم كامل. تغيرت الصورة جذريًا عندما أُضيفت كمية متواضعة من الجلوكوز مع المضاد الحيوي. في هذه الحالة، لاحظ الفريق «جبهة مميتة» حادة بشكل لافت تجتاح الداخل من الجانب المعرض: طبقة متقدمة تتحول فيها الخلايا الحية فجأة إلى خلايا ميتة. كانت سرعة هذه الجبهة تعتمد بشدة على إمداد المغذّي واستهلاكه، لكنها كانت غير حساسة إلى حد كبير لكمية المضاد الحيوي الإضافية بعد تجاوزها عتبة معينة. فالمزيد من السكر سرّع الجبهة؛ بينما المزيد من الخلايا، التي استهلكت السكر جماعيًا أسرع، أبطأها. ظهر سلوك مماثل مع عدة مغذّيات ومضادات حيوية أخرى، مما يشير إلى مبدأ عام بدلاً من خصوصية دواء واحد.
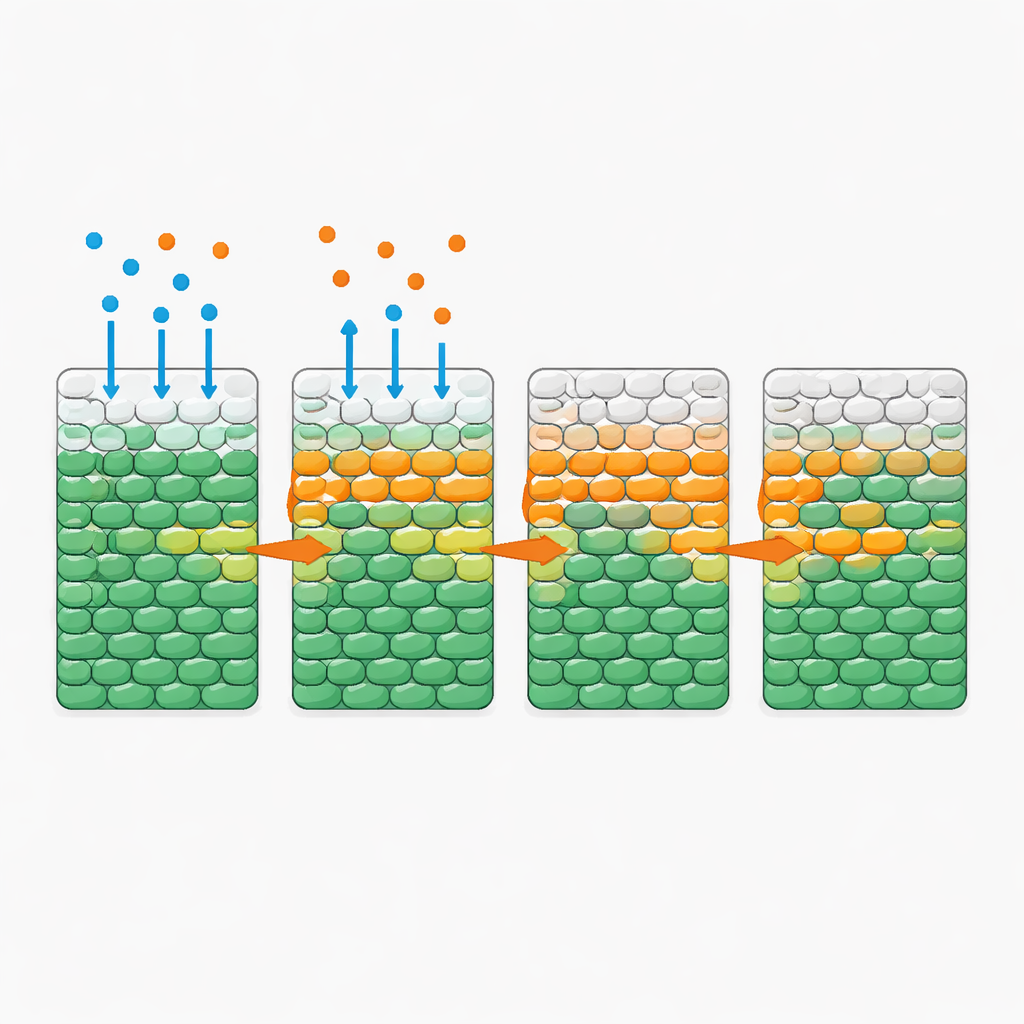
قواعد بسيطة وراء نمط معقّد
لفهم هذه الديناميكيات كميًا، بنى المؤلفون نموذجًا رياضيًا يتتبّع ثلاثة مكونات: البكتيريا، والمغذّي، والمضاد الحيوي. في النموذج، ينتشر المغذّي والمضاد الحيوي عبر التجمع؛ تستهلك الخلايا المغذّي لتنمو؛ ومتى تعرضت لما يكفي من المضاد الحيوي والمغذّي لفترة كافية، فإنها أولًا تتكاثر ثم تموت. جميع المعلمات قيسَت بشكل مستقل في مزروعات مختلطة جيدًا، لذا لم يتطلب النموذج أي تعديل لتجارب المساحة. ومع ذلك، أعادت محاكاته إنتاج الجبهات المميتة المرصودة واعتمادها على مستوى المغذّي وكثافة الخلايا ومعدل الاستهلاك. كشفت تحليلات النموذج عن كمية بلا بعد أساسية تقارن الزمن اللازم لنمو وموت الخلايا تحت التعرض للمضاد الحيوي مع الزمن اللازم لاستنفاد الإمداد المحلي من المغذّي. عندما يُستهلك المغذّي بسرعة، تبقى الخلايا الداخلية مجوعة وبذلك محمية إلى حد كبير؛ وعندما يكون الاستهلاك بطيئًا، يتوغّل المغذّي بعمق ويمكن للجبهة أن تجتاح كامل التجمع.
كيف تنشأ النجاة وإعادة النمو
نادرًا ما تكون تجمعات البكتيريا متجانسة في حساسيتها للأدوية، حتى عندما تشترك الخلايا في الخلفية الجينية نفسها. استخدم الفريق منصتهم لاستكشاف ما يحدث عندما تكون بعض الخلايا أكثر مقاومة من غيرها. عند جرعات متوسطة من المضاد الحيوي، استمرت الجبهة المميتة بالتشكّل والتحرّك إلى الداخل، لكن بعد مرورها بدأت مستعمرات دقيقة متناثرة من الخلايا الأكثر مقاومة في إعادة النمو خلفها، متغذية على المغذّيات التي أُطلقت في مناطق أصبحت أكثر خلوًا. إن خفض جرعة المضاد الحيوي أو زيادة كثافة الخلايا الابتدائية ضاعف من هذا إعادة النمو. في التجمعات المهيكلة، يمكن أن تبقى العديد من هذه الجيوب المقاومة جنبًا إلى جنب، خلافًا للمزارع المختلطة حيث يهيمن عادة فائز واحد. قد يمنح هذا النمط العدوى فرصًا أكثر لتطوّر مقاومة أعلى أو للانتعاش بعد العلاج.
ماذا يعني هذا لعلاج العدوى
يُظهر هذا العمل أن توافر المغذّيات ليس تفصيلًا ثانويًا بل عنق زجاجة مركزيًا يمكنه أن يتيح أو يحدّ القتل بالمضاد الحيوي في التجمعات البكتيرية المهيكلة. بدلًا من السؤال ببساطة ما إذا كان الدواء يمكنه الوصول إلى موقع العدوى، قد يحتاج الأطباء والباحثون أيضًا إلى السؤال كيف تتدفق مصادر الغذاء عبر المجتمع وبأي سرعة تستهلكها الخلايا. يوفر إطار الدراسة، بما في ذلك مقياسها البسيط لمتى يتجاوز استهلاك المغذّي معدل القتل، طريقة للتنبؤ متى سيتوقف العلاج بالمضاد الحيوي على قشرة حماية. كما يقترح أن الجمع بين المضادات الحيوية واستراتيجيات تغيّر اختراق المغذّي أو تزعزع البنية المكانية قد يجعل الأدوية الحالية أكثر فعالية، ويبيّن لماذا يمكن أن تكون العدوى الكثيفة الشبيهة بالطبقات الحيوية عنيدة حتى عندما تشير اختبارات المختبر إلى أن الدواء ينبغي أن يعمل.
الاستشهاد: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
الكلمات المفتاحية: مقاومة المضادات الحيوية, الطبقات البكتيرية الحيوية, تدرجات المغذّيات, فوسفوميسين, ديناميكيات التجمعات الميكروبية