Clear Sky Science · nl
Een voedingsknelpunt bepaalt de effectiviteit van antibiotica in gestructureerde bacteriële populaties
Waarom dit belangrijk is voor infecties
Antibiotica worden vaak getest in goed gemengde reageerbuizen, terwijl veel echte infecties bestaan uit dicht opeengepakte bacteriële gemeenschappen die aan weefsels of medische hulpmiddelen kleven. In deze drukke omgevingen sijpelen voedingsstoffen en medicijnen van buiten naar binnen en ontstaan scherpe chemische gradiënten die laboratoriumtests zelden vastleggen. Deze studie stelt een eenvoudige maar krachtige vraag: kan de manier waarop voedingsstoffen door zulke gestructureerde bacteriële populaties stromen bepalen hoe goed antibiotica werken — en zelfs helpen dat stukjes bacteriën overleven en terugkomen?
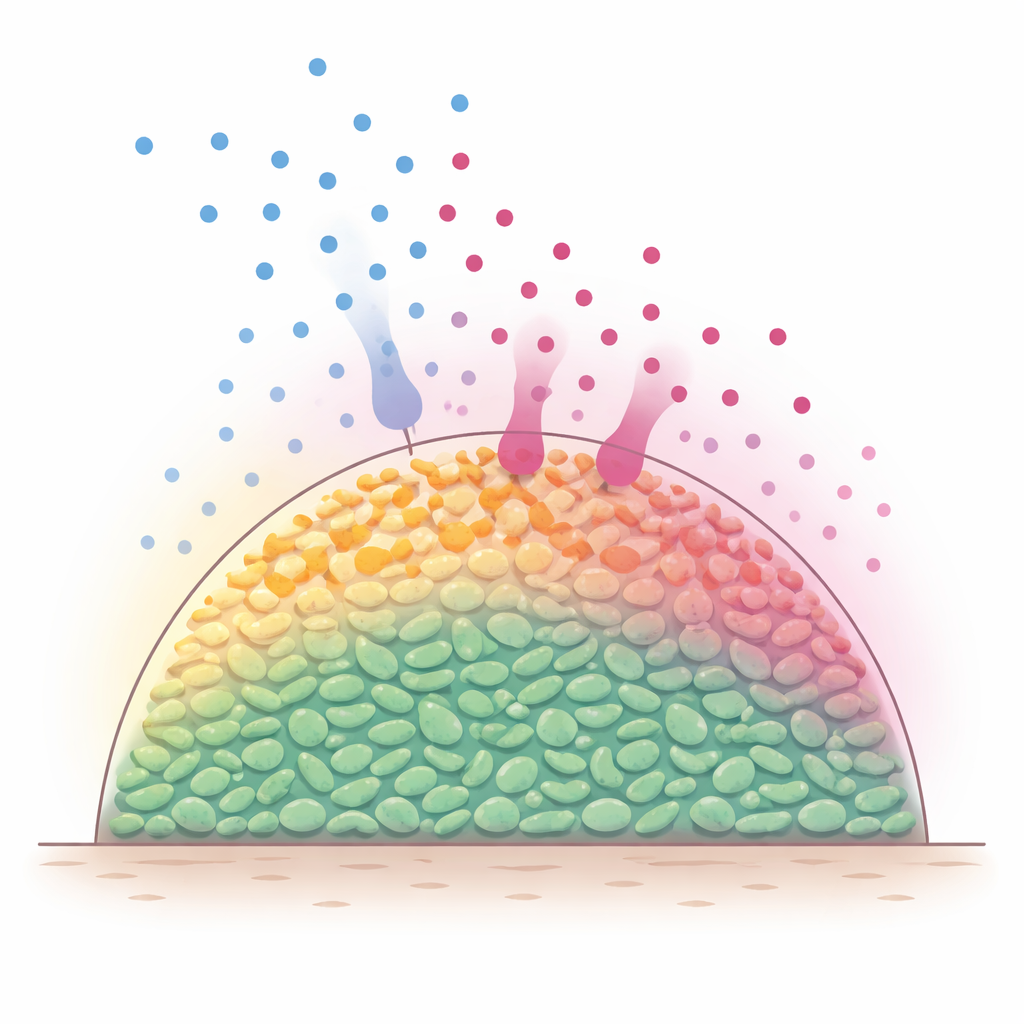
Verborgen lagen binnen bacteriële gemeenschappen
In natuurlijke omstandigheden leven bacteriën vaak in meercellige assemblages, soms biofilms genoemd, waarin cellen driedimensionaal op elkaar gepakt zitten. Voedingsmoleculen, zoals suikers, diffunderen van buiten naar binnen en worden snel opgegeten door de buitenste cellagen. Hierdoor blijven de oppervlaktelagen metabolisch actief, terwijl diepere cellen uitgehongerd en traag worden. Omdat veel antibiotica het meest effectief zijn tegen actief groeiende bacteriën, vermoeden wetenschappers al lang dat deze ingebouwde voedingsgradiënten een afgeschermd interieur creëren dat moeilijker te doden is. Het is echter lastig geweest om direct te volgen wat er binnen zulke dichte populaties gebeurt terwijl voedingsstoffen en antibiotica in de tijd bewegen en reageren.
Het bouwen van een bestuurbare mini-biofilm
Om deze uitdaging aan te pakken, vingen de onderzoekers E. coli-bacteriën op in transparante hydrogelmatrices — zachte, met water gevulde materialen waarvan de poriën cellen op hun plaats houden maar kleine moleculen toch laten diffunderen. Eén kant van elk gelblok bevatte bacteriën maar geen voedingsstoffen of medicijnen; de andere kant hield een reservoir met suiker (glucose), antibioticum (fosfomycine), of beide. Door een scheiding tussen de twee helften te verwijderen, konden de onderzoekers moleculen langzaam laten diffunderen terwijl ze met fluorescentiemicroscopie levende cellen van dode onderscheidden. Deze opstelling bootst een dwarsdoorsnede van een biofilm na, met de buitenwereld aan de ene kant en het beschermde interieur aan de andere, maar met veel striktere experimentele controle dan in natuurlijke monsters.
Wanneer voedsel dodelijke werking ontgrendelt
Verrassend genoeg bleven de meeste cellen, wanneer alleen het antibioticum in het bacteriële gebied diffundeerde — zelfs bij doses ver boven de standaard remmende niveaus — een hele dag in leven. Het beeld veranderde drastisch wanneer een bescheiden hoeveelheid glucose samen met het antibioticum werd toegevoegd. In dat geval zagen de onderzoekers een opvallend scherpe “doodsfront” dat van de blootgestelde zijde naar binnen schoof: een voortschrijdende laag waar levende cellen abrupt plaatsmaakten voor dode. De snelheid van dit front hing sterk af van de aanvoer en het verbruik van voedingsstoffen, maar was grotendeels ongevoelig voor hoeveel extra antibioticum werd toegevoegd zodra een bepaalde drempel was overschreden. Meer suiker versnelde het front; meer cellen, die samen de suiker sneller verbruikten, vertraagden het. Vergelijkbaar gedrag trad op met meerdere andere voedingsstoffen en antibiotica, wat wijst op een algemeen principe in plaats van een eigenaardigheid van één enkel geneesmiddel.
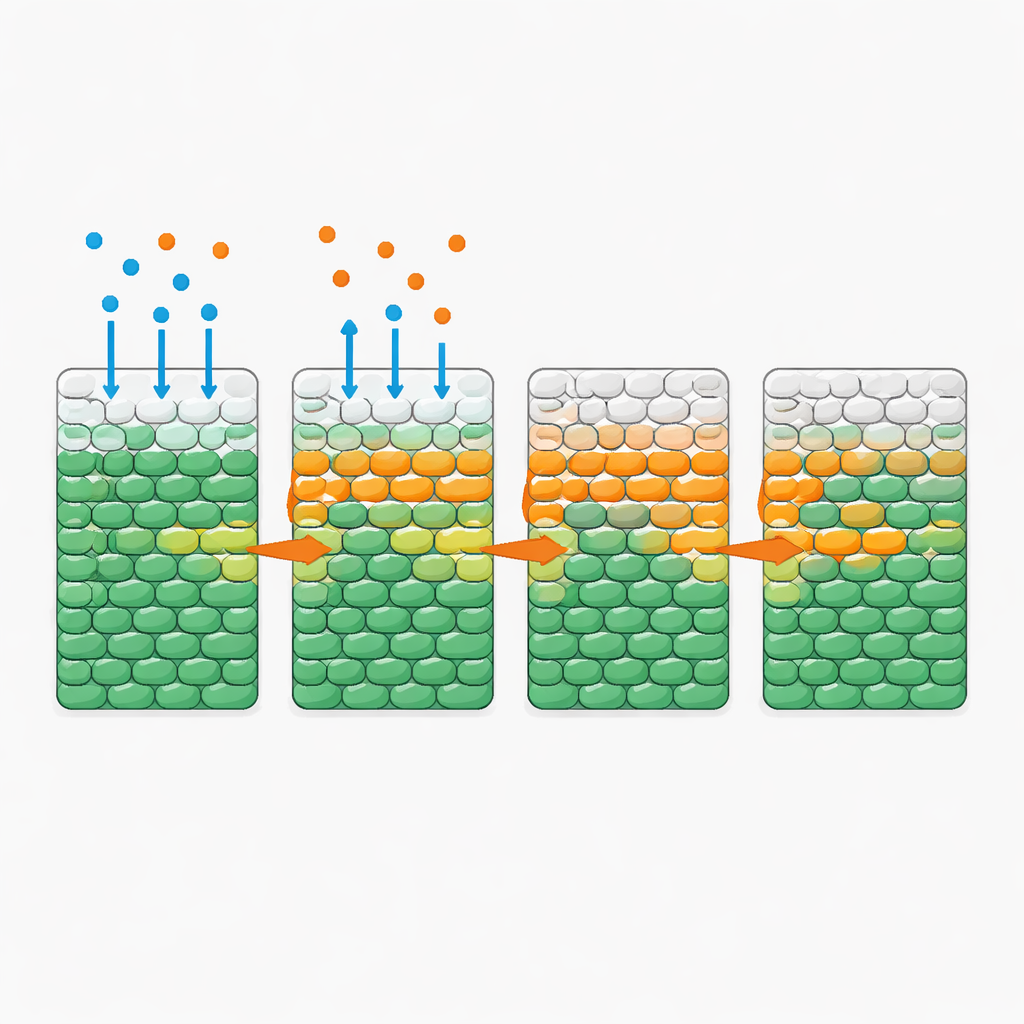
Eenvoudige regels achter een complex patroon
Om deze dynamiek kwantitatief te begrijpen, bouwden de auteurs een wiskundig model dat drie bestanddelen volgt: bacteriën, voedingsstof en antibioticum. In het model diffunderen voedingsstof en antibioticum door de populatie; cellen verbruiken voedingsstof om te groeien; en zodra ze lang genoeg aan voldoende antibioticum en voedingsstof zijn blootgesteld, vermenigvuldigen ze zich eerst en sterven daarna. Alle parameters waren onafhankelijk gemeten in goed gemengde culturen, zodat het model geen bijstelling nodig had voor de ruimtelijke experimenten. Toch reproduceerden de simulaties de waargenomen doodsfronten en hun afhankelijkheid van voedingsniveau, celdichtheid en verbruikssnelheid. Analyse van het model onthulde een belangrijke dimensieloos grootheid die de tijd vergelijkt die cellen nodig hebben om te groeien en te sterven onder antibioticumexpositie met de tijd die ze nodig hebben om hun lokale voedingsvoorraad uit te putten. Wanneer voedingsstoffen snel op raken, blijven innerlijke cellen uitgehongerd en dus grotendeels beschermd; wanneer verbruik traag is, dringt voeding diep door en kan het front door de hele populatie vegen.
Hoe overleving en herv groei ontstaan
Bacteriële populaties zijn zelden uniform in hun gevoeligheid voor geneesmiddelen, zelfs wanneer de cellen dezelfde genetische achtergrond delen. Het team gebruikte hun platform om te onderzoeken wat er gebeurt wanneer sommige cellen resistenter zijn dan andere. Bij intermediaire antibiotica-doses vormde het doodsfront zich nog steeds en bewoog naar binnen, maar nadat het gepasseerd was, begonnen verspreide microkolonies van meer resistente cellen zich in zijn kielzog te hergroeien, gevoed door voedingsstoffen die in de inmiddels leegere gebieden vrijkwamen. Het verlagen van de antibioticumdosis of het verhogen van de beginceldichtheid versterkte deze hergroei. In gestructureerde populaties kunnen veel van zulke resistente pocketjes naast elkaar blijven bestaan, in tegenstelling tot goed gemengde culturen waar doorgaans één winnaar domineert. Dit patroon kan infecties meer kansen geven om hogere resistentie te ontwikkelen of te herstellen na behandeling.
Wat dit betekent voor de behandeling van infecties
Dit werk toont aan dat de beschikbaarheid van voedingsstoffen niet slechts een achtergronddetail is, maar een centraal knelpunt dat het doden door antibiotica in gestructureerde bacteriële populaties kan mogelijk maken of beperken. In plaats van alleen te vragen of een medicijn een infectieplek kan bereiken, moeten clinici en onderzoekers mogelijk ook nagaan hoe voedselbronnen door de gemeenschap stromen en hoe snel cellen ze verbruiken. Het raamwerk van de studie, inclusief zijn eenvoudige maat voor wanneer voedingsverbruik het doden overtreft, biedt een manier om te voorspellen wanneer een antibiotische behandeling waarschijnlijk strandt bij een beschermende schil. Het suggereert ook dat het combineren van antibiotica met strategieën die de penetratie van voedingsstoffen veranderen of de ruimtelijke structuur verstoren bestaande geneesmiddelen effectiever kan maken, en verklaart waarom dichte, biofilmachtige infecties zo hardnekkig kunnen zijn, zelfs wanneer labtests aangeven dat een medicijn zou moeten werken.
Bronvermelding: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Trefwoorden: antibioticaresistentie, bacteriële biofilms, voedingsgradiënten, fosfomycine, microbiële populatiedynamica