Clear Sky Science · sv
En näringsflaskhals styr antibiotikas effektivitet i strukturerade bakteriepopulationer
Varför detta är viktigt för infektioner
Antibiotika testas ofta i välblandade provrör, men många verkliga infektioner involverar täta bakteriesamhällen som klamrar sig fast vid vävnader eller medicinska implantat. I dessa trånga miljöer sipprar näring och läkemedel in från utsidan och skapar skarpa kemiska gradienter som labbtester sällan fångar. Denna studie ställer en enkel men kraftfull fråga: kan sättet som näringsämnen flödar genom dessa strukturerade bakteriepopulationer styra hur väl antibiotika fungerar — och till och med hjälpa fickor av bakterier att överleva och komma tillbaka?
Dolda lager inom bakteriesamhällen
I naturliga miljöer lever bakterier ofta i flercelliga samlingar, ibland kallade biofilmer, där cellerna packas ihop i tre dimensioner. Näringsmolekyler, såsom socker, diffunderar in från utsidan och äts snabbt upp av de yttersta cellerna. Som ett resultat förblir ytlagren metabolt aktiva, medan djupare celler blir svälta och slöa. Eftersom många antibiotika är mest effektiva mot aktivt växande bakterier har forskare länge misstänkt att dessa inbyggda näringsgradienter skapar ett skyddat inre som är svårare att döda. Det har dock varit svårt att direkt iaktta vad som händer inuti sådana täta populationer när näringsämnen och antibiotika rör sig och reagerar över tid.
Bygga en kontrollerbar mini-biofilm
För att ta itu med denna utmaning fångade forskarna E. coli-bakterier inuti transparenta hydrogelmatriser — mjuka, vattenfyllda material vars porer håller cellerna på plats men ändå tillåter små molekyler att diffundera. Ena sidan av varje gelblock innehöll bakterier men inga näringsämnen eller läkemedel; den andra sidan innehöll ett reservoar med socker (glukos), antibiotika (fosfomycin) eller båda. Genom att ta bort en skiljevägg mellan de två halvorna kunde teamet låta molekyler långsamt diffundera samtidigt som de med fluorescensmikroskopi kunde skilja levande celler från döda. Denna uppställning efterliknar ett tvärsnitt av en biofilm, med omvärlden på ena sidan och det skyddade inre på den andra, men med mycket striktare experimentell kontroll än i naturliga prover.
När mat låser upp dödlig verkan
Överraskande nog förblev de flesta celler vid liv i ett helt dygn när antibiotikan ensam diffunderade in i bakterieregionen — även vid doser långt över standardhämmande nivåer. Bilden förändrades dramatiskt när en måttlig mängd glukos tillsattes tillsammans med antibiotikan. I det fallet observerade teamet en anmärkningsvärt skarp ”dödfront” som svepte in från den exponerade sidan: ett framryckande skikt där levande celler plötsligt gav vika för döda. Frontens hastighet berodde starkt på näringstillförseln och konsumtionen men var i stort sett okänslig för hur mycket extra antibiotika som tillfördes när det väl översteg en viss tröskel. Mer socker snabba upp fronten; fler celler, som tillsammans åt upp sockret snabbare, saktade ner den. Liknande beteende sågs med flera andra näringsämnen och antibiotika, vilket tyder på en allmän princip snarare än en knasighet hos ett enskilt läkemedel.
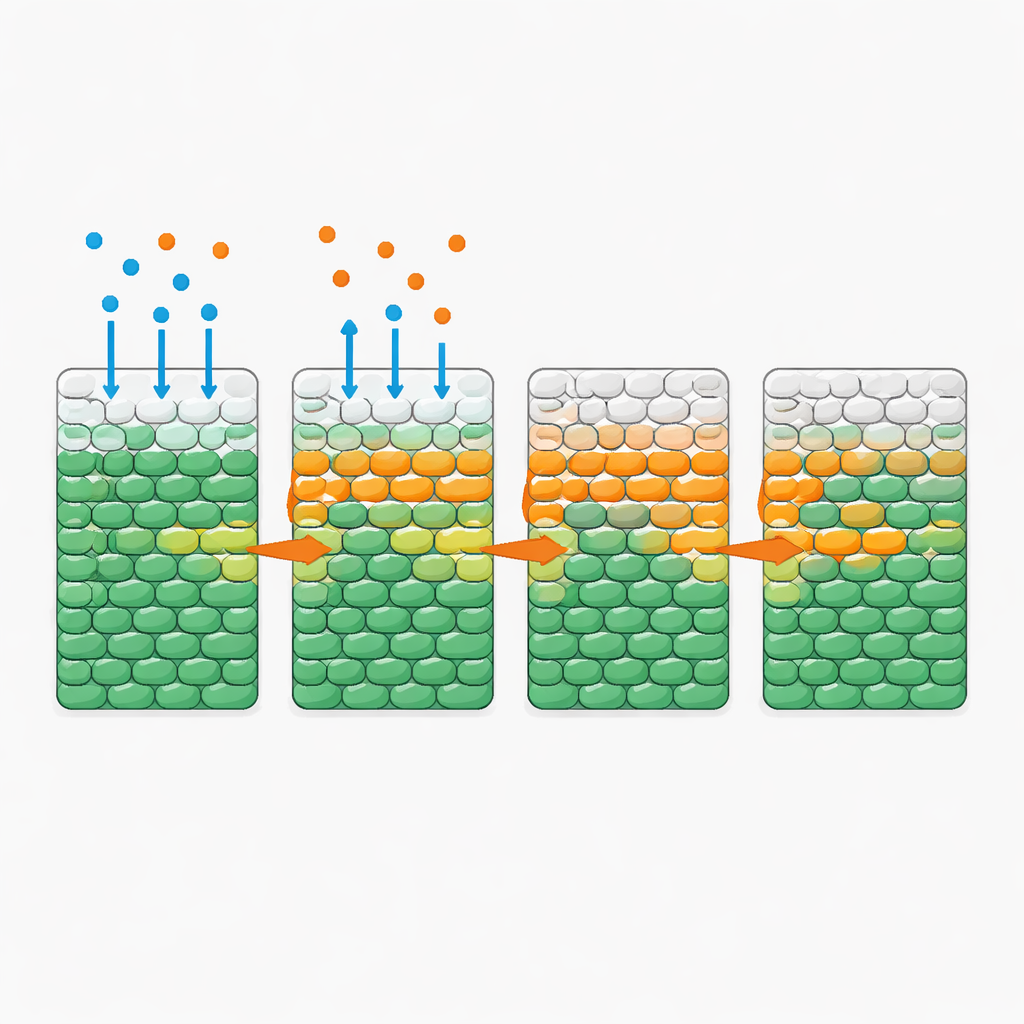
Enkla regler bakom ett komplext mönster
För att kvantitativt förstå dessa dynamiker byggde författarna en matematisk modell som följer tre ingredienser: bakterier, näring och antibiotika. I modellen diffunderar näring och antibiotika genom populationen; cellerna konsumerar näring för att växa; och när de utsätts för tillräckligt med antibiotika och näring under tillräckligt lång tid multiplicerar de först och dör sedan. Alla parametrar mättes oberoende i välblandade kulturer, så modellen krävde ingen justering för de rumsliga experimenten. Ändå reproducerade dess simuleringar de observerade dödfronterna och deras beroende av näringsnivå, celldensitet och konsumtionshastighet. Analys av modellen avslöjade en nyckel-dimensionlös storhet som jämför tiden det tar för cellerna att växa och dö under antibiotikaexponering med tiden det tar dem att tömma sitt lokala näringsförråd. När näringen förbrukas snabbt förblir de inre cellerna svälta och därmed i stort skyddade; när konsumtionen är långsam tränger näringen djupt och fronten kan svepa igenom hela populationen.
Hur överlevnad och återväxt uppstår
Bakteriepopulationer är sällan enhetliga i sin känslighet för läkemedel, även när cellerna delar samma genetiska bakgrund. Teamet använde sin plattform för att utforska vad som händer när vissa celler är mer resistenta än andra. Vid intermediära antibiotikadoser bildades och rörde sig dödfronten fortfarande inåt, men efter att den passerat började spridda mikrokolonier av mer resistenta celler att återväxa i dess kölvatten, och de utnyttjade näring som frigjordes i de nu mer tomma regionerna. Att sänka antibiotikadosen eller öka startcelldensiteten förstärkte denna återväxt. I strukturerade populationer kan många sådana resistenta fickor bestå sida vid sida, i kontrast till välblandade kulturer där typiskt en ensam vinnare dominerar. Detta mönster kan ge infektioner fler möjligheter att utveckla högre resistens eller återhämta sig efter behandling.
Vad detta betyder för behandling av infektioner
Denna forskning visar att näringstillgång inte bara är en bakgrundsdetalj utan en central flaskhals som antingen kan möjliggöra eller begränsa antibiotikadöd i strukturerade bakteriepopulationer. Istället för bara att fråga om ett läkemedel kan nå en infektionsplats kan kliniker och forskare också behöva fråga hur näringskällor flödar genom samhället och hur snabbt cellerna förbrukar dem. Studiens ramverk, inklusive dess enkla mått för när näringskonsumtion överstiger dödandet, erbjuder ett sätt att förutsäga när antibiotikabehandling sannolikt kommer att stanna vid ett skyddande skal. Det antyder också att kombinera antibiotika med strategier som ändrar näringspenetration eller stör den rumsliga strukturen skulle kunna göra befintliga läkemedel mer effektiva, och belyser varför täta, biofilmliknande infektioner kan vara så envisa även när labbtester säger att ett läkemedel borde fungera.
Citering: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Nyckelord: antibiotikaresistens, bakteriella biofilmer, näringsgradienter, fosfomycin, mikrobiell populationsdynamik