Clear Sky Science · de
Ein Nährstoff-Flaschenhals steuert die Wirksamkeit von Antibiotika in strukturierten bakteriellen Populationen
Warum das für Infektionen wichtig ist
Antibiotika werden oft in gut durchmischten Reagenzgläsern getestet, während viele reale Infektionen dichte bakterielle Gemeinschaften betreffen, die an Geweben oder medizinischen Geräten haften. In diesen überfüllten Umgebungen dringen Nährstoffe und Wirkstoffe von außen ein und erzeugen steile chemische Gradienten, die Laboruntersuchungen selten erfassen. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Kann die Art und Weise, wie Nährstoffe durch diese strukturierten bakteriellen Populationen fließen, die Wirksamkeit von Antibiotika steuern — und sogar Nischen von Bakterien das Überleben und die Erholung ermöglichen?
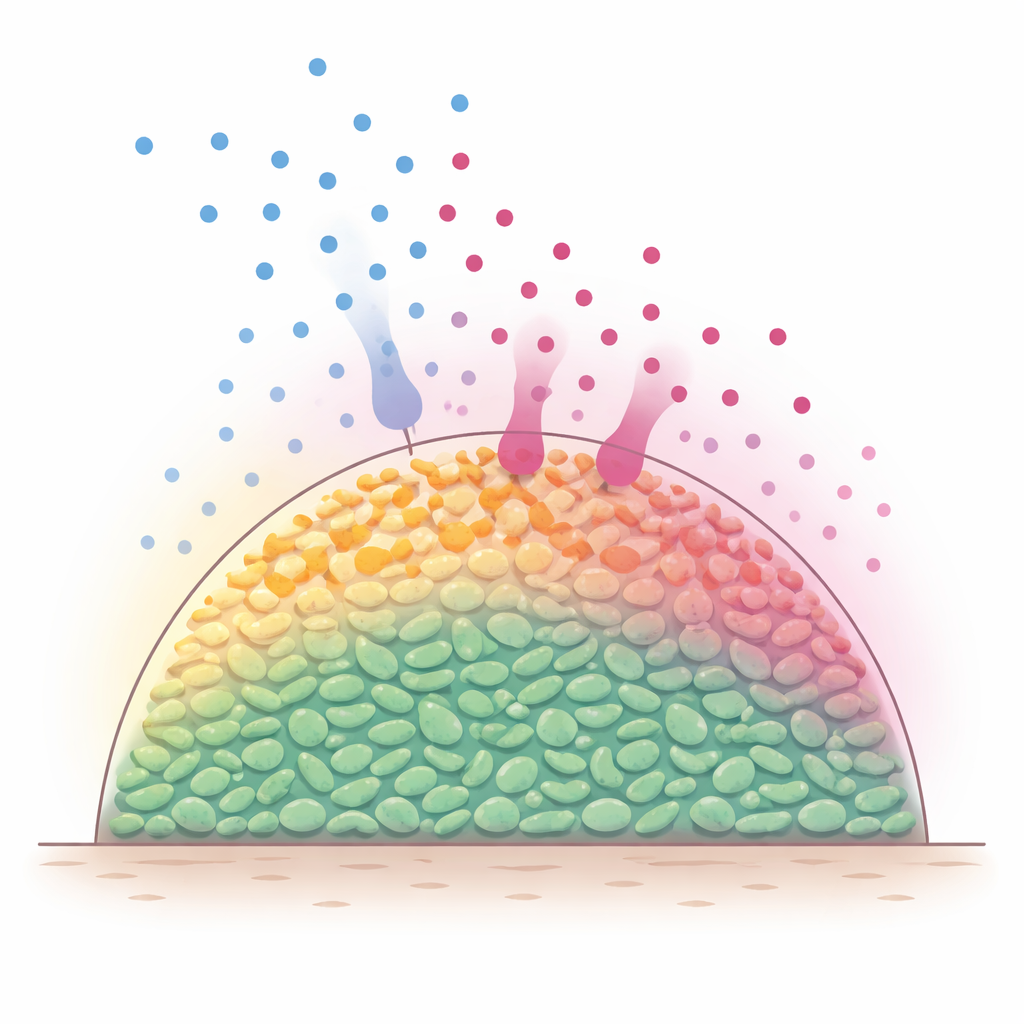
Verborgene Schichten innerhalb bakterieller Gemeinschaften
In natürlichen Umgebungen leben Bakterien häufig in mehrzelligen Verbänden, oft Biofilme genannt, in denen Zellen dreidimensional dicht gepackt sind. Nährstoffmoleküle wie Zucker diffundieren von außen hinein und werden schnell von den äußersten Zellen verbraucht. Folglich bleiben die Oberflächenschichten stoffwechselaktiv, während tiefere Zellen ausgehungert und träger werden. Da viele Antibiotika am effektivsten gegen aktiv wachsendes Bakterien wirken, vermuteten Forscher lange, dass diese eingebauten Nährstoffgradienten ein geschütztes Inneres bilden, das schwerer zu töten ist. Es war jedoch schwierig, direkt zu beobachten, was in solchen dichten Populationen geschieht, während Nährstoffe und Antibiotika sich mit der Zeit bewegen und reagieren.
Aufbau eines kontrollierbaren Mini-Biofilms
Um diese Herausforderung anzugehen, fingen die Forschenden E. coli-Bakterien in transparenten Hydrogelen ein — weichen, wassergefüllten Materialien, deren Poren die Zellen an Ort und Stelle halten, aber dennoch den Diffusionsfluss kleiner Moleküle erlauben. Eine Seite jedes Gelblocks enthielt Bakterien, aber keine Nährstoffe oder Wirkstoffe; die andere Seite hielt ein Reservoir aus Zucker (Glukose), Antibiotikum (Fosfomycin) oder beidem. Durch Entfernen einer Trennwand zwischen den beiden Hälften konnten die Forschenden Moleküle langsam diffundieren lassen und gleichzeitig mit Fluoreszenzmikroskopie lebende von toten Zellen unterscheiden. Dieses Setup ahmt einen Querschnitt durch einen Biofilm nach, mit der Außenwelt auf der einen Seite und dem geschützten Inneren auf der anderen, bietet jedoch viel engere experimentelle Kontrolle als natürliche Proben.
Wenn Nahrung tödliche Wirkung freischaltet
Erstaunlicherweise blieben die meisten Zellen einen ganzen Tag lang am Leben, wenn nur das Antibiotikum in die bakterielle Region diffundierte — selbst bei Dosen weit über den üblichen Hemmkonzentrationen. Das Bild änderte sich dramatisch, als eine mäßige Menge Glukose zusammen mit dem Antibiotikum hinzugefügt wurde. In diesem Fall beobachtete das Team eine auffallend scharfe „Todesfront“, die von der exponierten Seite nach innen vorrückte: eine voranschreitende Schicht, in der lebende Zellen abrupt toten wichen. Die Geschwindigkeit dieser Front hing stark von Nährstoffangebot und -verbrauch ab, war aber weitgehend unempfindlich gegenüber der zusätzlichen Antibiotikamenge, sobald ein bestimmter Schwellenwert überschritten war. Mehr Zucker beschleunigte die Front; mehr Zellen, die kollektiv den Zucker schneller verbrauchten, verlangsamten sie. Ähnliches Verhalten zeigte sich mit mehreren anderen Nährstoffen und Antibiotika, was auf ein allgemeines Prinzip und nicht auf eine Besonderheit eines einzelnen Wirkstoffs hinweist.
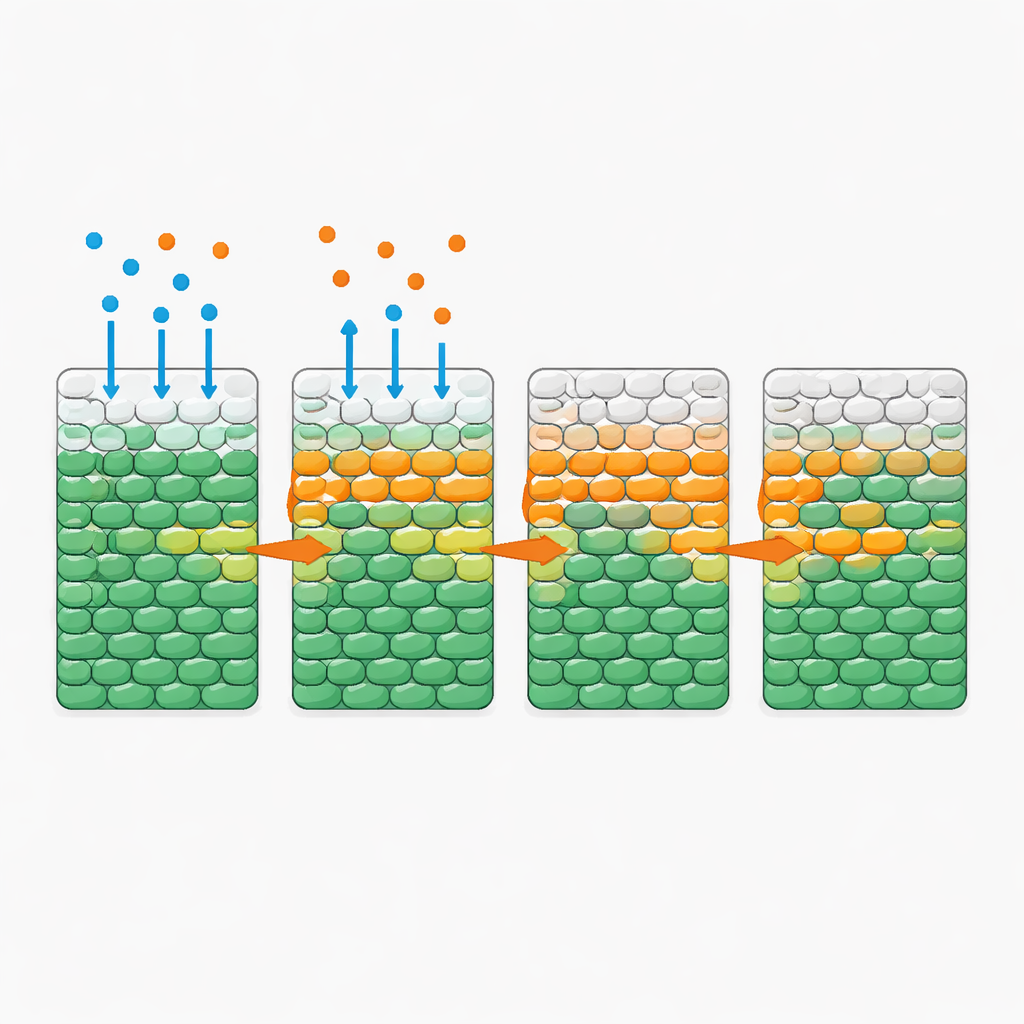
Einfache Regeln hinter einem komplexen Muster
Um diese Dynamik quantitativ zu verstehen, entwickelten die Autorinnen und Autoren ein mathematisches Modell, das drei Komponenten verfolgt: Bakterien, Nährstoff und Antibiotikum. Im Modell diffundieren Nährstoff und Antibiotikum durch die Population; Zellen verbrauchen Nährstoff zum Wachsen; und wenn sie lange genug ausreichend Antibiotikum und Nährstoff ausgesetzt sind, vermehren sie sich zunächst und sterben dann ab. Alle Parameter wurden unabhängig in gut durchmischten Kulturen gemessen, sodass das Modell für die räumlichen Experimente keiner Feinabstimmung bedurfte. Dennoch reproduzierten seine Simulationen die beobachteten Todesfronten und deren Abhängigkeit von Nährstoffniveau, Zelldichte und Verbrauchsrate. Die Analyse des Modells offenbarte eine wichtige dimensionslose Größe, die die Zeit zum Wachsen und Absterben unter Antibiotikabelastung mit der Zeit vergleicht, in der die lokale Nährstoffversorgung erschöpft wird. Wenn der Nährstoff schnell aufgebraucht ist, bleiben die inneren Zellen ausgehungert und damit weitgehend geschützt; ist der Verbrauch langsam, dringt der Nährstoff tief ein und die Front kann die gesamte Population durchlaufen.
Wie Überleben und Nachwachsen entstehen
Bakterielle Populationen sind selten einheitlich in ihrer Empfindlichkeit gegenüber Wirkstoffen, selbst wenn die Zellen denselben genetischen Hintergrund teilen. Das Team nutzte seine Plattform, um zu untersuchen, was passiert, wenn einige Zellen resistenter sind als andere. Bei mittleren Antibiotikadosen bildete sich die Todesfront weiterhin und zog nach innen, doch nachdem sie vorbeigezogen war, begannen verstreute Mikrokolonien resistenterer Zellen im Gefolge nachzuwachsen und ernährten sich von Nährstoffen, die in den nun leereren Regionen freigesetzt wurden. Das Senken der Antibiotikadosis oder Erhöhen der Anfangs-Zelldichte verstärkte dieses Nachwachsen. In strukturierten Populationen können viele solche resistenten Nischen nebeneinander bestehen, im Gegensatz zu gut durchmischten Kulturen, in denen typischerweise ein einzelner Gewinner dominiert. Dieses Muster könnte Infektionen mehr Möglichkeiten geben, höhere Resistenzen zu entwickeln oder nach der Behandlung zurückzuschlagen.
Was das für die Behandlung von Infektionen bedeutet
Diese Arbeit zeigt, dass die Verfügbarkeit von Nährstoffen nicht nur ein Hintergrunddetail ist, sondern ein zentrales Nadelöhr, das das Abtöten durch Antibiotika in strukturierten bakteriellen Populationen entweder ermöglicht oder begrenzt. Statt nur zu fragen, ob ein Wirkstoff einen Infektionsort erreicht, sollten Kliniker und Forschende auch betrachten, wie Nahrungsquellen durch die Gemeinschaft fließen und wie schnell Zellen sie verbrauchen. Das Rahmenwerk der Studie, einschließlich der einfachen Kennzahl dafür, wann der Nährstoffverbrauch das Abtöten überholt, bietet eine Möglichkeit vorherzusagen, wann eine Antibiotikabehandlung wahrscheinlich an einer schützenden Schale scheitert. Es legt außerdem nahe, dass die Kombination von Antibiotika mit Strategien, die die Nährstoffpenetration verändern oder die räumliche Struktur stören, vorhandene Medikamente wirksamer machen könnte, und erklärt, warum dichte, biofilmartige Infektionen so hartnäckig sein können, selbst wenn Labortests ein Wirkstoff wirken sollten.
Zitation: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Schlüsselwörter: Antibiotikaresistenz, bakterielle Biofilme, Nährstoffgradienten, Fosfomycin, mikrobielle Populationsdynamik