Clear Sky Science · es
Un cuello de botella nutricional controla la eficacia de los antibióticos en poblaciones bacterianas estructuradas
Por qué esto importa para las infecciones
Los antibióticos a menudo se prueban en tubos de ensayo bien mezclados, pero muchas infecciones reales implican comunidades bacterianas densas adheridas a tejidos o dispositivos médicos. En estos entornos abarrotados, los alimentos y los fármacos penetran desde el exterior, creando gradientes químicos pronunciados que las pruebas de laboratorio raramente capturan. Este estudio plantea una pregunta sencilla pero potente: ¿puede la forma en que los nutrientes fluyen a través de estas poblaciones bacterianas estructuradas controlar la eficacia de los antibióticos —e incluso ayudar a que bolsillos de bacterias sobrevivan y se recuperen?
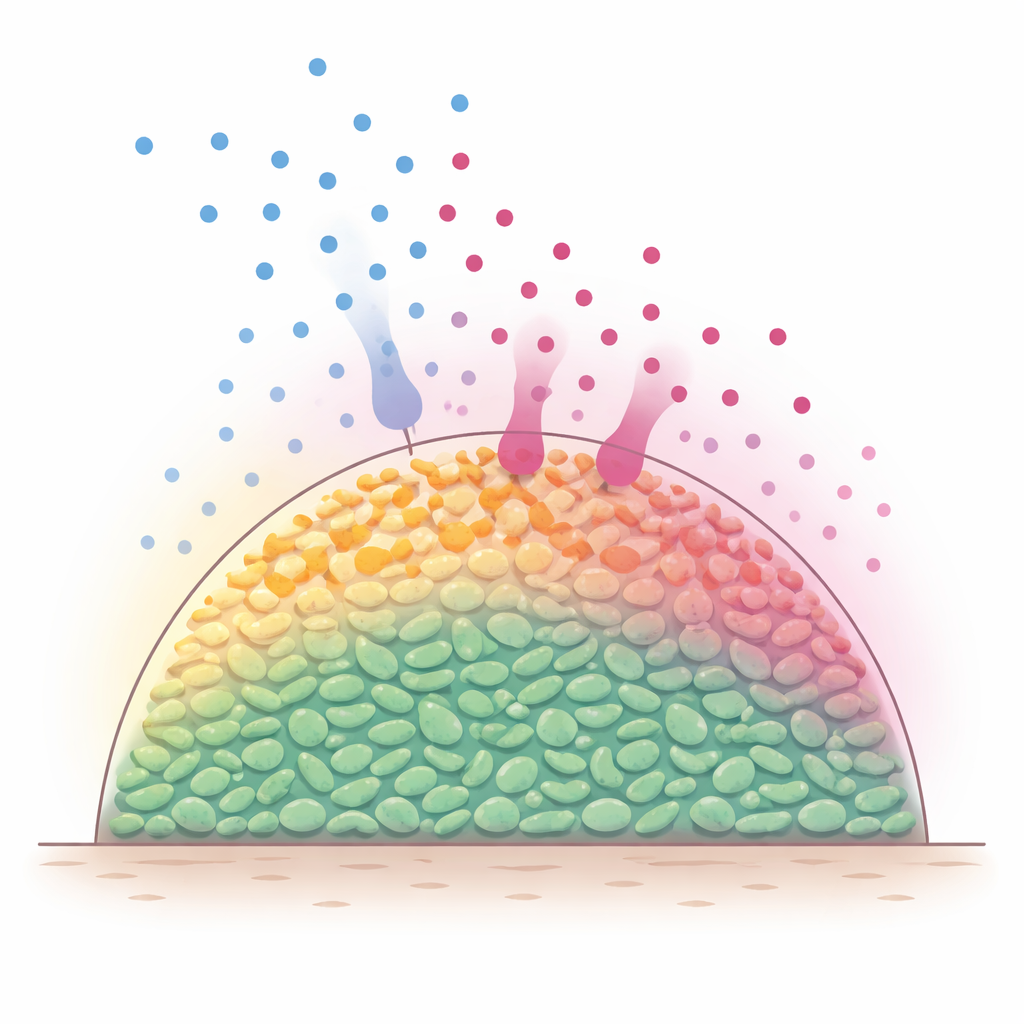
Capas ocultas dentro de las comunidades bacterianas
En entornos naturales, las bacterias con frecuencia viven en ensamblajes multicelulares, a veces llamados biopelículas, donde las células se empaquetan en tres dimensiones. Moléculas nutritivas, como los azúcares, difunden desde el exterior y son rápidamente consumidas por las células más externas. Como resultado, las capas superficiales permanecen metabólicamente activas, mientras que las células más profundas quedan privadas de alimento y ralentizadas. Dado que muchos antibióticos son más eficaces contra bacterias en crecimiento activo, los científicos han sospechado desde hace tiempo que estos gradientes nutricionales incorporados crean un interior protegido que es más difícil de matar. Sin embargo, ha sido difícil observar directamente lo que ocurre dentro de tales poblaciones densas a medida que nutrientes y antibióticos se desplazan y reaccionan con el tiempo.
Construir una mini-biopelícula controlable
Para abordar este desafío, los investigadores atraparon bacterias E. coli dentro de matrices de hidrogel transparentes: materiales suaves llenos de agua cuyos poros mantienen las células en su lugar pero permiten que difundan pequeñas moléculas. Un lado de cada bloque de gel contenía bacterias pero no nutrientes ni fármacos; el otro lado contenía un depósito de azúcar (glucosa), antibiótico (fosfomicina) o ambos. Al retirar un separador entre las dos mitades, el equipo permitió que las moléculas difundieran lentamente mientras usaba microscopía de fluorescencia para distinguir células vivas de células muertas. Esta configuración imita una sección transversal de una biopelícula, con el mundo exterior en un lado y el interior protegido en el otro, pero con un control experimental mucho más estricto que en las muestras naturales.
Cuando la comida desbloquea la acción letal
Sorprendentemente, cuando el antibiótico solo difundía hacia la región bacteriana —incluso a dosis muy superiores a los niveles inhibitorios estándar—, la mayoría de las células permanecieron vivas durante todo un día. El panorama cambió drásticamente cuando se añadió una cantidad moderada de glucosa junto con el antibiótico. En ese caso, el equipo observó un “frente de muerte” sorprendentemente nítido que barría hacia el interior desde el lado expuesto: una capa avanzada donde las células vivas daban paso abruptamente a células muertas. La velocidad de este frente dependía fuertemente del suministro y consumo de nutrientes, pero era en gran medida insensible a cuánto antibiótico adicional se añadiera una vez que superaba cierto umbral. Más azúcar aceleró el frente; más células, que colectivamente consumían el azúcar más rápido, lo ralentizaron. Un comportamiento similar apareció con varios otros nutrientes y antibióticos, lo que sugiere un principio general más que una rareza de un solo fármaco.
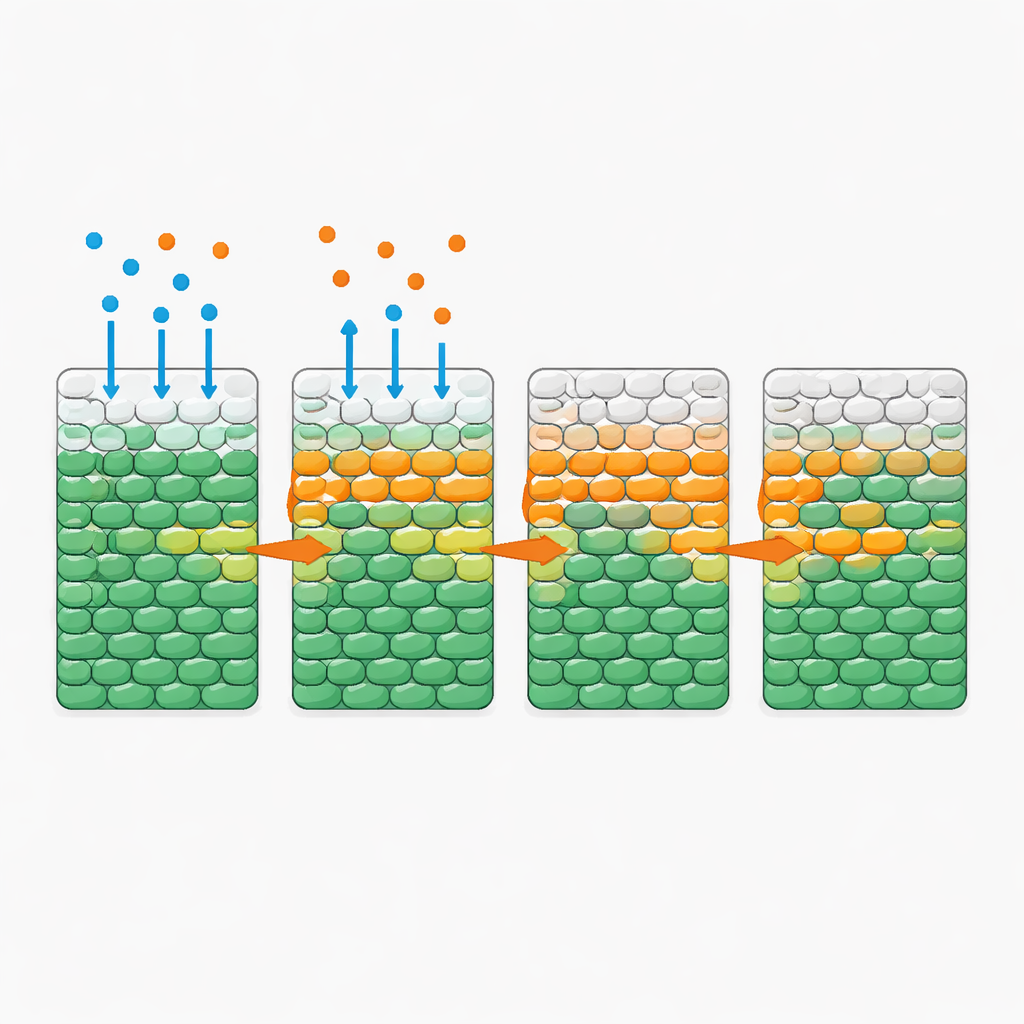
Reglas simples detrás de un patrón complejo
Para comprender cuantitativamente estas dinámicas, los autores construyeron un modelo matemático que rastrea tres ingredientes: bacterias, nutriente y antibiótico. En el modelo, nutriente y antibiótico difunden a través de la población; las células consumen nutriente para crecer; y una vez expuestas a suficiente antibiótico y nutriente durante el tiempo suficiente, primero se multiplican y luego mueren. Todos los parámetros se midieron de forma independiente en cultivos bien mezclados, por lo que el modelo no requirió ajuste para los experimentos espaciales. Aun así, sus simulaciones reprodujeron los frentes de muerte observados y su dependencia del nivel de nutrientes, densidad celular y tasa de consumo. El análisis del modelo reveló una cantidad adimensional clave que compara el tiempo que tardan las células en crecer y morir bajo exposición al antibiótico con el tiempo que tardan en agotar su suministro local de nutriente. Cuando el nutriente se agota rápidamente, las células internas permanecen hambrientas y, por tanto, en gran medida protegidas; cuando el consumo es lento, el nutriente penetra en profundidad y el frente puede barrer a través de toda la población.
Cómo emergen la supervivencia y la recolonización
Las poblaciones bacterianas rara vez son uniformes en su sensibilidad a los fármacos, incluso cuando las células comparten el mismo fondo genético. El equipo usó su plataforma para explorar qué ocurre cuando algunas células son más resistentes que otras. A dosis intermedias de antibiótico, el frente de muerte aún se formó y avanzó hacia el interior, pero tras su paso, microcolonias dispersas de células más resistentes comenzaron a volver a crecer en su estela, alimentándose de los nutrientes liberados en regiones ahora más vacías. Reducir la dosis de antibiótico o aumentar la densidad celular inicial amplificó esta recolonización. En poblaciones estructuradas, muchos de estos bolsillos resistentes pueden persistir lado a lado, en contraste con los cultivos bien mezclados donde típicamente domina un único ganador. Este patrón podría dar a las infecciones más oportunidades de evolucionar mayor resistencia o recuperarse después del tratamiento.
Qué significa esto para el tratamiento de infecciones
Este trabajo muestra que la disponibilidad de nutrientes no es solo un detalle de fondo, sino un cuello de botella central que puede permitir o limitar la acción bactericida de los antibióticos en poblaciones bacterianas estructuradas. En lugar de preguntar simplemente si un fármaco puede alcanzar el sitio de infección, clínicos e investigadores podrían también necesitar preguntar cómo fluyen las fuentes de alimento a través de la comunidad y con qué rapidez las células las consumen. El marco del estudio, incluido su métrico simple para cuando el consumo de nutrientes supera la capacidad de matar, ofrece una manera de predecir cuándo el tratamiento antibiótico probablemente se detendrá en una capa protectora. También sugiere que combinar antibióticos con estrategias que alteren la penetración de nutrientes o que perturben la estructura espacial podría hacer los fármacos existentes más eficaces, y pone de relieve por qué las infecciones densas, parecidas a biopelículas, pueden ser tan tenaces incluso cuando las pruebas de laboratorio indican que un fármaco debería funcionar.
Cita: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Palabras clave: resistencia a los antibióticos, biopelículas bacterianas, gradientes de nutrientes, fosfomicina, dinámica de poblaciones microbianas