Clear Sky Science · he
צוואר בקבוק תזונתי שולט ביעילות האנטיביוטיקה באוכלוסיות חיידקיות ממוספרות
מדוע זה חשוב לזיהומים
אנטיביוטיקה נבדקת לעתים קרובות בצינורות מבחנה מעורבבים היטב, אך רבים מהזיהומים בעולם האמיתי כוללים קהילות חיידקיות צפופות הדבקות לרקמות או למכשירים רפואיים. בהגדרות צפופות אלה המזון והתרופות מחלחלים מהחוץ ויוצרים גרדיאנטים כימיים חדים שמבחני מעבדה לעתים קרובות אינם משחזרים. המחקר שואל שאלה פשוטה אך עוצמתית: האם הדרך שבה מזון זורם דרך אוכלוסיות חיידקיות מובנות יכולה לקבוע עד כמה אנטיביוטיקה יעילה — ואפילו לעזור לכיסי חיידקים לשרוד ולשוב?
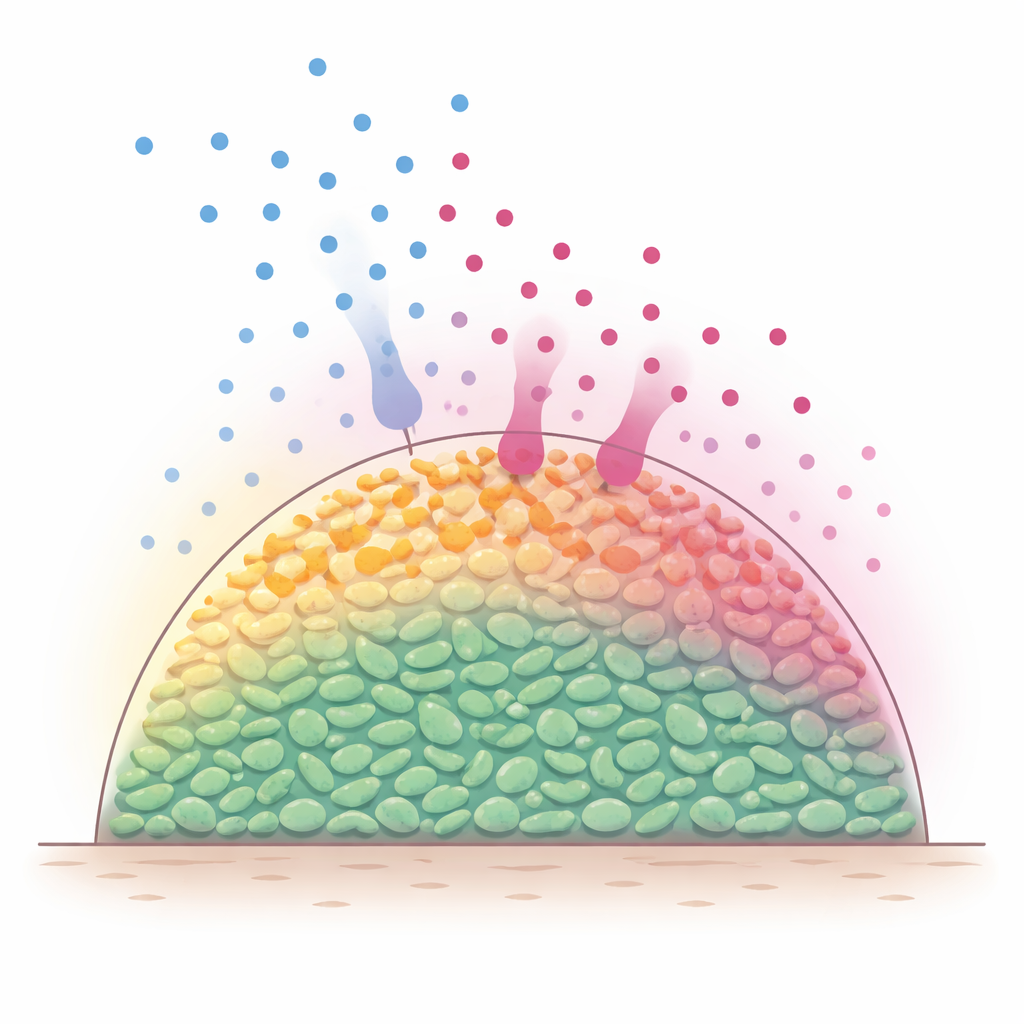
שכבות חבויות בתוך קהילות חיידקיות
במצבים טבעיים חיידקים חיים לעתים קרובות באסיפות רב-תאיות, שמכונים לעתים ביופילמים, שבהן התאים דחוסים בתלת־ממד. מולקולות מזון, כמו סוכרים, מדיפוזות מהחוץ ונאכלות במהירות על ידי התאים החיצוניים. כתוצאה מכך השכבות החיצוניות נשארות פעילות מטבולית, בעוד שהתאים העמוקים נרעבים ומאיטים. מאחר שאנטיביוטיקה רבות יעילות במיוחד נגד חיידקים בצמיחה פעילה, מדענים כבר חשדו שגרדיאנטים תזונתיים מובנים אלה יוצרים פנים מוגן שקשה יותר להרוג. עם זאת, קשה היה לצפות ישירות מה קורה בתוך אוכלוסיות צפופות כאלה בזמן שהמזון והאנטיביוטיקה זזים ומגיבים.
בניית מיני-ביופילם שניתן לשלוט בו
כדי להתמודד עם האתגר תקעו החוקרים חיידקי E. coli בתוך מטריצות הידרוג'ל שקופות — חומרים רכים מלאי מים הנמצאים בהם נקבים המחזיקים את התאים במקומם אך מאפשרים למולקולות קטנות לדיפוזה. צד אחד של כל קוביית ג'ל הכיל חיידקים אך לא מזון או תרופות; הצד השני הכיל מאגר של סוכר (גלוקוז), אנטיביוטיקה (פוספומיצין), או שניהם. על ידי הסרת מחיצה בין שני החצאים, הצוות איפשר למולקולות להתפשט לאט בזמן שהשתמשו במיקרוסקופיה פלואורסצנטית להבחין בין תאים חיים למתים. סידור זה מחקה חתך רוחב של ביופילם, עם העולם החיצון בצד אחד והחלק המוגן בצד השני, אך עם שליטה ניסויית הדוקה הרבה יותר מאשר בדגימות טבעיות.
מתי מזון מפעיל פעולה קטלנית
להפתעת החוקרים, כאשר האנטיביוטיקה לבדה חדרה לאזור החיידקים — גם במינונים שגבוהים בהרבה מהערכים המעכבים הסטנדרטיים — רוב התאים נשארו חיים במשך יום שלם. התמונה השתנתה באופן דרמטי כאשר הכנסו כמויות צנועות של גלוקוז יחד עם האנטיביוטיקה. במצב זה הצוות תיעד "חזית מוות" חדה להפליא שגלשה פנימה מהצד החשוף: שכבה מתקדמת שבה תאים חיים נעלמו בפתאומיות לטובת תאים מתים. מהירות החזית תלתה בחוזקה באספקת ובצריכת המזון אך הייתה חסינה במידה רבה לכמות האנטיביוטיקה שנוספה לאחר שעברה סף מסוים. יותר סוכר מהיר את החזית; יותר תאים, שאכלו את הסוכר במהירות גדולה יותר, האטו אותה. התנהגות דומה הופיעה עם מספר מזונות ואנטיביוטיקה נוספים, מה שמרמז על עיקרון כללי ולא רק תכונה של תרופה אחת.
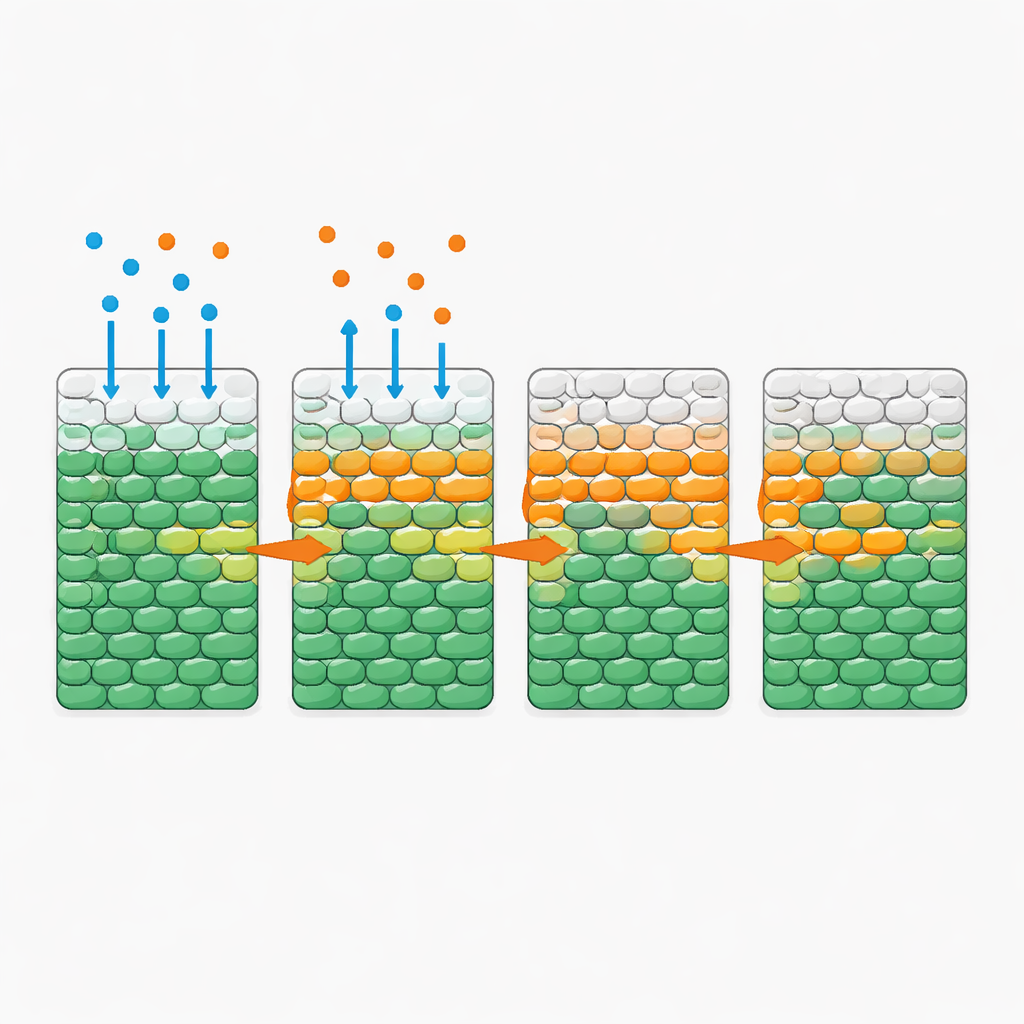
חוקים פשוטים מאחורי דפוס מורכב
כדי להבין את הדינמיקה הזאת כמותית, המחברים בנו מודל מתמטי שעוקב אחרי שלושה מרכיבים: חיידקים, מזון ואנטיביוטיקה. במודל המזון והאנטיביוטיקה מדיפוזים דרך האוכלוסייה; התאים צורכים מזון כדי לגדול; וכאשר הם נחשפים לכמות מספקת של אנטיביוטיקה ומזון לאורך זמן מספיק, הם ראשית מתרבים ואז מתים. כל הפרמטרים נמדדו באופן עצמאי בתרביות מעורבבות היטב, כך שהמודל לא דרש כוונון לניסויים המרחביים. ובכל זאת, הסימולציות שלו שיחזרו את חזיתות המוות הנצפות ואת התלות שלהן ברמת המזון, בצפיפות התאים ובקצב הצריכה. ניתוח המודל חשף כמות חסרת־ממדים מרכזית שמשווה בין הזמן שלוקח לתאים לגדול ולמות בחשיפה לאנטיביוטיקה לבין הזמן שלוקח להם לרוקן את מאגר המזון המקומי. כשהמזון נאכל מהר, התאים הפנימיים נשארים רעבים ולכן מוגנים במידה רבה; כשהצריכה איטית, המזון חודר לעומק והחזית יכולה לעבור דרך כל האוכלוסייה.
כיצד ניצול וצמיחה מחדש מתגלים
אוכלוסיות חיידקיות נדירות אינן אחידות ברגישותן לתרופות, גם כאשר התאים חולקים רקע גנטי זהה. הצוות השתמש בפלטפורמה שלהם כדי לחקור מה קורה כאשר חלק מהתאים עמידים יותר מאחרים. במינוני אנטיביוטיקה בינוניים החזית עדיין נוצרה ונעה פנימה, אך לאחר שעברה נפוצו מאקרו־קולוניות מפוזרות של תאים עמידים יותר שהחלו לצמוח שוב בעקבותיה, ניזונות מהמזון ששוחרר לאזורים הריקים כעת. הורדת מינון האנטיביוטיקה או הגדלת צפיפות התאים ההתחלתית הגבירה את הצמיחה המחודשת. באוכלוסיות ממוסגרות, כיסי עמידות רבים כאלה יכולים להתקיים זה לצד זה, בניגוד לתרביות מעורבבות שבהן בדרך כלל דומינטור יחיד גובר. דפוס זה יכול להעניק לזיהומים הזדמנויות נוספות לפתח עמידות גבוהה יותר או להתאושש לאחר טיפול.
ממה זה נובע לטיפול בזיהומים
המחקר מראה כי זמינות המזון אינה רק פרט שולי אלא צוואר בקבוק מרכזי שיכול לאפשר או להגביל את השכחת האנטיביוטיקה באוכלוסיות חיידקיות ממוסגרות. במקום לשאול רק האם תרופה יכולה להגיע לאתר הזיהום, קלינאים וחוקרים עשויים גם להתבקש לשאול כיצד מקורות המזון זורמים דרך הקהילה וכמה מהר התאים צורכים אותם. המתווה של המחקר, כולל המדד הפשוט שלו לזמן שבו צריכת המזון מהירה יותר מהרציחה, מציע דרך לחזות מתי טיפול אנטיביוטי צפוי להיתקע בקליפה המגוננת. הוא גם מציע ששילוב אנטיביוטיקה עם אסטרטגיות שמשנות את חדירת המזון או מפרקות את המבנה המרחבי יכול להפוך תרופות קיימות ליעילות יותר, ומדגיש מדוע זיהומים צפופים בסגנון ביופילם יכולים להיות עקשניים אף על פי שמבחני מעבדה מצביעים על כך שהתרופה אמורה לעבוד.
ציטוט: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
מילות מפתח: עמידות לאנטיביוטיקה, ביופילמים חיידקיים, גרדיאנטים של מזון, פוספומיצין, דינמיקה של אוכלוסיות מיקרוביאליות