Clear Sky Science · ja
構造化した細菌集団における栄養素のボトルネックが抗生物質の有効性を制御する
感染への影響がなぜ重要か
抗生物質はしばしば均一に混ざった試験管内で評価されますが、実際の多くの感染は組織や医療機器に付着した密な細菌コミュニティを伴います。こうした過密な環境では、栄養や薬剤が外側から染み込み、実験室の試験ではめったに再現できない鋭い化学勾配が生じます。本研究は単純だが強力な問いを投げかけます:栄養素がこうした構造化された細菌集団を通じて移動する仕方が、抗生物質の効き方を制御し、細菌の集団の一部が生き延びて回復するのを助けることがあり得るか?
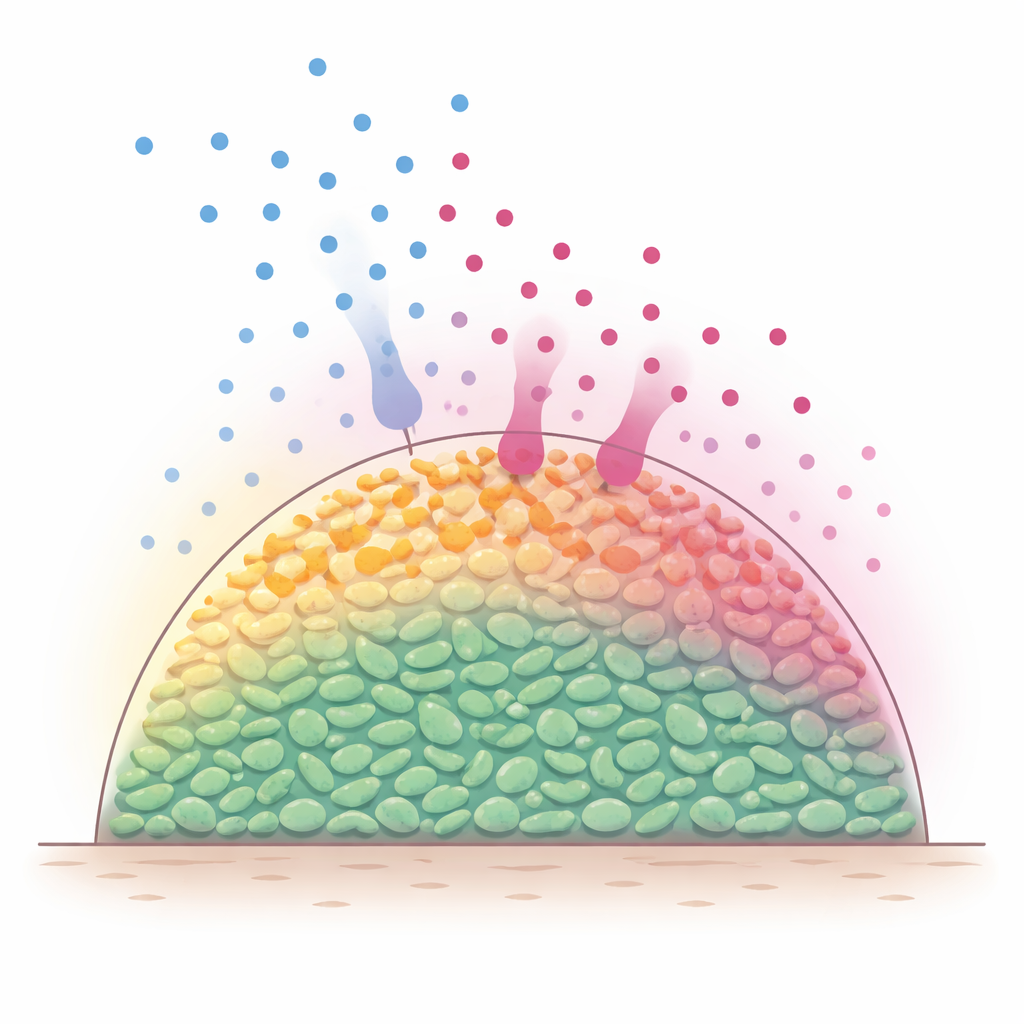
細菌コミュニティの内部に潜む層
自然環境では、細菌はしばしばバイオフィルムと呼ばれる多細胞の集合体として三次元的に詰まって生活します。糖などの栄養分子は外側から拡散して入り、最外層の細胞によって素早く消費されます。その結果、表面の層は代謝的に活発なままですが、より深い細胞は飢餓状態になり活動が鈍くなります。多くの抗生物質は増殖中の細菌に対して最も効果的であるため、こうした内在的な栄養勾配が殺しにくい保護された内部を生むと長く疑われてきました。しかし、栄養と抗生物質が時間をかけて移動・反応する中で、密な集団の内部で実際に何が起きているかを直接観察することは難しかったのです。
制御可能なミニ・バイオフィルムの構築
この課題に取り組むため、研究者らは大腸菌(E. coli)を透明なハイドロゲルマトリクスの中に閉じ込めました。ハイドロゲルは柔らかい水含有材料で、その孔が細胞を位置にとどめつつ小さな分子の拡散は許します。ゲルブロックの一方の面には細菌が入っているが栄養や薬剤はない領域を、反対側にはブドウ糖、抗生物質(ホスホマイシン)、あるいはその両方を入れたリザーバーを置きました。両半分の間の仕切りを取り除くことで、分子がゆっくり拡散するのを許し、蛍光顕微鏡で生細胞と死細胞を区別しながら観察できます。このセットアップは、片側が外界で反対側が保護された内部というバイオフィルムの断面を模倣しつつ、自然試料よりはるかに厳密に実験条件を制御できます。
栄養が致死作用のスイッチを入れるとき
驚くべきことに、抗生物質だけが細菌領域に拡散した場合、標準的な阻害濃度を大きく上回る投与量でも、ほとんどの細胞は1日間までは生存しました。状況が劇的に変わったのは、抗生物質とともに適度な量のブドウ糖が加えられたときでした。その場合、露出側から内側へ向けて驚くほど鋭い「死の前線」が進行するのが観察されました:生細胞が突然死細胞に置き換わる進行性の層です。この前線の速度は栄養供給と消費に強く依存しましたが、ある閾値を超えた抗生物質量の増加にはほとんど感度を示しませんでした。糖が多いほど前線は速く進み、細胞が多いほど集合的に糖を速く消費するため前線は遅くなりました。複数の他の栄養素や抗生物質でも同様の挙動が見られ、この現象が単一薬剤の特殊性ではなく一般的な原理を示唆することが示されました。
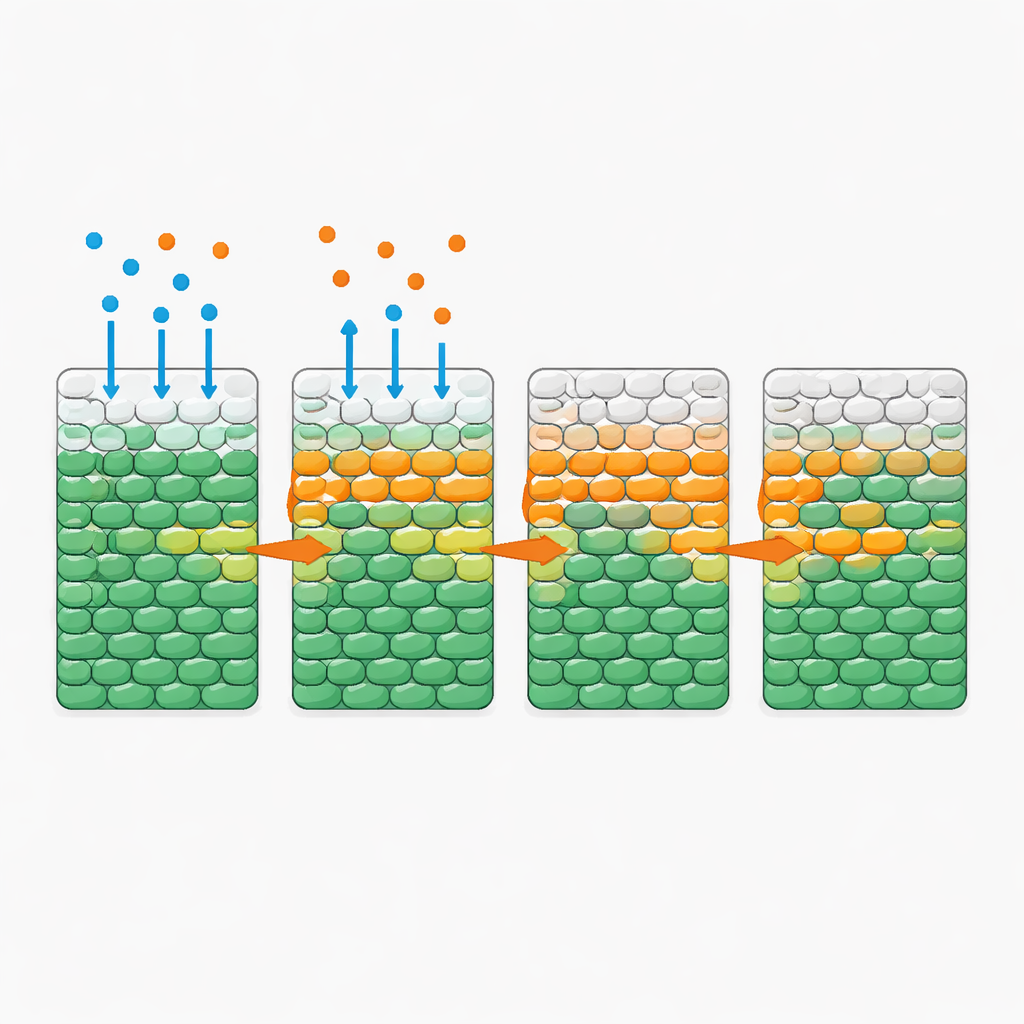
複雑なパターンの背後にある単純な規則
これらのダイナミクスを定量的に理解するため、著者らは細菌、栄養、抗生物質の三成分を追う数理モデルを構築しました。モデルでは、栄養と抗生物質が集団中に拡散し、細胞は成長のために栄養を消費し、十分な抗生物質と栄養に長時間さらされると増殖の後に死に至る、という挙動を取り込みます。すべてのパラメータは均一混合培養で独立に測定されており、空間実験のために調整は不要でした。それでもシミュレーションは観察された死の前線と、その栄養レベル、細胞密度、消費速度への依存性を再現しました。モデル解析は、抗生物質暴露下で細胞が成長・死に至るまでの時間と局所的な栄養供給を枯渇させる時間を比較する重要な無次元量を明らかにしました。栄養が速く枯渇すると内側の細胞は飢餓状態のままで大部分が保護され、消費が遅いと栄養は深く浸透して前線は集団全体を駆け抜け得るのです。
生存と再成長はどのように生まれるか
細菌集団は、同一の遺伝的背景であっても薬剤感受性が均一であることはめったにありません。研究チームは自分たちのプラットフォームを使って、一部の細胞が他より抵抗性を持つ場合に何が起きるかを調べました。中等度の抗生物質濃度では、死の前線は依然として形成され内側へ進みましたが、前線が通過した後に散在するより耐性のある小さなマイクロコロニーがその跡で再成長を始め、より空いた領域に放出された栄養を利用しました。抗生物質量を下げるか初期の細胞密度を上げるとこの再成長は増幅されました。構造化された集団では、多くのそのような耐性ポケットが並存し得るのに対し、均一混合培養では通常一つの勝者が支配することが多いという対比が生まれます。このパターンは、感染がより高い耐性を進化させる機会や治療後に反発する可能性を増やすかもしれません。
感染治療への含意
この研究は、栄養の利用可能性が単なる背景情報ではなく、構造化した細菌集団での抗生物質殺菌を可能にしたり制限したりする中心的なボトルネックであることを示しています。薬が感染部位に到達できるかどうかを問うだけでなく、栄養源がコミュニティをどのように流れるか、細胞がそれをどれだけ速く消費するかを問うことが臨床家や研究者にとって重要になり得ます。栄養消費が殺菌を上回るときの単純な指標を含む本研究の枠組みは、抗生物質治療が保護的な殻で停滞する状況を予測する方法を提供します。さらに、栄養浸透を変えたり空間構造を乱したりする戦略と抗生物質を組み合わせることで既存の薬剤をより効果的にできることを示唆しており、ラボ試験で薬が効くとされても密なバイオフィルム様感染が頑強になり得る理由を明らかにしています。
引用: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
キーワード: 抗生物質耐性, 細菌バイオフィルム, 栄養勾配, ホスホマイシン, 微生物集団動態