Clear Sky Science · fr
Un goulot d’étranglement nutritionnel contrôle l’efficacité des antibiotiques dans des populations bactériennes structurées
Pourquoi c’est important pour les infections
Les antibiotiques sont souvent testés dans des éprouvettes homogènes, alors que de nombreuses infections réelles impliquent des communautés bactériennes denses qui adhèrent aux tissus ou aux dispositifs médicaux. Dans ces environnements encombrés, les nutriments et les médicaments pénètrent depuis l’extérieur, générant des gradients chimiques prononcés que les tests de laboratoire saisissent rarement. Cette étude pose une question simple mais fondamentale : la manière dont les nutriments circulent à travers ces populations bactériennes structurées peut-elle contrôler l’efficacité des antibiotiques — et même permettre à des poches de bactéries de survivre et de repousser ?
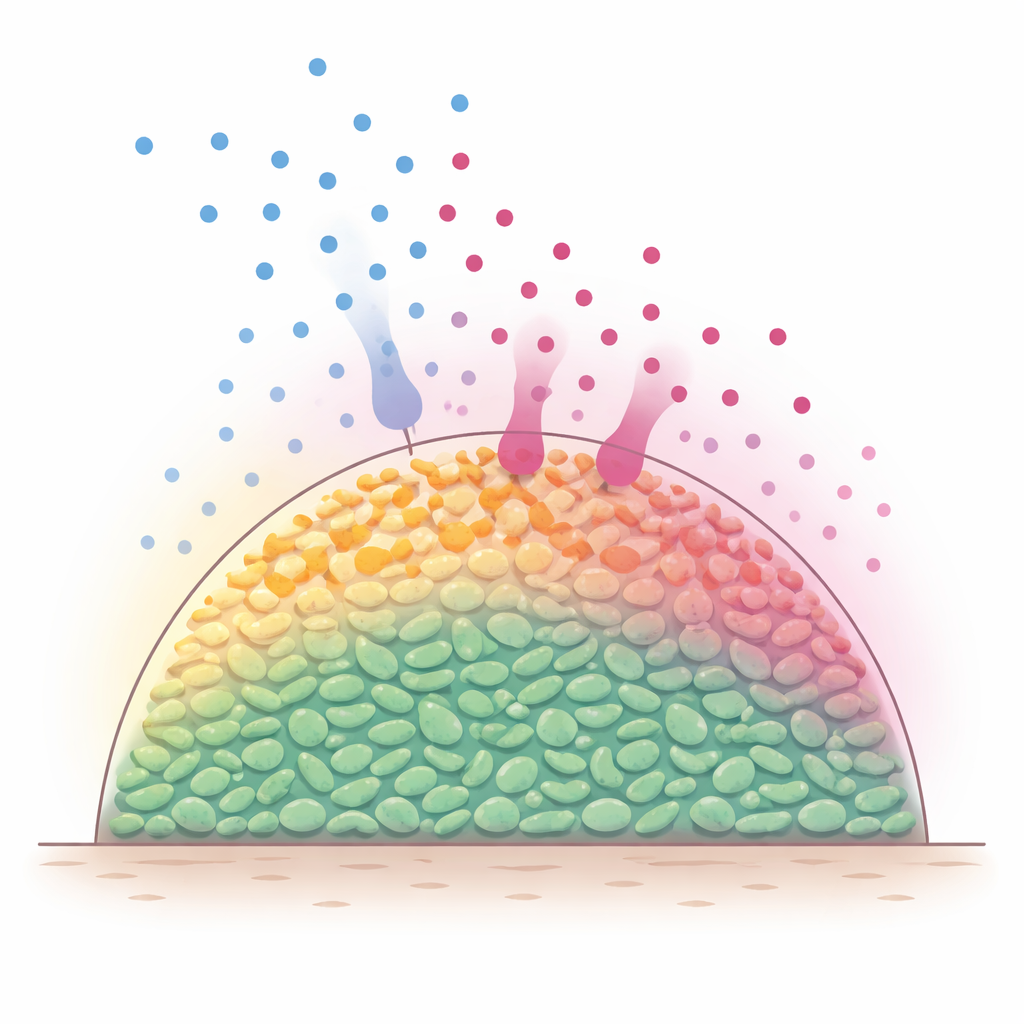
Couches cachées à l’intérieur des communautés bactériennes
Dans la nature, les bactéries vivent fréquemment en assemblages multicellulaires, parfois appelés biofilms, où les cellules se tassent en trois dimensions. Les molécules nutritives, comme les sucres, diffusent depuis l’extérieur et sont rapidement consommées par les cellules les plus externes. En conséquence, les couches superficielles restent métaboliquement actives, tandis que les cellules plus profondes deviennent affamées et ralenties. Comme de nombreux antibiotiques sont plus efficaces contre des bactéries en croissance active, les scientifiques ont longtemps supposé que ces gradients nutritifs intrinsèques créent un intérieur protégé, plus difficile à tuer. Cependant, il a été difficile d’observer directement ce qui se passe à l’intérieur de ces populations denses au fur et à mesure que nutriments et antibiotiques se déplacent et réagissent dans le temps.
Construire un mini-biofilm contrôlable
Pour relever ce défi, les chercheurs ont piégé des bactéries E. coli dans des matrices d’hydrogel transparentes — des matériaux mous remplis d’eau dont les pores maintiennent les cellules en place tout en laissant diffuser les petites molécules. Un côté de chaque bloc de gel contenait des bactéries mais pas de nutriments ni de médicament ; l’autre côté possédait un réservoir de sucre (glucose), d’antibiotique (fosfomycine), ou des deux. En retirant une séparation entre les deux moitiés, l’équipe a laissé les molécules diffuser lentement tout en utilisant la microscopie à fluorescence pour distinguer les cellules vivantes des cellules mortes. Ce dispositif imite une coupe transversale de biofilm, avec le monde extérieur d’un côté et l’intérieur protégé de l’autre, mais offre un contrôle expérimental beaucoup plus strict que les échantillons naturels.
Quand la nourriture déclenche l’action létale
De façon surprenante, lorsque seul l’antibiotique a diffusé dans la zone bactérienne — même à des doses bien supérieures aux niveaux inhibiteurs standards —, la plupart des cellules sont restées vivantes pendant une journée entière. Le tableau a changé radicalement lorsqu’une quantité modeste de glucose a été ajoutée avec l’antibiotique. Dans ce cas, l’équipe a observé un « front de mort » remarquablement net avançant vers l’intérieur depuis le côté exposé : une couche progressant où les cellules vivantes cédaient brusquement la place à des cellules mortes. La vitesse de ce front dépendait fortement de l’apport et de la consommation de nutriments mais était largement insensible à l’ajout d’antibiotique au-delà d’un certain seuil. Plus de sucre accélérera le front ; plus de cellules, qui consomment collectivement le sucre plus rapidement, le ralentissent. Un comportement similaire est apparu avec plusieurs autres nutriments et antibiotiques, ce qui suggère un principe général plutôt qu’une particularité d’un seul médicament.
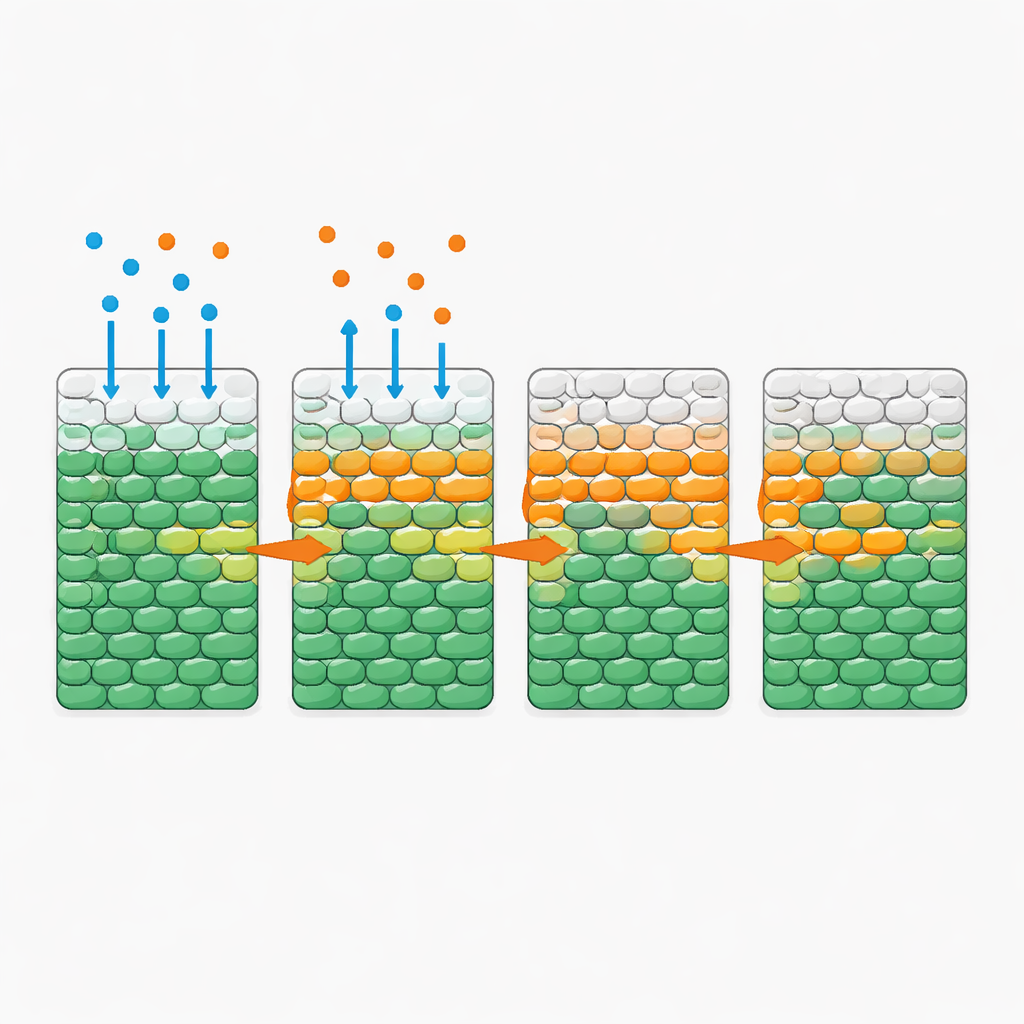
Règles simples derrière un motif complexe
Pour comprendre ces dynamiques quantitativement, les auteurs ont construit un modèle mathématique qui suit trois ingrédients : bactéries, nutriment et antibiotique. Dans le modèle, le nutriment et l’antibiotique diffusent à travers la population ; les cellules consomment le nutriment pour croître ; et une fois exposées à suffisamment d’antibiotique et de nutriment pendant un temps suffisant, elles se multiplient d’abord puis meurent. Tous les paramètres ont été mesurés indépendamment dans des cultures bien mélangées, de sorte que le modèle n’a nécessité aucun réglage pour les expériences spatiales. Pourtant, ses simulations ont reproduit les fronts de mort observés et leur dépendance au niveau de nutriment, à la densité cellulaire et au taux de consommation. L’analyse du modèle a révélé une quantité sans dimension clé qui compare le temps nécessaire aux cellules pour croître et mourir sous exposition antibiotique au temps qu’il leur faut pour épuiser leur approvisionnement local en nutriment. Lorsque le nutriment est rapidement épuisé, les cellules internes restent affamées et donc en grande partie protégées ; lorsque la consommation est lente, le nutriment pénètre profondément et le front peut balayer l’ensemble de la population.
Comment survie et repousse émergent
Les populations bactériennes sont rarement uniformes dans leur sensibilité aux médicaments, même lorsque les cellules partagent le même bagage génétique. L’équipe a utilisé leur plateforme pour explorer ce qui se passe lorsque certaines cellules sont plus résistantes que d’autres. À des doses intermédiaires d’antibiotique, le front de mort s’est formé et a continué d’avancer vers l’intérieur, mais après son passage, des microcolonies éparses de cellules plus résistantes ont commencé à repousser dans son sillage, se nourrissant des nutriments libérés dans des régions désormais plus vides. Diminuer la dose d’antibiotique ou augmenter la densité initiale des cellules amplifiait cette repousse. Dans les populations structurées, beaucoup de ces poches résistantes peuvent persister côte à côte, contrairement aux cultures bien mélangées où typiquement un seul gagnant domine. Ce schéma pourrait offrir aux infections plus d’occasions d’évoluer vers une résistance accrue ou de rebondir après le traitement.
Ce que cela signifie pour le traitement des infections
Ce travail montre que la disponibilité des nutriments n’est pas seulement un détail de fond mais un goulot d’étranglement central qui peut soit permettre soit limiter l’action des antibiotiques dans des populations bactériennes structurées. Plutôt que de se contenter de demander si un médicament peut atteindre un site infectieux, cliniciens et chercheurs devront peut‑être aussi s’interroger sur la façon dont les sources alimentaires traversent la communauté et sur la vitesse à laquelle les cellules les consomment. Le cadre proposé par l’étude, y compris sa métrique simple pour savoir quand la consommation de nutriment dépasse la mortalité, offre un moyen de prédire quand un traitement antibiotique risque de s’arrêter derrière une coque protectrice. Il suggère aussi que combiner des antibiotiques avec des stratégies modifiant la pénétration des nutriments ou perturbant la structure spatiale pourrait rendre des médicaments existants plus efficaces, et il explique pourquoi les infections denses, de type biofilm, peuvent être si tenaces même lorsque les tests de laboratoire indiquent qu’un médicament devrait fonctionner.
Citation: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Mots-clés: résistance aux antibiotiques, biofilms bactériens, gradients de nutriments, fosfomycine, dynamique des populations microbiennes