Clear Sky Science · pt
Um gargalo nutricional controla a eficácia de antibióticos em populações bacterianas estruturadas
Por que isso importa para infecções
Antibióticos costumam ser testados em tubos de ensaio bem misturados, mas muitas infecções reais envolvem comunidades bacterianas densas aderidas a tecidos ou dispositivos médicos. Nesses ambientes compactos, alimentos e remédios penetram de fora, criando gradientes químicos acentuados que os testes de laboratório raramente reproduzem. Este estudo faz uma pergunta simples, porém poderosa: a forma como os nutrientes fluem por essas populações bacterianas estruturadas pode controlar quão bem os antibióticos funcionam — e até ajudar bolsões de bactérias a sobreviver e se recuperar?
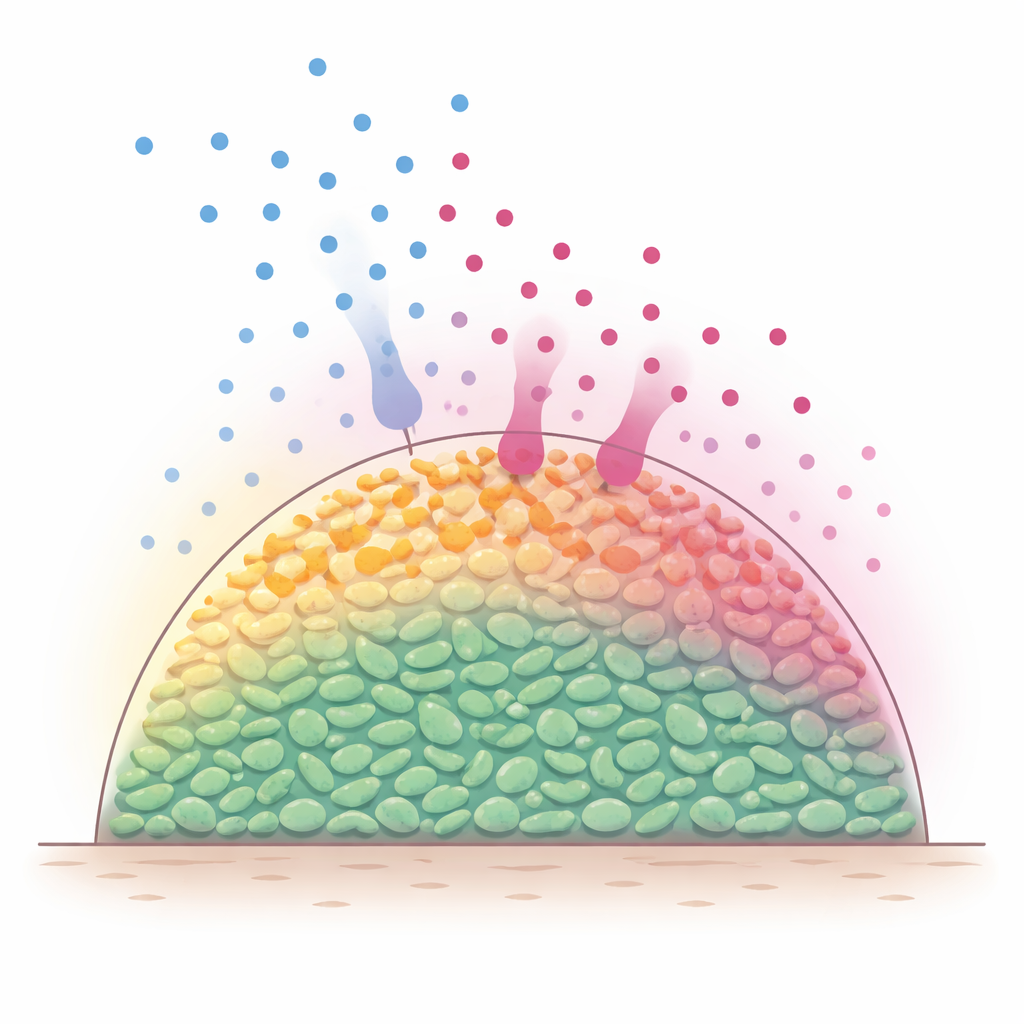
Camadas ocultas dentro de comunidades bacterianas
Em ambientes naturais, bactérias frequentemente vivem em aglomerados multicelulares, às vezes chamados de biofilmes, onde as células se empacotam em três dimensões. Moléculas nutritivas, como açúcares, difundem-se a partir do exterior e são rapidamente consumidas pelas células mais externas. Como resultado, as camadas superficiais permanecem metabolicamente ativas, enquanto células mais profundas ficam famintas e lentas. Como muitos antibióticos são mais eficazes contra bactérias em crescimento ativo, cientistas suspeitam há tempos que esses gradientes nutricionais embutidos criam um interior protegido que é mais difícil de matar. No entanto, tem sido difícil observar diretamente o que acontece dentro de populações tão densas à medida que nutrientes e antibióticos se movem e reagem ao longo do tempo.
Construindo um mini-biofilme controlável
Para enfrentar esse desafio, os pesquisadores aprisionaram bactérias E. coli dentro de matrizes de hidrogel transparentes — materiais macios preenchidos com água cujos poros mantêm as células no lugar, mas ainda permitem que pequenas moléculas difundam-se. Um lado de cada bloco de gel continha bactérias, mas não nutrientes nem drogas; o outro lado continha um reservatório de açúcar (glicose), antibiótico (fosfomicina) ou ambos. Ao remover uma divisória entre as duas metades, a equipe permitiu que as moléculas difundissem lentamente enquanto usava microscopia de fluorescência para distinguir células vivas de mortas. Esse arranjo imita uma seção transversal de um biofilme, com o mundo externo de um lado e o interior protegido do outro, porém com controle experimental muito mais rigoroso do que em amostras naturais.
Quando alimento desbloqueia a ação letal
Surpreendentemente, quando o antibiótico sozinho difundiu-se para a região bacteriana — mesmo em doses muito acima dos níveis inibitórios padrão — a maioria das células permaneceu viva por um dia inteiro. O quadro mudou dramaticamente quando uma quantidade moderada de glicose foi adicionada junto com o antibiótico. Nesse caso, a equipe observou uma “frente de morte” notavelmente nítida varrendo para o interior a partir do lado exposto: uma camada avançando onde células vivas cediam abruptamente às mortas. A velocidade dessa frente dependia fortemente do suprimento e do consumo de nutrientes, mas era em grande parte insensível à quantidade adicional de antibiótico depois que esta excedia um certo limiar. Mais açúcar acelerou a frente; mais células, que coletivamente consumiam o açúcar mais rápido, a retardaram. Comportamento semelhante apareceu com vários outros nutrientes e antibióticos, sugerindo um princípio geral em vez de um pormenor de um único fármaco.
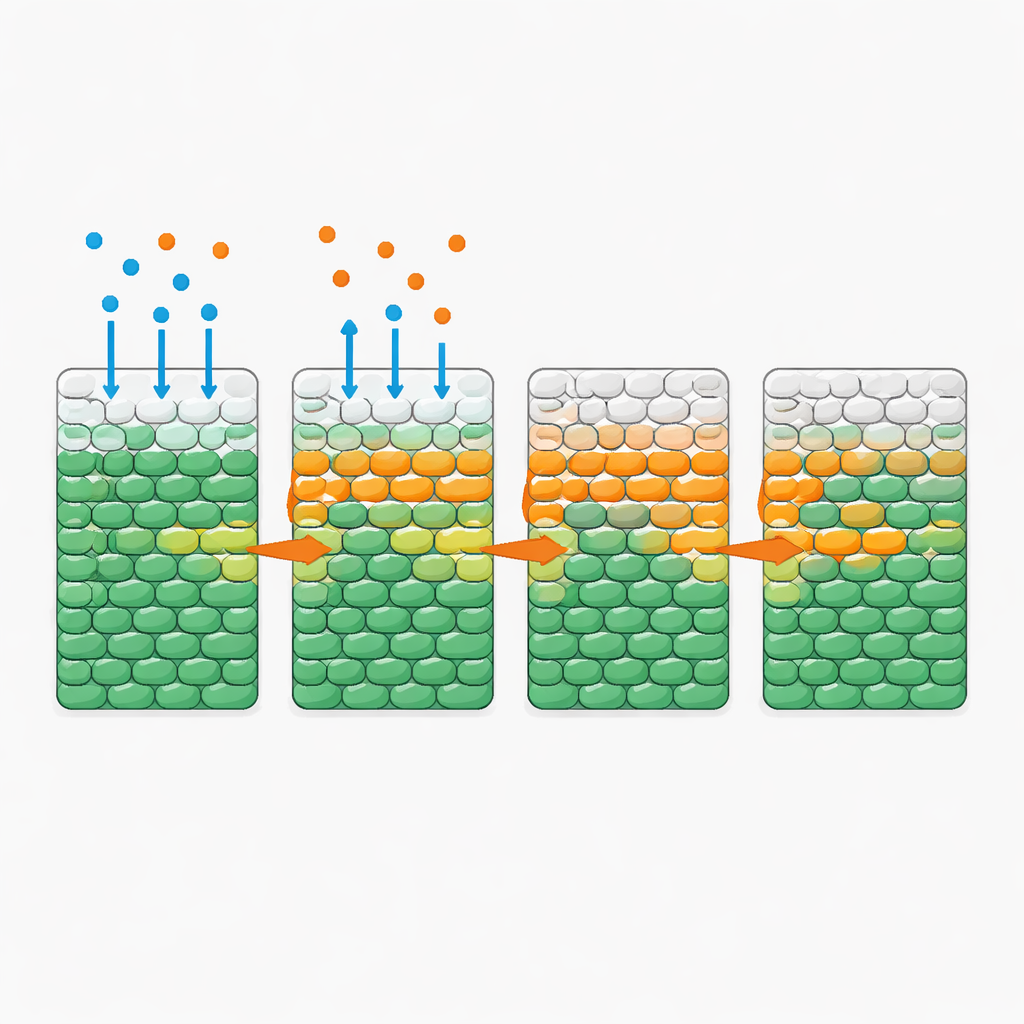
Regras simples por trás de um padrão complexo
Para entender essas dinâmicas quantitativamente, os autores construíram um modelo matemático que acompanha três ingredientes: bactérias, nutriente e antibiótico. No modelo, nutriente e antibiótico difundem-se pela população; as células consomem nutriente para crescer; e, uma vez expostas a antibiótico e nutriente suficientes por tempo suficiente, primeiro multiplicam-se e depois morrem. Todos os parâmetros foram medidos independentemente em culturas bem misturadas, de modo que o modelo não exigiu ajuste para os experimentos espaciais. Ainda assim, suas simulações reproduziram as frentes de morte observadas e sua dependência do nível de nutriente, da densidade celular e da taxa de consumo. A análise do modelo revelou uma quantidade adimensional chave que compara o tempo que as células levam para crescer e morrer sob exposição ao antibiótico com o tempo que levam para esgotar o suprimento local de nutriente. Quando o nutriente é esgotado rapidamente, as células internas permanecem famintas e, portanto, em grande parte protegidas; quando o consumo é lento, o nutriente penetra profundamente e a frente pode varrer toda a população.
Como surgem sobrevivência e recrescimento
Populações bacterianas raramente são uniformes em sua sensibilidade a drogas, mesmo quando as células compartilham o mesmo fundo genético. A equipe usou sua plataforma para explorar o que acontece quando algumas células são mais resistentes do que outras. Em doses intermediárias de antibiótico, a frente de morte ainda se formou e avançou para o interior, mas depois de sua passagem, microcolônias dispersas de células mais resistentes começaram a recrescer em seu rastro, alimentando-se de nutrientes liberados em regiões agora mais vazias. Reduzir a dose de antibiótico ou aumentar a densidade celular inicial amplificou esse recrescimento. Em populações estruturadas, muitos desses bolsões resistentes podem persistir lado a lado, em contraste com culturas bem misturadas onde tipicamente um único vencedor domina. Esse padrão pode dar às infecções mais oportunidades de evoluir maior resistência ou de se recuperar após o tratamento.
O que isso significa para tratar infecções
Este trabalho mostra que a disponibilidade de nutrientes não é apenas um detalhe de fundo, mas um gargalo central que pode permitir ou limitar a ação de antibióticos em populações bacterianas estruturadas. Em vez de simplesmente perguntar se um fármaco pode atingir o local da infecção, clínicos e pesquisadores também podem precisar perguntar como as fontes de alimento fluem pela comunidade e quão rápido as células as consomem. A estrutura do estudo, incluindo sua métrica simples para quando o consumo de nutriente supera a capacidade de matar, oferece uma maneira de prever quando o tratamento com antibiótico provavelmente vai estagnar em uma casca protetora. Também sugere que combinar antibióticos com estratégias que alterem a penetração de nutrientes ou perturbem a estrutura espacial poderia tornar fármacos existentes mais eficazes, e ressalta por que infecções densas, semelhantes a biofilmes, podem ser tão persistentes mesmo quando testes de laboratório indicam que um remédio deveria funcionar.
Citação: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Palavras-chave: resistência a antibióticos, biofilmes bacterianos, gradientes de nutrientes, fosfomicina, dinâmica de populações microbianas