Clear Sky Science · pl
Wąskie gardło związane z dostępnością składników kontroluje skuteczność antybiotyków w uporządkowanych populacjach bakterii
Dlaczego to ma znaczenie dla zakażeń
Antybiotyki najczęściej testuje się w dobrze wymieszanych probówkach, podczas gdy wiele rzeczywistych zakażeń obejmuje gęste społeczności bakteryjne przylegające do tkanek lub urządzeń medycznych. W takich zatłoczonych środowiskach pokarm i leki przenikają od zewnątrz, tworząc ostre gradienty chemiczne, których testy laboratoryjne rzadko oddają. W badaniu zadano proste, ale istotne pytanie: czy sposób przepływu składników odżywczych przez te uporządkowane populacje bakterii może kontrolować skuteczność antybiotyków — a nawet pozwalać kieszeniom bakterii na przetrwanie i odrodzenie?
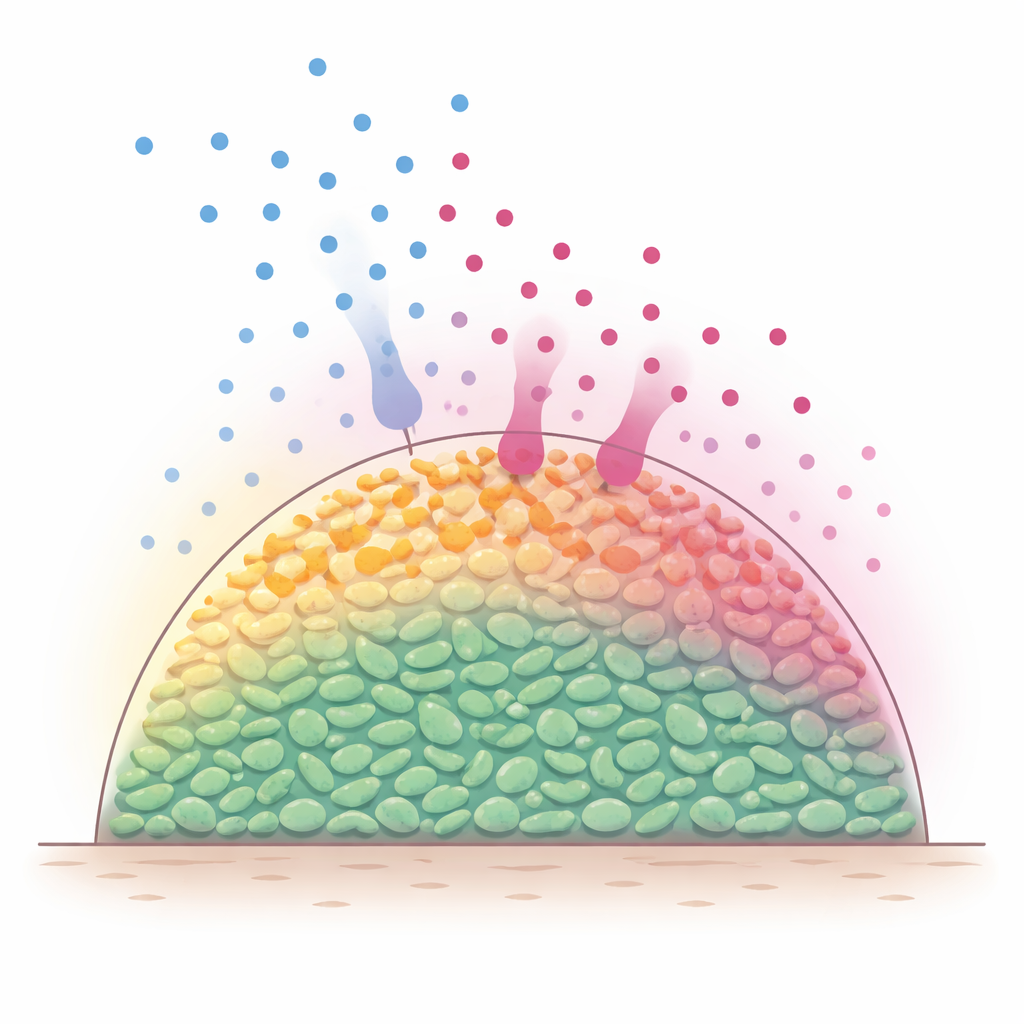
Ukryte warstwy w społecznościach bakteryjnych
W warunkach naturalnych bakterie często żyją w zespołach wielokomórkowych, zwanych czasem biofilmami, gdzie komórki układają się w trzech wymiarach. Cząsteczki składników odżywczych, takie jak cukry, dyfundują od zewnątrz i są szybko wykorzystywane przez zewnętrzne warstwy komórek. W efekcie powierzchniowe warstwy pozostają metabolicznie aktywne, podczas gdy komórki głębiej stają się głodowane i spowolnione. Ponieważ wiele antybiotyków działa najlepiej na aktywnie rosnące bakterie, naukowcy od dawna podejrzewali, że te wbudowane gradienty składników odżywczych tworzą osłonięte wnętrze trudniejsze do zabicia. Jednak obserwowanie bezpośrednio, co dzieje się wewnątrz takich gęstych populacji, gdy składniki odżywcze i antybiotyki przemieszczają się i reagują w czasie, było trudne.
Budowanie kontrolowalnego mini-biofilmu
Aby sprostać temu wyzwaniu, badacze uwięzili bakterie E. coli w przezroczystych matrycach hydrożelowych — miękkich, wypełnionych wodą materiałach, których pory utrzymują komórki na miejscu, ale wciąż pozwalają małym cząsteczkom dyfundować. Jedna strona każdego bloku żelu zawierała bakterie, ale nie miała składników odżywczych ani leków; druga strona miała rezerwuar cukru (glukozy), antybiotyku (fosfomycyny) lub obu. Po usunięciu przegrody między połowami, zespół pozwalał cząsteczkom powoli dyfundować, używając mikroskopii fluorescencyjnej do rozróżnienia żywych i martwych komórek. To ustawienie naśladuje przekrój biofilmu, zewnętrzny świat po jednej stronie i chronione wnętrze po drugiej, ale z dużo precyzyjniejszą kontrolą eksperymentalną niż w próbkach naturalnych.
Kiedy pokarm uruchamia śmiercionośne działanie
Zaskakująco, gdy sam antybiotyk dyfundował do obszaru z bakteriami — nawet w dawkach znacznie przekraczających standardowe poziomy hamujące — większość komórek pozostała przy życiu przez cały dzień. Obraz dramatycznie się zmienił, gdy razem z antybiotykiem dodano umiarkowaną ilość glukozy. Wtedy zespół zaobserwował niezwykle wyraźny „front śmierci” przesuwający się do wnętrza od strony wystawionej na działanie: postępującą warstwę, gdzie żywe komórki nagle ustępowały miejsca martwym. Prędkość tego frontu w dużej mierze zależała od podaży i zużycia składnika odżywczego, ale była stosunkowo niewrażliwa na zwiększanie dawki antybiotyku, gdy przekraczała pewien próg. Więcej cukru przyspieszało front; więcej komórek, które wspólnie konsumowały cukier szybciej, spowalniało go. Podobne zachowanie zaobserwowano dla kilku innych składników odżywczych i antybiotyków, co sugeruje zasadę ogólną, a nie przypadek jednej substancji.
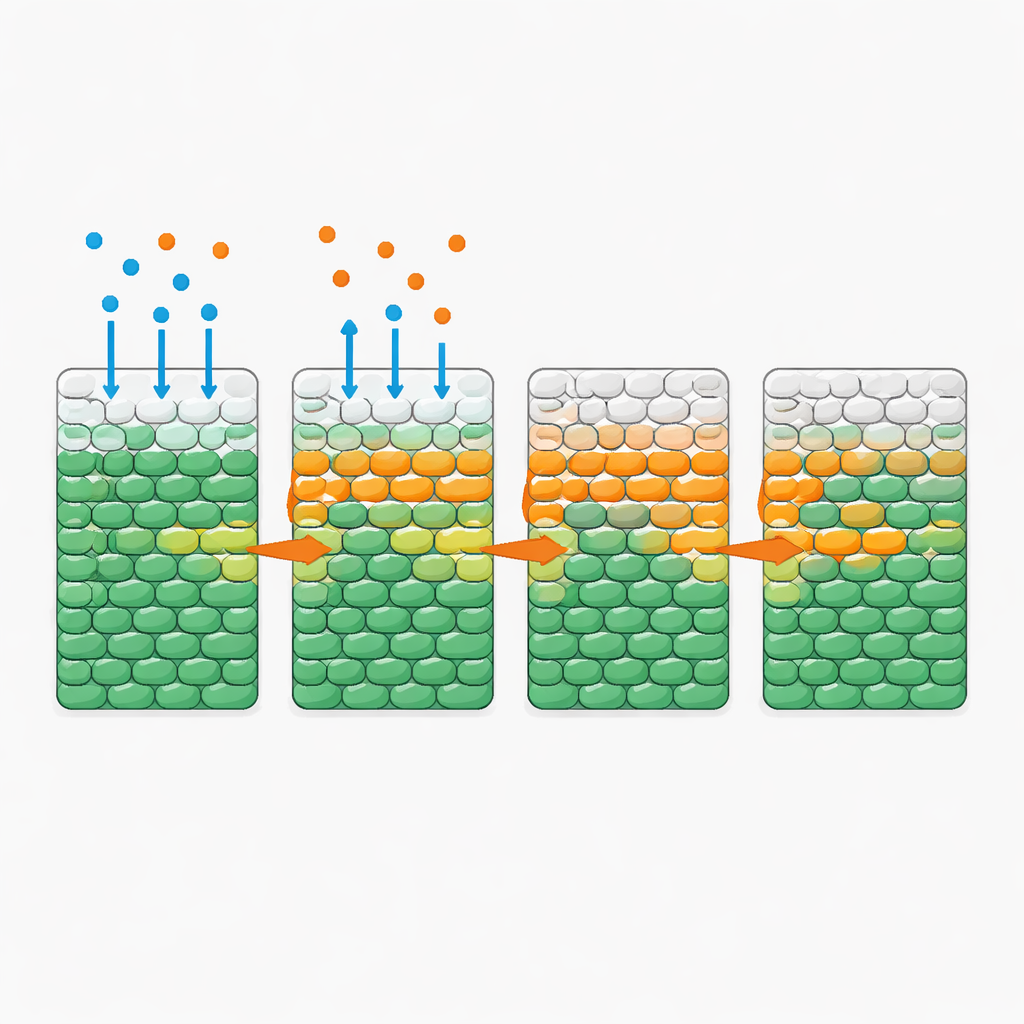
Proste reguły stojące za złożonym wzorem
Aby ilościowo zrozumieć te dynamiki, autorzy zbudowali model matematyczny śledzący trzy składniki: bakterie, składnik odżywczy i antybiotyk. W modelu składnik odżywczy i antybiotyk dyfundują przez populację; komórki zużywają składnik odżywczy, aby rosnąć; a po wystawieniu na działanie wystarczającej ilości antybiotyku i składnika odżywczego przez odpowiedni czas najpierw rozmnażają się, a potem umierają. Wszystkie parametry zmierzono niezależnie w dobrze wymieszanych hodowlach, więc model nie wymagał dopasowywania do eksperymentów przestrzennych. Mimo to symulacje odtworzyły obserwowane fronty śmierci i ich zależność od poziomu składnika odżywczego, gęstości komórek i szybkości konsumpcji. Analiza modelu ujawniła kluczową wielkość bezwymiarową porównującą czas potrzebny komórkom na wzrost i śmierć pod wpływem antybiotyku z czasem potrzebnym na wyczerpanie lokalnych zapasów składnika odżywczego. Gdy składnik zostaje szybko wyczerpany, wewnętrzne komórki pozostają głodzone i tym samym w dużej mierze chronione; gdy konsumpcja jest wolna, składnik penetruje głębiej i front może przetoczyć się przez całą populację.
Jak powstaje przetrwanie i odrost
Populacje bakteryjne rzadko są jednorodne pod względem wrażliwości na leki, nawet gdy komórki mają to samo podłoże genetyczne. Zespół wykorzystał swoją platformę, aby zbadać, co się dzieje, gdy część komórek jest bardziej oporna niż inne. Przy średnich dawkach antybiotyku front śmierci nadal się tworzył i przesuwał do wnętrza, ale po jego przejściu zaczęły w jego śladzie odrastać rozproszone mikrokolonie bardziej odpornych komórek, wykorzystując składniki odżywcze uwolnione do teraz bardziej pustych obszarów. Obniżenie dawki antybiotyku lub zwiększenie początkowej gęstości komórek wzmacniało ten odrost. W uporządkowanych populacjach wiele takich opornych kieszeni może trwać obok siebie, w przeciwieństwie do kultur dobrze wymieszanych, gdzie zazwyczaj dominuje pojedynczy zwycięzca. Ten układ może dać zakażeniom więcej okazji do ewolucji wyższej oporności lub odbicia po leczeniu.
Co to oznacza dla leczenia zakażeń
Wyniki pokazują, że dostępność składników odżywczych nie jest tylko tłem, lecz centralnym wąskim gardłem, które może umożliwiać lub ograniczać zabijanie przez antybiotyki w uporządkowanych populacjach bakterii. Zamiast jedynie pytać, czy lek może dotrzeć do miejsca zakażenia, klinicyści i badacze powinni również rozważyć, jak źródła pokarmu przepływają przez społeczność i jak szybko komórki je konsumują. Ramy zaproponowane w badaniu, w tym prosta miara określająca, kiedy konsumpcja składnika odżywczego wyprzedza zabijanie, oferują sposób przewidywania, kiedy leczenie antybiotykowe prawdopodobnie ugrzęźnie na ochronnej powłoce. Sugeruje to także, że łączenie antybiotyków ze strategiami zmieniającymi penetrację składników odżywczych lub zaburzającymi strukturę przestrzenną mogłoby zwiększyć skuteczność istniejących leków i wyjaśnia, dlaczego gęste, przypominające biofilm zakażenia mogą być tak oporne, nawet gdy testy laboratoryjne wskazują, że lek powinien działać.
Cytowanie: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Słowa kluczowe: oporność na antybiotyki, biofilmy bakteryjne, gradienty składników odżywczych, fosfomycyna, dynamika populacji mikrobiologicznych