Clear Sky Science · tr
Yapılandırılmış bakteri popülasyonlarında bir besin darboğazı antibiyotik etkinliğini kontrol ediyor
Enfeksiyonlar için neden önemli
Antibiyotikler sıklıkla iyi karışmış deney tüplerinde test edilir, oysa birçok gerçek enfeksiyon dokulara veya tıbbi cihazlara tutunan yoğun bakteri topluluklarını içerir. Bu kalabalık ortamlarda besinler ve ilaçlar dışarıdan sızar ve laboratuvarda nadiren yakalanan keskin kimyasal gradyanlar oluşturur. Bu çalışma basit ama güçlü bir soruyu gündeme getiriyor: besinlerin bu yapılandırılmış bakteri popülasyonları boyunca akışı, antibiyotiklerin ne kadar etkili olduğunu kontrol edebilir mi — hatta bakterilerin bazı cepelerini hayatta kalmaya ve yeniden çoğalmaya yardımcı olabilir mi?
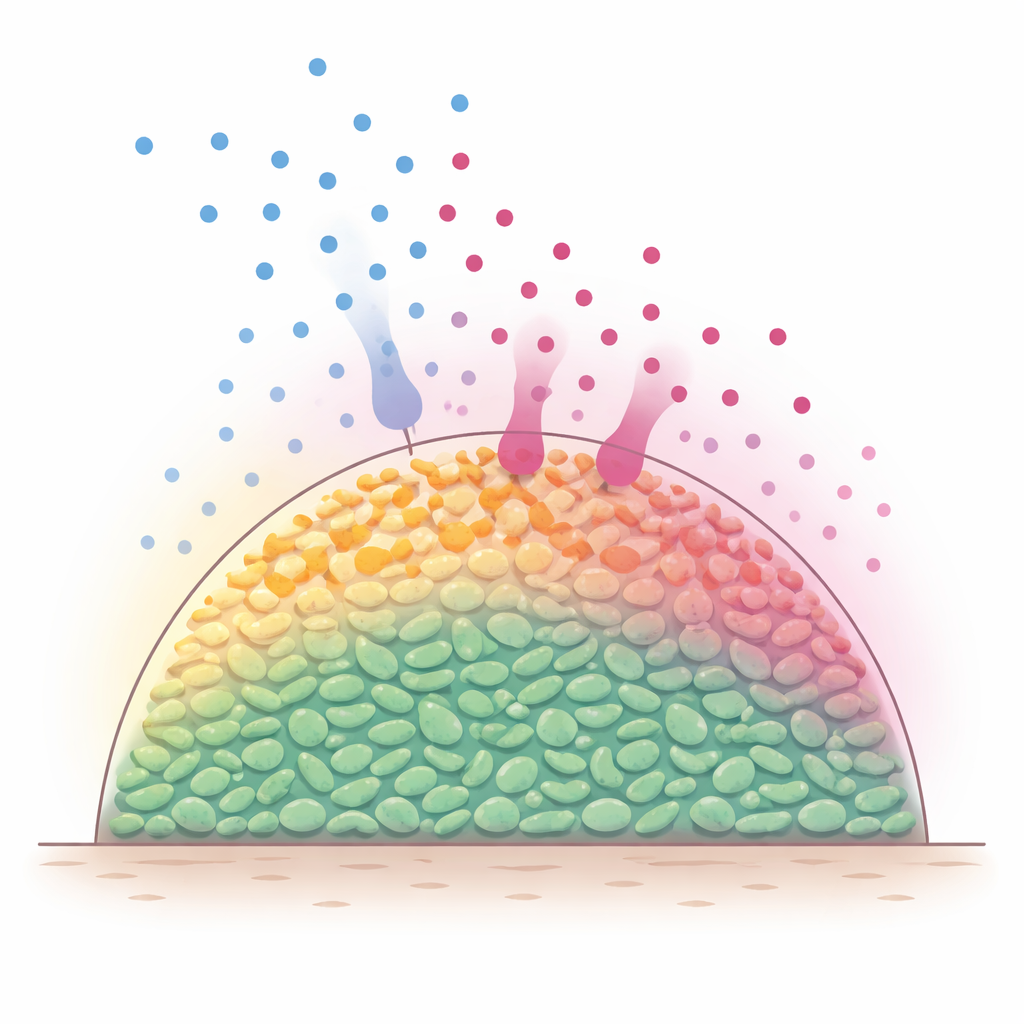
Bakteri topluluklarının içindeki gizli katmanlar
Doğal ortamlarda bakteriler sıklıkla hücrelerin üç boyutta bir araya geldiği çok hücreli düzenlerde, bazen biyofilmler olarak adlandırılan yapılar içinde yaşar. Şeker gibi besin molekülleri dışarıdan difüze olur ve en dıştaki hücreler tarafından hızla tüketilir. Sonuç olarak, yüzey katmanlar metabolik olarak aktif kalırken daha derindeki hücreler aç kalır ve yavaşlar. Pek çok antibiyotiğin en etkili olduğu hedefler aktif olarak büyüyen bakteriler olduğu için bilim insanları uzun süredir bu yerleşik besin gradyanlarının öldürülmesi daha zor korunaklı bir iç bölge yarattığından şüpheleniyordu. Ancak besinler ve antibiyotikler zaman içinde hareket edip reaksiyona girerken bu yoğun popülasyonların içinde doğrudan ne olduğunu gözlemlemek zordu.
Kontrollü bir mini-biyofilm oluşturmak
Bu zorluğun üstesinden gelmek için araştırmacılar E. coli bakterilerini saydam hidrojel matrisleri içine hapsedip çalıştılar — gözenekleri hücreleri yerinde tutan ancak küçük moleküllerin difüze olmasına izin veren yumuşak, su dolu materyaller. Her jel bloğunun bir tarafında bakteri vardı ama besin veya ilaç yoktu; diğer tarafında şeker (glukoz), antibiyotik (fosfomisin) veya her ikisinin rezervuarı bulunuyordu. İki yarıyı ayıran bölmeyi kaldırarak moleküllerin yavaşça difüze olmasına izin verdiler ve canlı hücreleri ölü hücrelerden ayırt etmek için floresan mikroskopi kullandılar. Bu düzenleme bir biyofilmin kesitini taklit eder: bir tarafta dış dünya, diğer tarafta korunmuş iç kısım vardır; ancak doğal örneklerden çok daha sıkı deneysel kontrol sağlar.
Besin öldürücü etkiyi nasıl açığa çıkarır
Şaşırtıcı bir şekilde, antibiyotik tek başına bakteri bölgesine difüze olduğunda — standart inhibe edici düzeylerin çok üstünde dozlarda bile — çoğu hücre bir gün boyunca canlı kaldı. Durum, antibiyotikle birlikte mütevazı miktarda glukoz eklendiğinde dramatik biçimde değişti. Bu durumda ekip, maruz kalan taraftan içeri doğru süzülen olağanüstü keskin bir “ölüm cephesi” gözlemledi: canlı hücrelerin aniden ölü hücrelere dönüştüğü ilerleyen bir katman. Bu cephenin hızı besin arzı ve tüketimine güçlü biçimde bağlıydı, ancak belirli bir eşiği aştıktan sonra eklenen antibiyotik miktarına büyük ölçüde duyarsızdı. Daha fazla şeker cephaneyi hızlandırdı; kolektif olarak şekeri daha hızlı tüketen daha fazla hücre ise yavaşlattı. Benzer davranışlar birkaç farklı besin ve antibiyotikle de görüldü; bu da tek bir ilacın tuhaflığı yerine genel bir ilkeye işaret ediyor.
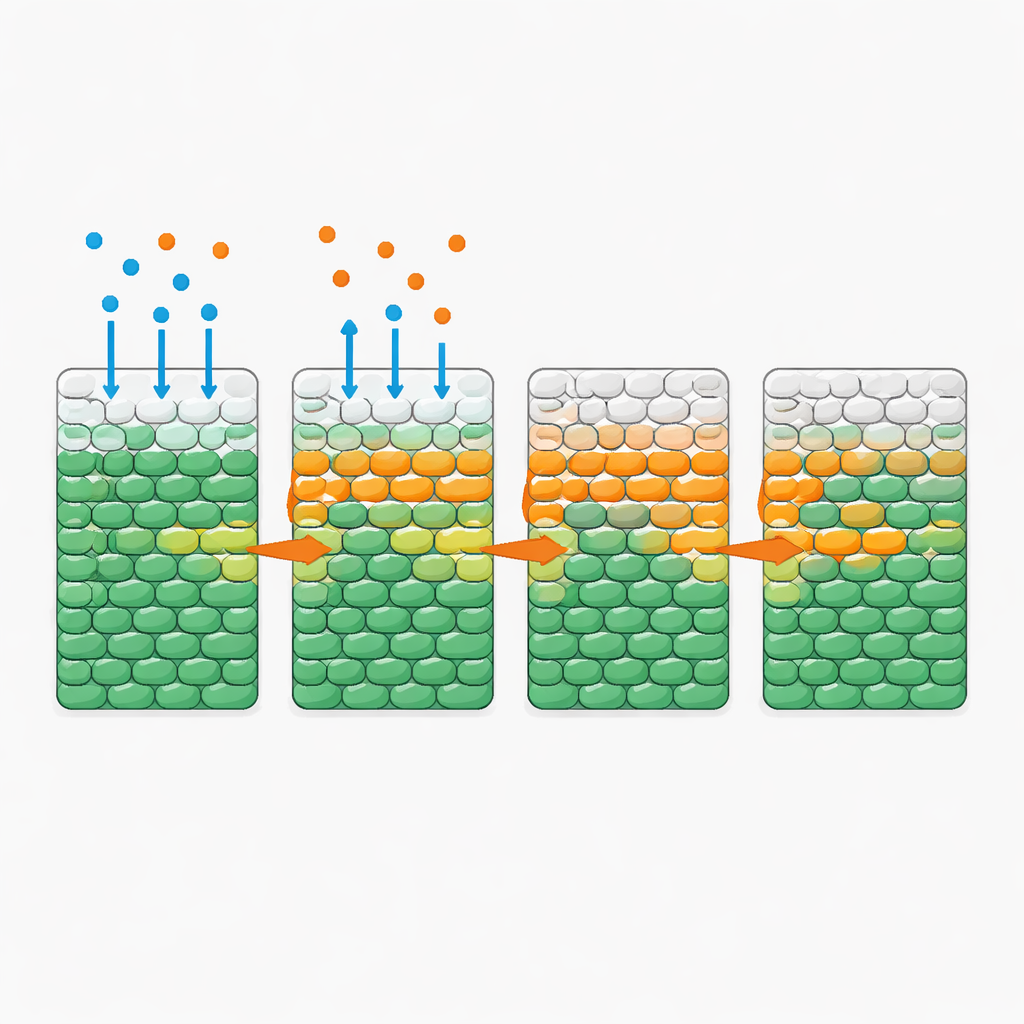
Basit kuralların arkasındaki karmaşık desen
Bu dinamikleri niceliksel olarak anlamak için yazarlar üç bileşeni izleyen bir matematiksel model kurdular: bakteri, besin ve antibiyotik. Modelde besin ve antibiyotik popülasyon boyunca difüze olur; hücreler büyümek için besini tüketir; ve yeterli antibiyotik ve besine yeterince uzun süre maruz kaldıklarında önce çoğalır sonra ölürler. Tüm parametreler iyi karışmış kültürlerde bağımsız olarak ölçüldü, bu yüzden model mekânsal deneyler için ayar gerektirmedi. Buna rağmen simülasyonları gözlemlenen ölüm cephanelerini ve bunların besin düzeyi, hücre yoğunluğu ve tüketim hızına bağlılığını yeniden üretti. Modelin analizi, hücrelerin antibiyotik maruziyeti altında büyüyüp ölme sürelerini yerel besin arzını tüketme süreleriyle karşılaştıran önemli bir boyutsuz niceliği ortaya koydu. Besin hızla tükenirse iç hücreler aç kalır ve bu nedenle büyük ölçüde korunmuş kalır; tüketim yavaşsa besin derinlere nüfuz eder ve cephe tüm popülasyonu süpürebilir.
Hayatta kalma ve yeniden büyümenin nasıl ortaya çıktığı
Bakteri popülasyonları genellikle ilaçlara duyarlılık bakımından tek tip değildir, hücreler aynı genetik arka plana sahip olsa bile. Ekip platformlarını bazı hücreler diğerlerinden daha dirençli olduğunda ne olduğunu keşfetmek için kullandı. Orta düzey antibiyotik dozlarında ölüm cephesi yine oluştu ve içeri doğru hareket etti, ancak geçtiğinde daha dirençli hücrelerin dağınık mikrokolonileri arkasında yeniden büyümeye başladı ve şimdi daha boş olan bölgelerde serbest kalan besinlerle beslendi. Antibiyotik dozunu düşürmek veya başlangıç hücre yoğunluğunu artırmak bu yeniden büyümeyi güçlendirdi. Yapılandırılmış popülasyonlarda birçok böyle dirençli cep yan yana varlığını sürdürebilir; oysa iyi karışmış kültürlerde genellikle tek bir baskın tür kazanır. Bu desen, enfeksiyonlara daha yüksek direnç evrimi veya tedaviden sonra yeniden patlama için daha fazla fırsat sağlayabilir.
Enfeksiyonların tedavisi için ne anlama geliyor
Bu çalışma, besin erişilebilirliğinin sadece arka planda kalan bir ayrıntı olmadığını, yapılandırılmış bakteri popülasyonlarında antibiyotikle öldürmeyi ya mümkün kılan ya da sınırlayan merkezi bir darboğaz olduğunu gösteriyor. Bir ilacın enfeksiyon bölgesine ulaşıp ulaşamayacağını sormanın ötesinde, klinisyenlerin ve araştırmacıların topluluk boyunca besin kaynaklarının nasıl aktığını ve hücrelerin bunları ne kadar hızlı tükettiğini de sorgulamaları gerekebilir. Çalışmanın çerçevesi, besin tüketiminin öldürmeyi ne zaman geride bıraktığını belirten basit bir ölçüt de dahil olmak üzere, antibiyotik tedavisinin koruyucu bir kabukta takılıp kalacağı zamanları öngörmenin bir yolunu sunuyor. Ayrıca antibiyotikleri besin nüfuzunu değiştiren veya mekânsal yapıyı bozan stratejilerle birleştirmenin mevcut ilaçları daha etkili kılabileceğini ve yoğun, biyofilm benzeri enfeksiyonların laboratuvar testleri ilacın işe yarayacağını söylese bile neden bu kadar inatçı olabileceğini açıklıyor.
Atıf: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Anahtar kelimeler: antibiyotik direnci, bakteriyel biyofilmler, besin gradyanları, fosfomisin, mikrobiyal popülasyon dinamikleri