Clear Sky Science · it
Un collo di bottiglia nutrizionale controlla l’efficacia degli antibiotici in popolazioni batteriche strutturate
Perché questo è importante per le infezioni
Gli antibiotici sono spesso testati in provette ben miscelate, ma molte infezioni reali coinvolgono comunità batteriche dense che aderiscono a tessuti o dispositivi medici. In questi ambienti affollati, cibo e farmaci filtrano dall’esterno, creando forti gradienti chimici che i test di laboratorio raramente riproducono. Questo studio pone una domanda semplice ma potente: il modo in cui i nutrienti scorrono attraverso queste popolazioni batteriche strutturate può controllare quanto bene funzionano gli antibiotici — e persino aiutare nicchie di batteri a sopravvivere e riprendersi?
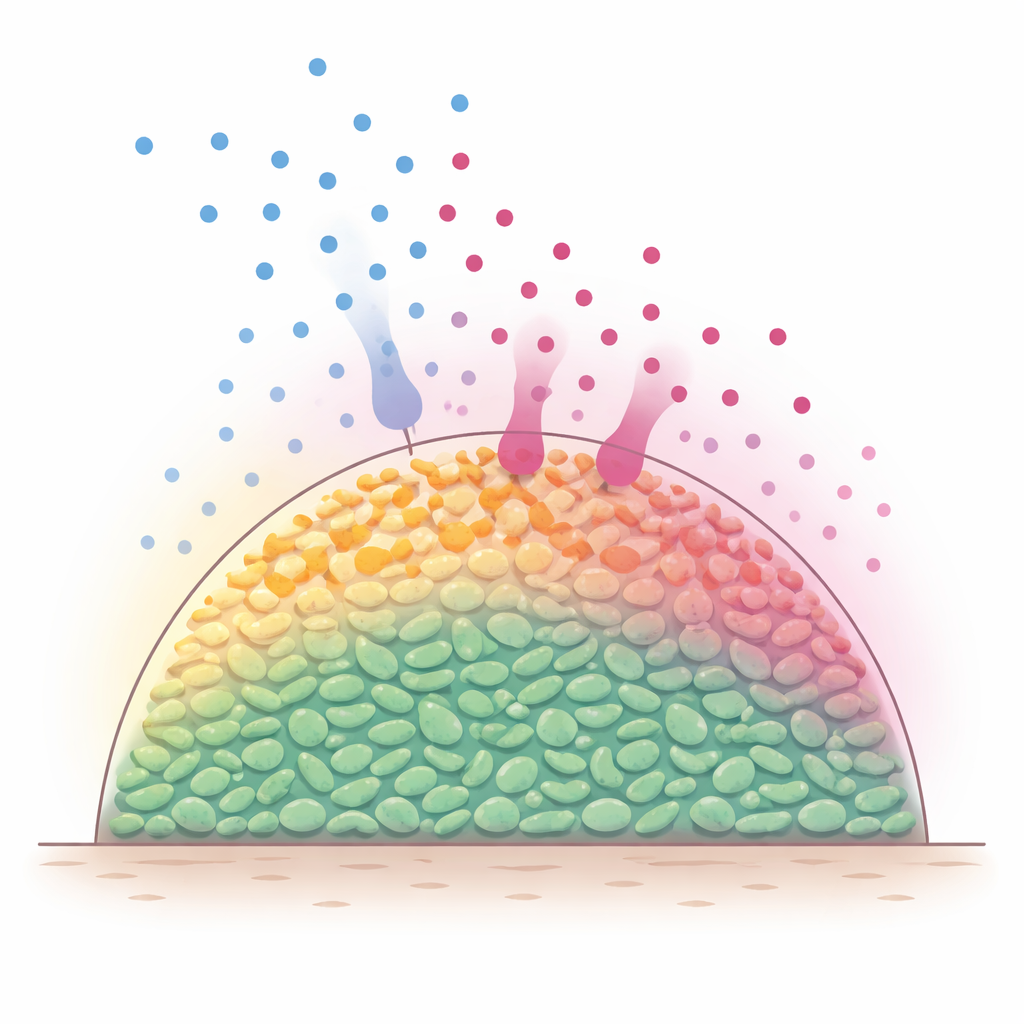
Strati nascosti all’interno delle comunità batteriche
In ambienti naturali i batteri vivono spesso in aggregati multicellulari, talvolta chiamati biofilm, dove le cellule sono impaccate in tre dimensioni. Le molecole nutritive, come gli zuccheri, diffondono dall’esterno e vengono rapidamente consumate dalle cellule più esterne. Perciò gli strati superficiali restano metabolicamente attivi, mentre le cellule più profonde diventano affamate e lente. Poiché molti antibiotici sono più efficaci contro batteri in crescita attiva, gli scienziati hanno a lungo sospettato che questi gradienti nutritivi interni creino un interno schermato più difficile da uccidere. Tuttavia, è stato difficile osservare direttamente cosa accade all’interno di tali popolazioni dense mentre nutrienti e antibiotici si muovono e reagiscono nel tempo.
Costruire un mini-biofilm controllabile
Per affrontare questa sfida, i ricercatori intrappolarono batteri E. coli all’interno di matrici idrogel trasparenti — materiali morbidi pieni d’acqua i cui pori mantengono le cellule in posizione ma permettono comunque la diffusione di piccole molecole. Un lato di ogni blocco di gel conteneva batteri ma nessun nutriente o farmaco; l’altro lato ospitava un serbatoio di zucchero (glucosio), antibiotico (fosfomicina), o entrambi. Rimuovendo un divisorio tra le due metà, il team lasciava le molecole diffondere lentamente mentre usava la microscopia a fluorescenza per distinguere cellule vive da cellule morte. Questo allestimento imita una sezione trasversale di un biofilm, con il mondo esterno da un lato e l’interno protetto dall’altro, ma con un controllo sperimentale molto più stretto rispetto ai campioni naturali.
Quando il cibo sblocca l’azione letale
Sorprendentemente, quando l’antibiotico da solo diffuse nella regione batterica — anche a dosi ben oltre i livelli inibitori standard — la maggior parte delle cellule rimase viva per un intero giorno. Il quadro cambiò drasticamente quando una modesta quantità di glucosio fu aggiunta insieme all’antibiotico. In quel caso il team osservò un «fronte di morte» straordinariamente netto che avanzava verso l’interno dalla parte esposta: uno strato avanzante in cui le cellule vive cedevano bruscamente il posto a cellule morte. La velocità di questo fronte dipendeva fortemente dalla fornitura e dal consumo di nutrienti ma era in gran parte insensibile alla quantità di antibiotico aggiunta una volta superata una certa soglia. Più zucchero accelerava il fronte; più cellule, che collettivamente consumavano lo zucchero più rapidamente, lo rallentavano. Un comportamento simile si osservò con altri nutrienti e antibiotici, suggerendo un principio generale piuttosto che una singolarità di un solo farmaco.
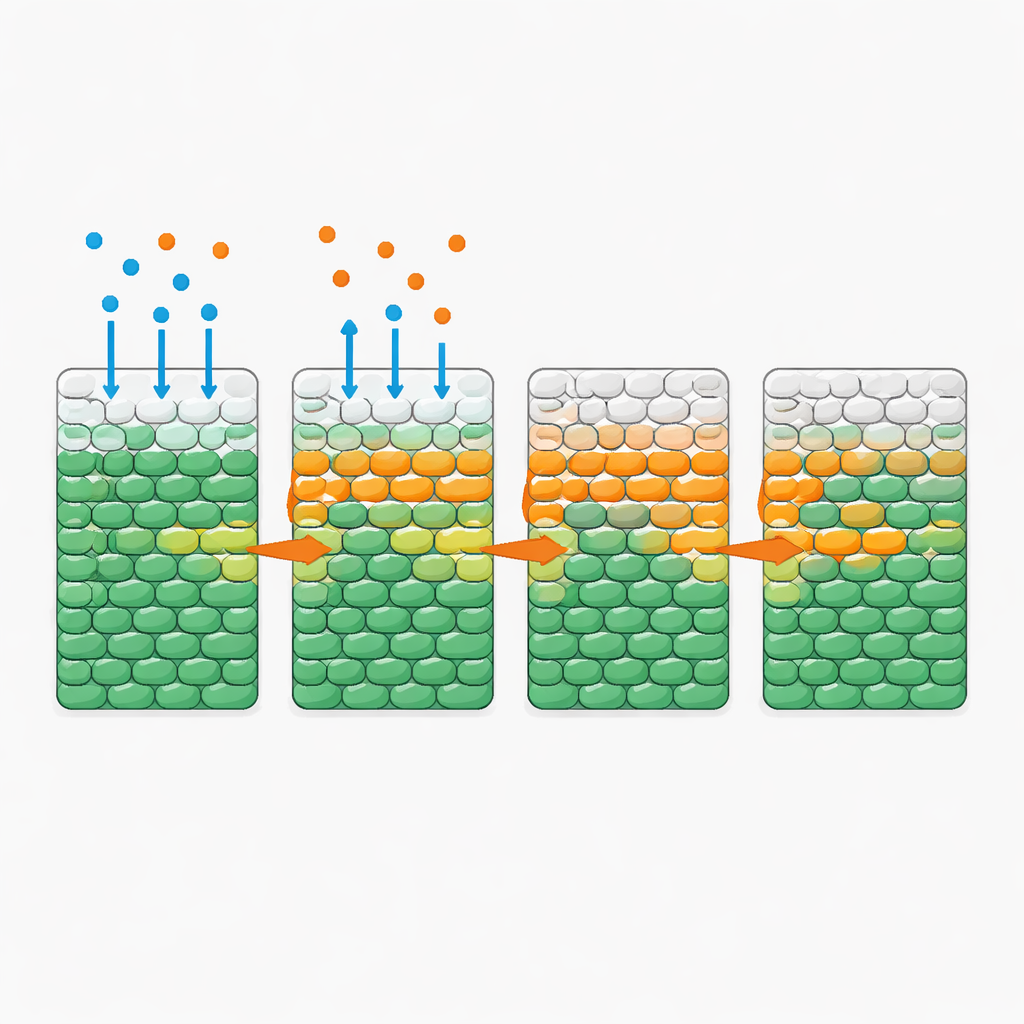
Regole semplici dietro un pattern complesso
Per comprendere quantitativamente queste dinamiche, gli autori costruirono un modello matematico che tiene traccia di tre componenti: batteri, nutriente e antibiotico. Nel modello, nutriente e antibiotico diffondono attraverso la popolazione; le cellule consumano il nutriente per crescere; e una volta esposte a sufficiente antibiotico e nutriente per un tempo adeguato, prima si moltiplicano e poi muoiono. Tutti i parametri furono misurati indipendentemente in colture ben miscelate, quindi il modello non richiese calibrazione per gli esperimenti spaziali. Eppure le sue simulazioni riprodussero i fronti di morte osservati e la loro dipendenza dal livello di nutrienti, dalla densità cellulare e dal tasso di consumo. L’analisi del modello rivelò una quantità adimensionale chiave che confronta il tempo necessario alle cellule per crescere e morire sotto esposizione antibiotica con il tempo necessario a esaurire la riserva locale di nutrienti. Quando il nutriente viene esaurito rapidamente, le cellule interne restano affamate e quindi in gran parte protette; quando il consumo è lento, il nutriente penetra in profondità e il fronte può attraversare l’intera popolazione.
Come emergono sopravvivenza e ricrescita
Le popolazioni batteriche raramente sono uniformi nella loro sensibilità ai farmaci, anche quando le cellule condividono lo stesso background genetico. Il team usò la sua piattaforma per esplorare cosa succede quando alcune cellule sono più resistenti di altre. A dosi antibiotiche intermedie, il fronte di morte si formava ancora e si muoveva verso l’interno, ma dopo il suo passaggio iniziarono a ricrescere, sparse, microcolonie di cellule più resistenti, nutrendosi dei nutrienti rilasciati in regioni ora più vuote. Ridurre la dose di antibiotico o aumentare la densità cellulare iniziale amplificava questa ricrescita. Nelle popolazioni strutturate, molte di queste nicchie resistenti possono persistere fianco a fianco, diversamente dalle colture ben miscelate dove tipicamente domina un unico vincitore. Questo pattern potrebbe offrire alle infezioni più opportunità di evolvere una resistenza maggiore o di riprendersi dopo il trattamento.
Cosa significa per il trattamento delle infezioni
Questo lavoro mostra che la disponibilità di nutrienti non è solo un dettaglio di sfondo ma un collo di bottiglia centrale che può permettere o limitare l’uccisione da parte degli antibiotici nelle popolazioni batteriche strutturate. Invece di chiedersi soltanto se un farmaco riesce a raggiungere il sito di infezione, clinici e ricercatori potrebbero anche dover considerare come le fonti di cibo fluiscono attraverso la comunità e quanto rapidamente le cellule le consumano. Il quadro offerto dallo studio, compresa la sua semplice misura per quando il consumo di nutrienti supera l’uccisione, fornisce un modo per prevedere quando il trattamento antibiotico probabilmente si arresterà su una conchiglia protettiva. Suggerisce inoltre che combinare antibiotici con strategie che alterano la penetrazione dei nutrienti o che perturbano la struttura spaziale potrebbe rendere i farmaci esistenti più efficaci, e mette in luce perché le infezioni dense, simili a biofilm, possono essere così ostinate anche quando i test di laboratorio indicano che un farmaco dovrebbe funzionare.
Citazione: Hancock, A.M., Dill-Macky, A.S., Moore, J.A. et al. A nutrient bottleneck controls antibiotic efficacy in structured bacterial populations. Nat Commun 17, 3337 (2026). https://doi.org/10.1038/s41467-026-69625-4
Parole chiave: resistenza agli antibiotici, biofilm batterici, gradienti di nutrienti, fosfomicina, dinamica delle popolazioni microbiche