Clear Sky Science · zh
关于分级 DNMT3A 自抑制及其在疾病中失调的结构见解
细胞如何标记其 DNA
我们体内的每个细胞都携带相同的 DNA,但心脏细胞与脑细胞的行为截然不同。细胞实现这一差异的一种方式是在线性 DNA 上添加微小的化学标签,帮助基因开启或关闭。本文探讨了一种关键的标记酶 DNMT3A 如何被严密控制——以及其结构上的微小改变如何使这些标记偏离目标并促成人类疾病。
对 DNA 的谨慎“上色者”
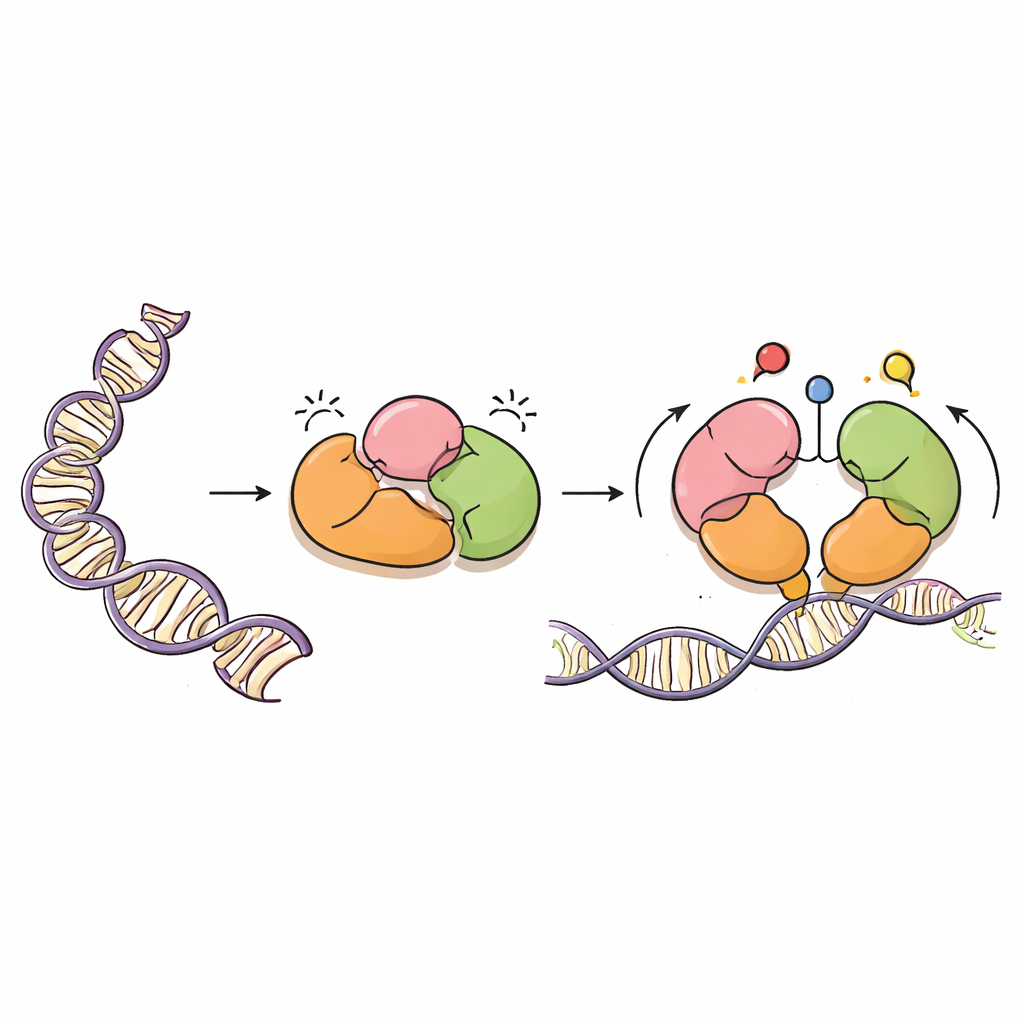
DNMT3A 是一种将甲基组——简单的碳基标记——添加到特定 DNA 碱基上的酶,通常作用于称为 CpG 的二核苷酸位点。这些标记对正常发育、亲本基因的印记以及基因组的长期稳定性至关重要。但像一台强力的喷漆机一样,DNMT3A 必须被精确引导。它与伴侣蛋白 DNMT3L 协同工作,并携带若干“读取”区,从而感知将 DNA 打包成染色质的组蛋白。这些读取区帮助 DNMT3A 判断应在何处工作以及何处保持沉默。
酶内置的刹车
作者使用冷冻电子显微镜解析了主要 DNMT3A 形式(DNMT3A2)与 DNMT3L 结合的三维结构。他们发现 DNMT3A 含有分层的自我制动机制,即自抑制。两个读取区,称为 PWWP 和 ADD,折回覆盖在酶的催化核心上,以物理方式阻挡识别 CpG 位点的区域,以及通常感应组蛋白化学标记的口袋。这种紧凑的构象阻止 DNMT3A 接触 DNA,在出现合适信号之前将其甲基化活性保持在较低水平。
组蛋白信号释放刹车
研究团队将他们的结构与先前已知的 DNMT3A 及相关蛋白与组蛋白片段结合的结构进行了叠加比对。比较显示,当组蛋白尾部携带特定标记——特别是未修饰的赖氨酸4(H3K4me0)和二甲基化的赖氨酸36(H3K36me2)——时,它们会与 DNMT3A 的内部联系发生竞争。组蛋白标记的结合把 PWWP 和 ADD 区域从催化核心以及识别 CpG 位点的柔性环上撬开。分子动力学模拟(模拟蛋白随时间的运动)显示,一旦这些内部夹具松动,识别 CpG 的环变得更具活动性并暴露出来,更有利于与 DNA 结合。实质上,DNMT3A 只有在感知到合适的染色质环境时,才从封闭的静息构象切换为更开放、更活跃的构象。
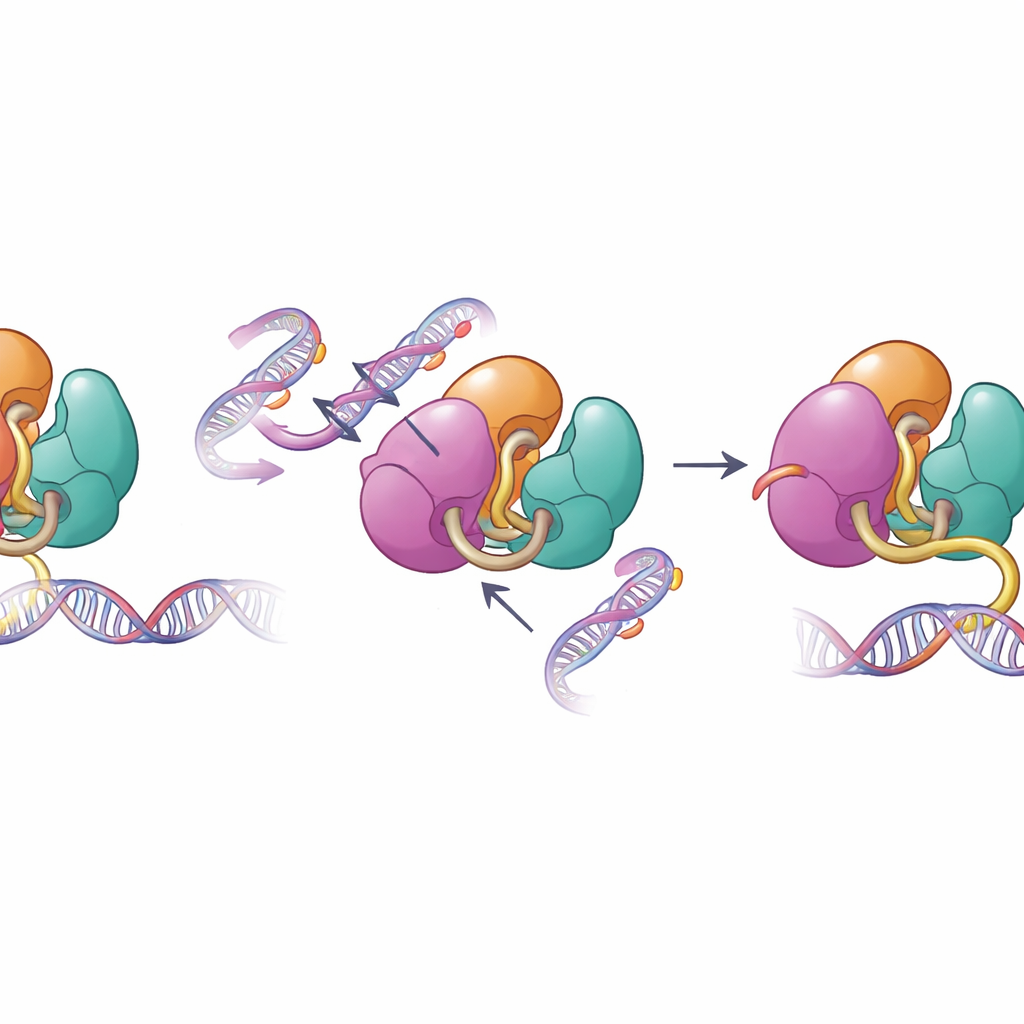
当结构防护失效时
介导自抑制的同一表面在多种人类疾病中经常被改变。作者检查了在血液癌症和发育障碍中发现的与疾病相关的 DNMT3A 变体,包括发生在 PWWP 和 ADD 区域的突变。生化测试显示,这些突变削弱了维持 DNMT3A 受控的内部接触,增强了其在体外实验中结合 DNA 并对其进行甲基化的能力。当团队在携带其中一种突变的小鼠干细胞中查看甲基化模式时,发现 DNMT3A 对正常组蛋白信号 H3K36me2 的响应减弱,并开始对通常较少被标记的基因组区段进行甲基化。这种靶向精确性的丧失有助于解释为何这些突变与患者中广泛且错位的 DNA 甲基化相关联。
这对健康意味着什么
总体而言,该研究揭示了 DNMT3A 是一台精细调控的机器,其活性由多层自我约束控制,仅在适当的染色质环境下被解除。通过精确描绘这些内部刹车如何工作——以及致病突变如何使其失效——这项工作为理解癌症和发育综合征中的异常 DNA 甲基化提供了结构蓝图。长远来看,对这些控制点的认识可能指导药物设计工作,温和地恢复 DNMT3A 的适当调控,纠正错误施加的 DNA 标记,而不完全关闭这一必需酶的功能。
引用: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
关键词: DNA 甲基化, 表观遗传学, DNMT3A, 染色质调控, 癌症突变