Clear Sky Science · tr
Hiyerarşik DNMT3A otoinhibisyonuna yapısal bakış ve hastalıkta bozulması
Hücreler DNA’larını nasıl işaretliyor
Vücudumuzdaki her hücre aynı DNA’yı taşır, ancak kalp hücreleri beyin hücrelerinden çok farklı davranır. Hücrelerin bunu başarmasının yollarından biri DNA’ya küçük kimyasal etiketler koymaktır; bu etiketler genleri açıp kapamaya yardımcı olur. Bu makale, ana etiketleme enzimi DNMT3A’nın nasıl sıkı şekilde kontrol altında tutulduğunu —ve yapısındaki küçük değişikliklerin bu etiketleri nasıl yanlış yönlendirebileceğini ve insan hastalıklarına nasıl katkıda bulunabileceğini— inceliyor.
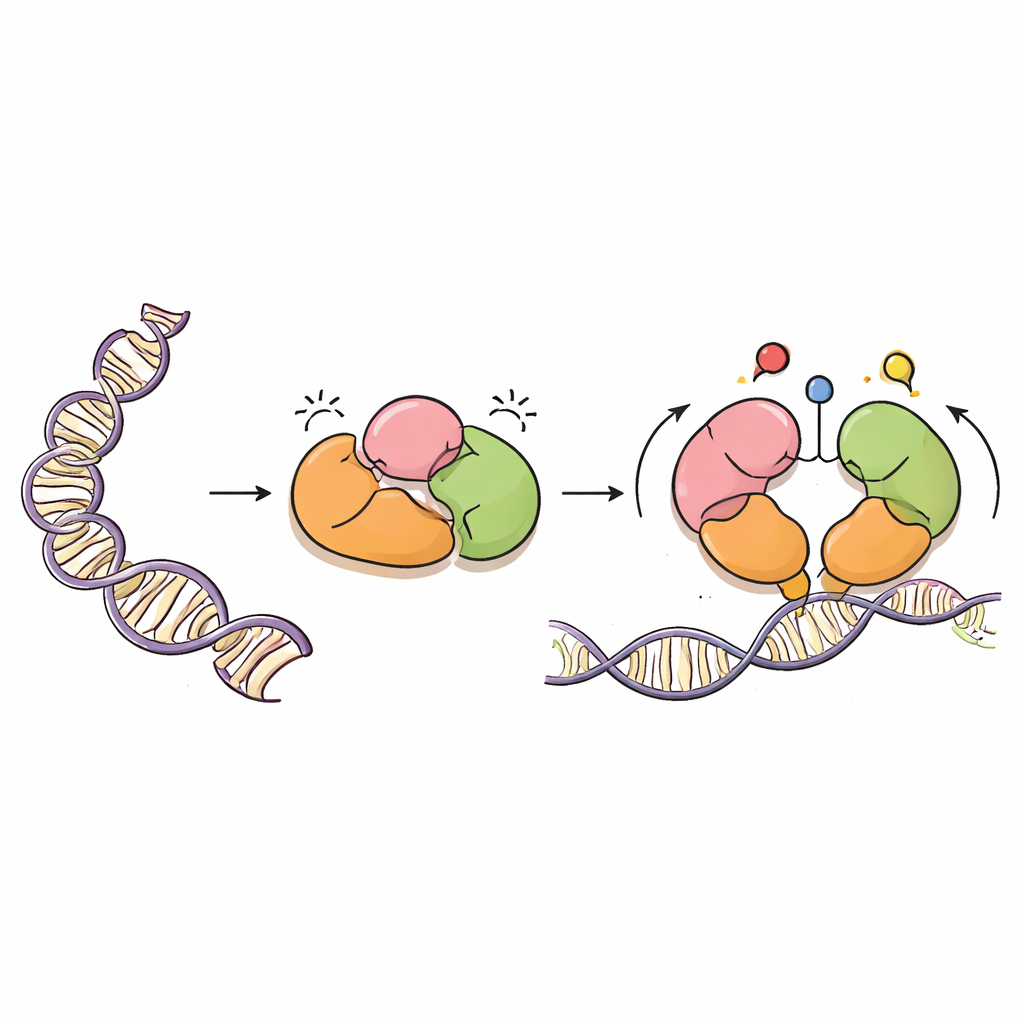
DNA’nın titiz bir boyacısı
DNMT3A, genellikle CpG dinükleotidleri adı verilen yerlerde belirli DNA bazlarına metil grupları—basit karbon temelli işaretler—ekleyen bir enzimdir. Bu işaretler normal gelişim, ebeveyn genlerinin imprinting’i ve genomlarımızın uzun vadeli stabilitesi için hayati öneme sahiptir. Ancak güçlü bir boya tabancası gibi, DNMT3A’nın da kesin biçimde yönlendirilmesi gerekir. DNMT3L adlı bir ortak proteinle birlikte çalışır ve DNA’yı kromatin halinde paketleyen histonlar adı verilen yakın proteinleri algılayan birkaç “okuyucu” bölge taşır. Bu okuyucu bölgeler DNMT3A’ya nerede çalışması gerektiğini ve nerede sessiz kalması gerektiğini bildirir.
Enzimin içindeki yerleşik frenler
Kryo-elektron mikroskopisi kullanarak, yazarlar DNMT3L’ye bağlı önemli bir DNMT3A formunun (DNMT3A2) üç boyutlu yapısını çözdüler. DNMT3A’nın katmanlı kendi kendini frenleme, yani otoinhibisyon içerdiğini keşfettiler. PWWP ve ADD adlı iki okuyucu bölge, enzim katalitik çekirdeğine geri katlanarak proteinin CpG bölgelerini tanıyan kısmını ve normalde histonlardaki kimyasal işaretleri algılayan cepleri fiziksel olarak engelliyor. Bu sıkı düzenleme, DNMT3A’nın DNA’ya erişimini engelleyerek doğru sinyaller ortaya çıkana dek metilasyon aktivitesini düşük tutar.
Histon sinyalleri frenleri serbest bırakır
Araştırma ekibi yapılarını, DNMT3A ve ilişkili proteinlerin histon parçacıklarına bağlı daha önce bilinen yapılarıyla üst üste koydu. Bu karşılaştırma, histon kuyrukları belirli işaretler taşıdığında—özellikle modifiye olmamış lizine-4 (H3K4me0) ve dimetile lizine-36 (H3K36me2)—DNMT3A’nın iç temaslarıyla yarıştığını gösterdi. Bu histon işaretlerinin bağlanması PWWP ve ADD bölgelerini katalitik çekirdekten ve CpG bölgelerini tanıyan esnek bir halkadan uzaklaştırıyor. Zaman içinde protein hareketini modelleyen moleküler dinamik simülasyonlar, bu iç kelepçeler gevşediğinde CpG tanıma halkasının daha hareketli ve açığa çıkmış hale geldiğini, böylece DNA ile etkileşime girmeye daha uygun konuma geldiğini ortaya koydu. Özetle, DNMT3A yalnızca uygun bir kromatin ortamı algıladığında kapalı, dinlenme halindeki biçiminden daha açık, aktif bir biçime geçer.
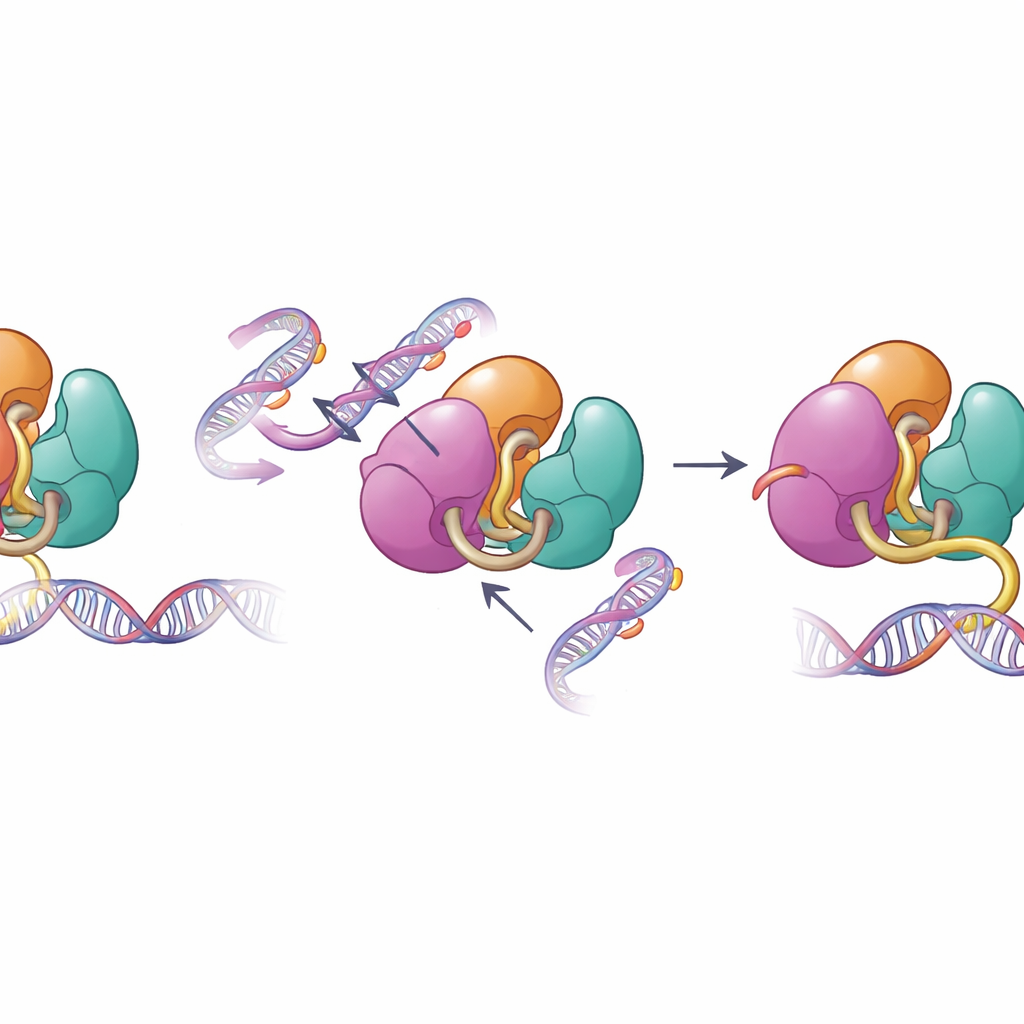
Yapısal koruyucular başarısız olduğunda
Otoinhibisyonu sağlayan aynı yüzeyler insan hastalıklarında sıklıkla değiştirilir. Yazarlar, kan kanserleri ve gelişimsel bozukluklarda görülen, PWWP ve ADD bölgelerindeki mutasyonlar dahil DNMT3A’daki hastalık ilişkili değişiklikleri incelediler. Biyokimyasal testler bu mutasyonların DNMT3A’yı dizginleyen iç temasları zayıflattığını, test tüpü deneylerinde onun DNA’ya bağlanma ve metileme yeteneğini artırdığını gösterdi. Ekip, bu mutasyonlardan birini taşıyan fare kök hücrelerindeki metilasyon desenlerine baktığında, DNMT3A’nın normal histon sinyali H3K36me2’ye daha az yanıt verdiğini ve genellikle daha az işaretli kalan genom bölgelerini metileştirmeye başladığını gördü. Hedefleme hassasiyetinin bu kaybı, bu tür mutasyonların hastalardaki yaygın ve yanlış yerdeki DNA metilasyonu ile ilişkilendirilmesini açıklamaya yardımcı olur.
Sağlık için neden önemli
Genel olarak çalışma, aktivitesi katmanlı oto-kısıtlamalarla yönetilen hassas ayarlı bir makine olarak DNMT3A’yı ortaya koyuyor; bu kısıtlamalar yalnızca doğru kromatin bağlamında serbest bırakılıyor. Bu iç frenlerin tam olarak nasıl çalıştığını—ve hastalık yapıcı mutasyonların bunları nasıl devre dışı bıraktığını—haritalayarak çalışma, kanser ve gelişimsel sendromlarda anormal DNA metilasyonunu anlamak için yapısal bir plan sunuyor. Uzun vadede, bu kontrol noktalarına ilişkin içgörüler, bu temel enzimi tamamen kapatmadan DNMT3A düzenlemesini nazikçe eski haline getirebilecek ilaç tasarım çabalarına yol gösterebilir.
Atıf: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Anahtar kelimeler: DNA metilasyonu, epigenetik, DNMT3A, kromatin düzenlemesi, kanser mutasyonları