Clear Sky Science · fr
Aperçu structural de l’autoinhibition hiérarchique de DNMT3A et de sa dérégulation dans les maladies
Comment les cellules marquent leur ADN
Toutes les cellules de notre corps portent le même ADN, pourtant les cellules cardiaques se comportent très différemment des cellules cérébrales. L’un des moyens par lesquels les cellules réalisent cela est l’apposition de minuscules marques chimiques sur l’ADN, qui contribuent à activer ou à réprimer des gènes. Cet article explore comment une enzyme clé de marquage, DNMT3A, est strictement contrôlée — et comment de petites altérations de sa structure peuvent dévier ces marques et contribuer à des maladies humaines.
Un peintre minutieux de l’ADN
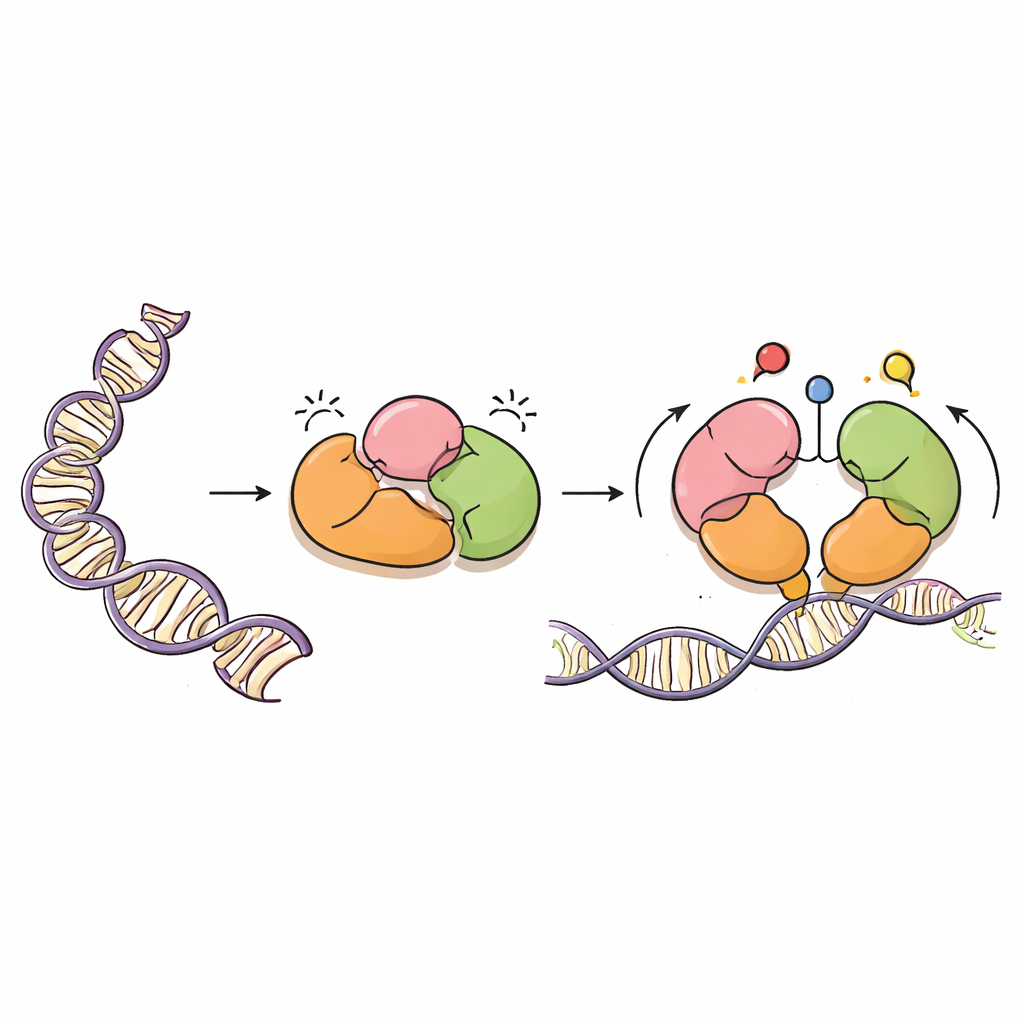
DNMT3A est une enzyme qui ajoute des groupes méthyle — de simples marques à base de carbone — à des lettres d’ADN spécifiques, généralement sur des sites appelés dinucléotides CpG. Ces marques sont essentielles au développement normal, à l’empreinte parentale des gènes et à la stabilité à long terme de nos génomes. Mais, à l’image d’un puissant pistolet à peinture, DNMT3A doit être guidée avec précision. Elle agit aux côtés d’une protéine partenaire, DNMT3L, et possède plusieurs régions « lectrices » qui détectent des protéines voisines appelées histones, lesquelles empaquettent l’ADN en chromatine. Ces régions lectrices aident DNMT3A à savoir où agir et où rester silencieuse.
Des freins intégrés dans l’enzyme
À l’aide de la cryo‑microscopie électronique, les auteurs ont résolu la structure tridimensionnelle d’une forme majeure de DNMT3A (DNMT3A2) liée à DNMT3L. Ils ont découvert que DNMT3A présente des niveaux d’autofreinage superposés, ou autoinhibition. Deux régions lectrices, appelées PWWP et ADD, se replient sur le cœur catalytique de l’enzyme de manière à bloquer physiquement la partie de la protéine qui reconnaît les sites CpG, ainsi que des poches qui détectent normalement des marques chimiques sur les histones. Cette configuration compacte empêche DNMT3A d’accéder à l’ADN, maintenant son activité de méthylation à un niveau bas jusqu’à l’apparition des signaux appropriés.
Les signaux des histones relâchent les freins
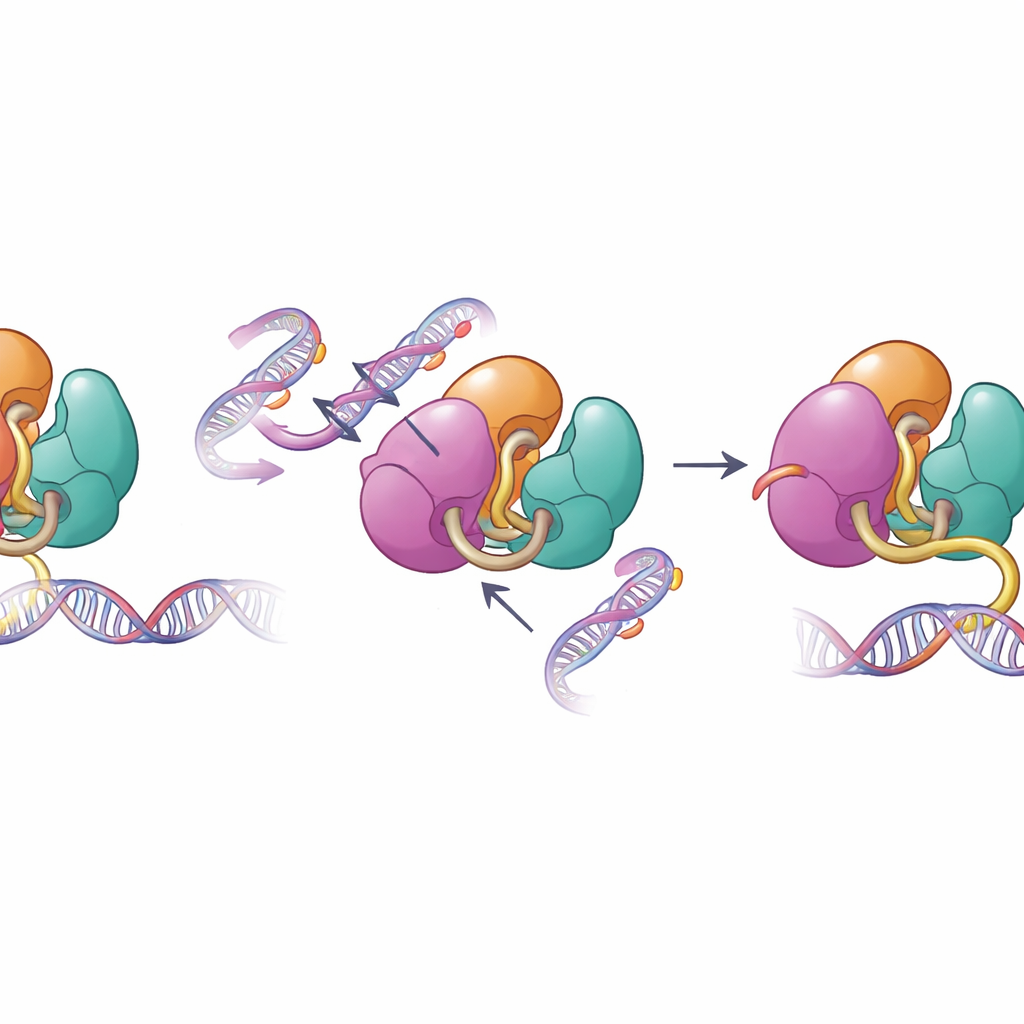
L’équipe a superposé leur structure avec des structures déjà connues de DNMT3A et de protéines apparentées liées à des fragments d’histones. Cette comparaison a montré que lorsque les queues d’histone portent certaines marques — spécifiquement la lysine‑4 non modifiée (H3K4me0) et la lysine‑36 diméthylée (H3K36me2) — elles entrent en compétition avec les contacts internes de DNMT3A. La liaison de ces marques d’histone éloigne les régions PWWP et ADD du cœur catalytique et d’une boucle flexible qui reconnaît les sites CpG. Des simulations de dynamique moléculaire, qui modélisent le mouvement des protéines dans le temps, ont révélé qu’une fois ces « serrures » internes desserrées, la boucle de reconnaissance des CpG devient plus mobile et exposée, mieux positionnée pour interagir avec l’ADN. En substance, DNMT3A bascule d’une conformation fermée et au repos vers une conformation plus ouverte et active uniquement lorsqu’elle détecte un environnement de chromatine approprié.
Quand les sécurités structurelles échouent
Les mêmes surfaces qui médiatisent l’autoinhibition sont fréquemment altérées dans les maladies humaines. Les auteurs ont examiné des altérations de DNMT3A liées à des maladies, observées dans des cancers du sang et des troubles du développement, incluant des mutations dans les régions PWWP et ADD. Des tests biochimiques ont montré que ces mutations affaiblissent les contacts internes qui maintiennent DNMT3A sous contrôle, augmentant sa capacité à se lier à l’ADN et à le méthyler dans des expériences in vitro. Lorsque l’équipe a analysé les profils de méthylation dans des cellules souches de souris portant l’une de ces mutations, ils ont constaté que DNMT3A devenait moins réactif au signal histone normal H3K36me2 et commençait à méthyler des portions du génome qui resteraient habituellement peu marquées. Cette perte de précision de ciblage aide à expliquer pourquoi de telles mutations s’associent à une méthylation de l’ADN étendue et déplacée chez les patients.
Pourquoi cela importe pour la santé
Dans l’ensemble, l’étude révèle DNMT3A comme une machine finement réglée dont l’activité est gouvernée par des couches imbriquées d’auto‑contrainte, relâchées seulement dans le bon contexte chromatine. En cartographiant précisément le fonctionnement de ces freins internes — et comment des mutations pathologiques les désactivent — ce travail fournit une feuille de route structurelle pour comprendre la méthylation anormale de l’ADN dans le cancer et les syndromes du développement. À terme, la compréhension de ces points de contrôle pourrait orienter la conception de médicaments visant à restaurer doucement la régulation correcte de DNMT3A, corrigeant les marques d’ADN mal appliquées sans inactiver totalement cette enzyme essentielle.
Citation: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Mots-clés: Méthylation de l’ADN, Épigénétique, DNMT3A, Régulation de la chromatine, Mutations liées au cancer