Clear Sky Science · it
Comprensione strutturale dell’autoinibizione gerarchica di DNMT3A e della sua disfunzione nelle malattie
Come le cellule segnano il loro DNA
Ogni cellula del nostro corpo contiene lo stesso DNA, eppure le cellule cardiache si comportano in modo molto diverso dalle cellule cerebrali. Un modo in cui le cellule ottengono questo risultato è posizionando piccole etichette chimiche sul DNA, che aiutano ad attivare o disattivare i geni. Questo articolo esplora come un enzima chiave per l’etichettatura, DNMT3A, viene mantenuto sotto stretto controllo—e come piccole modifiche alla sua struttura possano dirottare queste etichette e contribuire alle malattie umane.
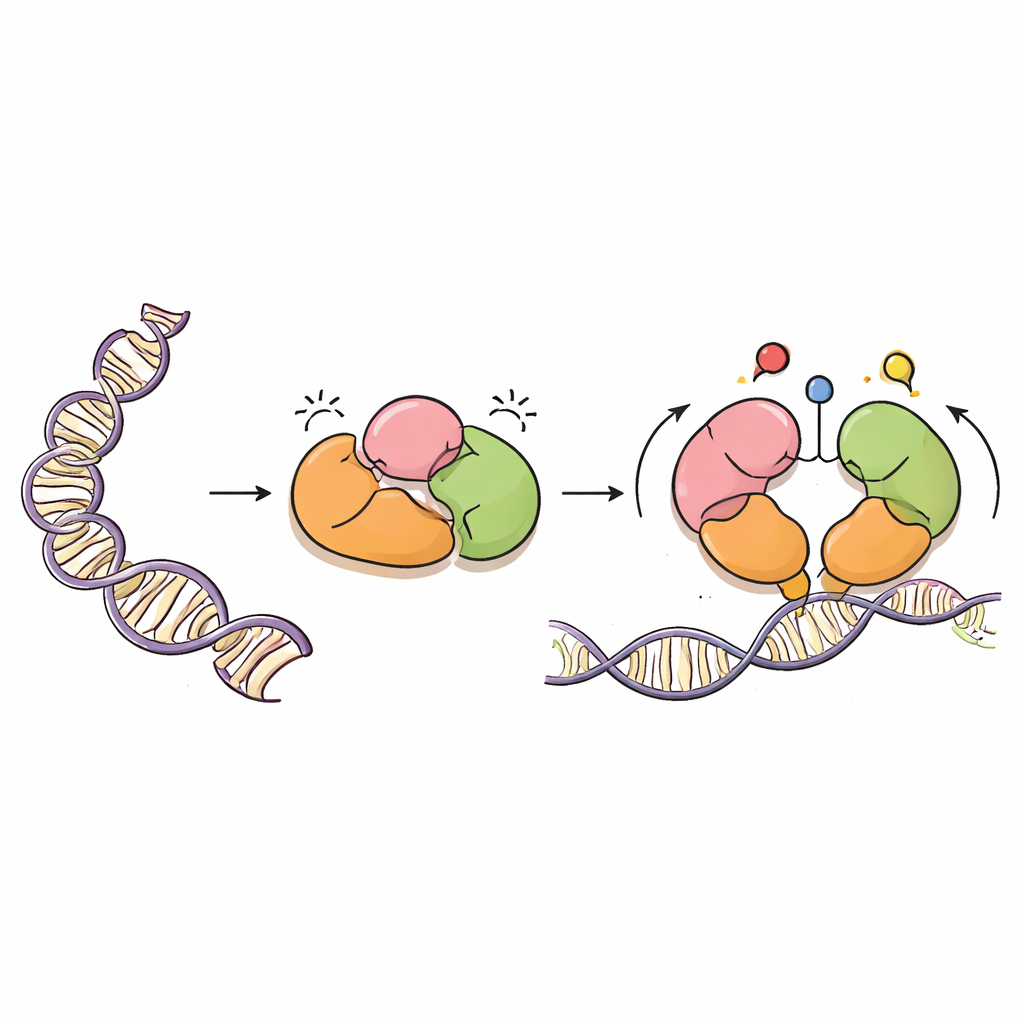
Un pittore accurato del DNA
DNMT3A è un enzima che aggiunge gruppi metile—semplici segni a base di carbonio—a specifiche lettere del DNA, di solito in siti chiamati dinucleotidi CpG. Questi segni sono fondamentali per lo sviluppo normale, l’imprinting dei geni parentali e la stabilità a lungo termine dei nostri genomi. Ma come uno spruzzatore di vernice potente, DNMT3A deve essere guidato con precisione. Opera insieme a una proteina partner, DNMT3L, e possiede diverse regioni “lettrici” che rilevano proteine vicine chiamate istoni, che impacchettano il DNA nella cromatina. Queste regioni lettrici aiutano DNMT3A a sapere dove deve operare e dove invece rimanere inattivo.
Freni incorporati all’interno dell’enzima
Usando la criomicroscopia elettronica, gli autori hanno risolto la struttura tridimensionale di una forma principale di DNMT3A (DNMT3A2) legata a DNMT3L. Hanno scoperto che DNMT3A contiene freni a strati, o autoinibizione. Due regioni lettrici, chiamate PWWP e ADD, si ripiegano sul core catalitico dell’enzima in modo da bloccare fisicamente la parte della proteina che riconosce i siti CpG, così come tasche che normalmente percepiscono i segni chimici sugli istoni. Questo assetto compatto impedisce a DNMT3A di accedere al DNA, mantenendo bassa la sua attività di metilazione fino a quando non compaiono i segnali appropriati.
I segnali degli istoni rilasciano i freni
Il gruppo ha sovrapposto la loro struttura con strutture precedentemente note di DNMT3A e proteine correlate legate a frammenti istonici. Il confronto ha mostrato che quando le code istoniche portano certi segni—specificamente la lisina-4 non modificata (H3K4me0) e la lisina-36 dimetilata (H3K36me2)—essi competono con i contatti interni di DNMT3A. Il legame di questi segni istonici stacca le regioni PWWP e ADD dal core catalitico e da un anello flessibile che riconosce i siti CpG. Le simulazioni di dinamica molecolare, che modellano il movimento delle proteine nel tempo, hanno rivelato che una volta allentate queste speciali clamp interne, l’anello di riconoscimento dei CpG diventa più mobile ed esposto, meglio posizionato per interagire con il DNA. In sostanza, DNMT3A passa da una forma chiusa e a riposo a una forma più aperta e attiva solo quando percepisce un ambiente cromatinico adatto.
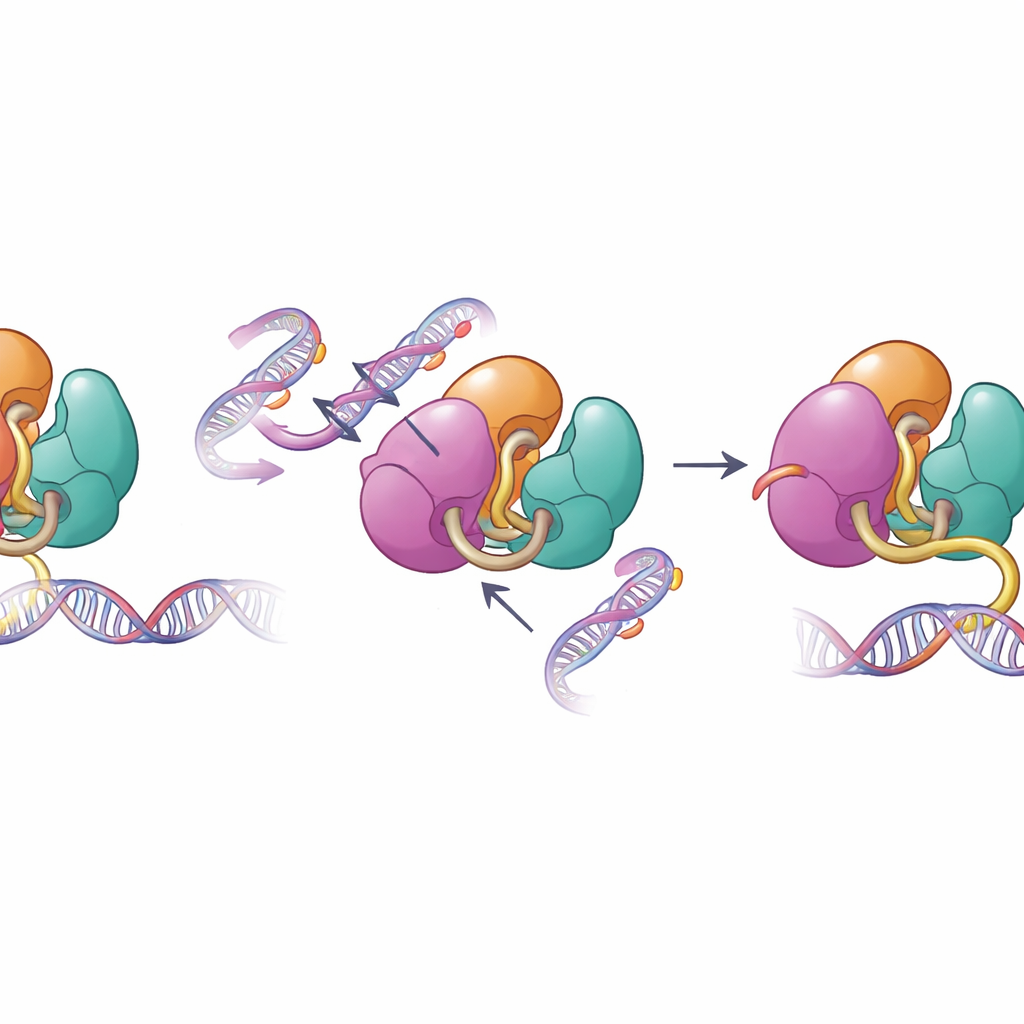
Quando le salvaguardie strutturali falliscono
Le stesse superfici che mediano l’autoinibizione sono frequentemente alterate nelle malattie umane. Gli autori hanno esaminato cambiamenti correlati a malattie in DNMT3A riscontrati nei tumori del sangue e nei disturbi dello sviluppo, incluse mutazioni nelle regioni PWWP e ADD. Test biochimici hanno mostrato che queste mutazioni indeboliscono i contatti interni che tengono DNMT3A sotto controllo, aumentando la sua capacità di legare il DNA e di metilarlo in esperimenti in provetta. Quando il gruppo ha analizzato i modelli di metilazione in cellule staminali murine portatrici di una di queste mutazioni, ha riscontrato che DNMT3A diventava meno sensibile al normale segnale istonico H3K36me2 e cominciava a metilare tratti del genoma che normalmente rimarrebbero meno marcati. Questa perdita di precisione nel targeting aiuta a spiegare perché tali mutazioni sono associate a una metilazione del DNA diffusa e mal indirizzata nei pazienti.
Perché questo è importante per la salute
Nel complesso, lo studio rivela DNMT3A come una macchina finemente tarata la cui attività è governata da strati annidati di auto-restrizione, rilasciati solo nel giusto contesto cromatinico. Mappando esattamente come funzionano questi freni interni—e come le mutazioni patogene li disattivano—il lavoro fornisce una guida strutturale per comprendere la metilazione anomala del DNA nel cancro e nelle sindromi dello sviluppo. A lungo termine, le intuizioni su questi punti di controllo potrebbero orientare gli sforzi per progettare farmaci che ripristinino delicatamente la regolazione corretta di DNMT3A, correggendo i segni del DNA applicati in modo errato senza spegnere completamente questo enzima essenziale.
Citazione: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Parole chiave: Metilazione del DNA, Epigenetica, DNMT3A, Regolazione della cromatina, Mutazioni nel cancro