Clear Sky Science · de
Strukturelle Einblicke in die hierarchische Autoinhibition von DNMT3A und ihre Fehlregulation bei Krankheiten
Wie Zellen ihre DNA markieren
Jede Zelle in unserem Körper trägt dieselbe DNA, und doch verhalten sich Herz- und Nervenzellen sehr unterschiedlich. Eine Möglichkeit, wie Zellen das erreichen, ist das Anbringen winziger chemischer Markierungen an der DNA, die helfen, Gene ein- oder auszuschalten. Dieser Artikel untersucht, wie ein zentrales Markierungsenzym, DNMT3A, streng kontrolliert wird — und wie kleine Veränderungen seiner Struktur diese Markierungen fehlleiten und zu menschlichen Erkrankungen beitragen können.
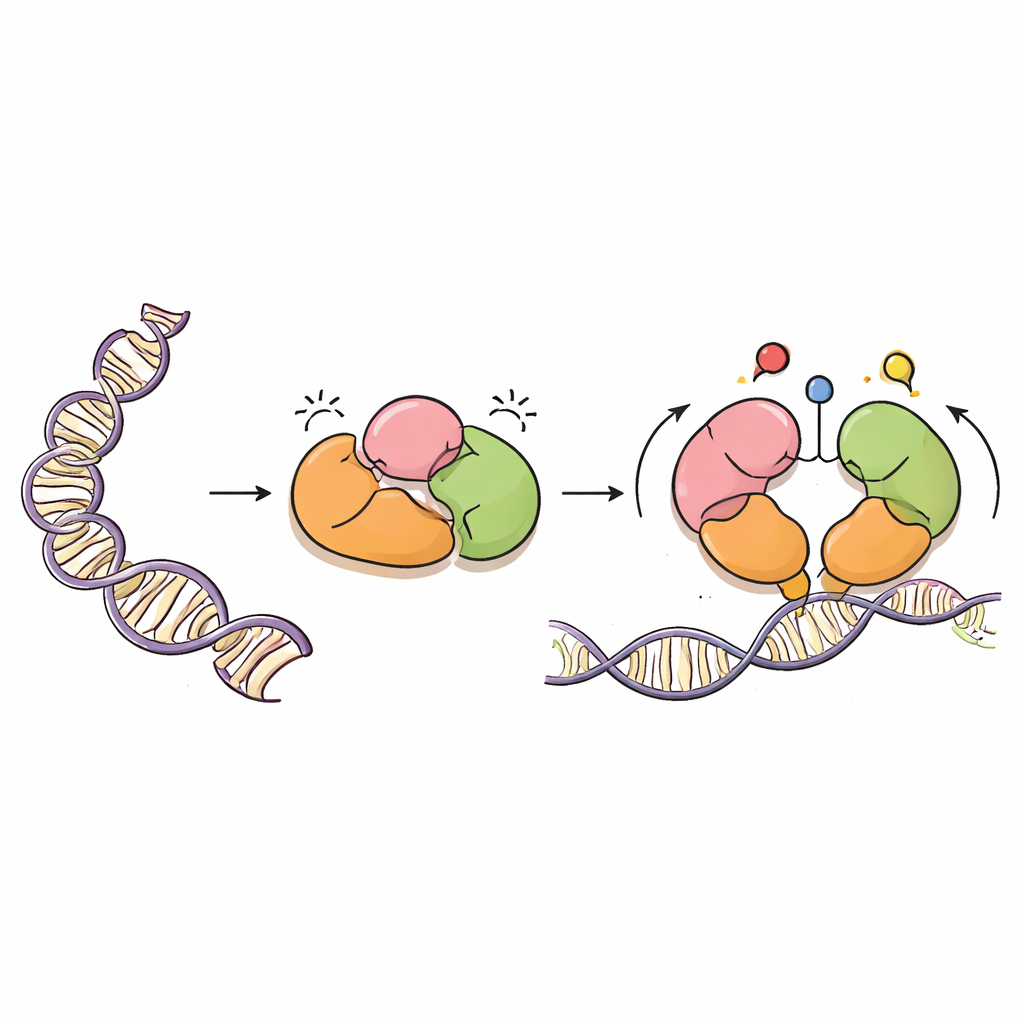
Ein sorgfältiger Maler der DNA
DNMT3A ist ein Enzym, das Methylgruppen — einfache kohlenstoffbasierte Markierungen — an bestimmte DNA-Buchstaben anbringt, üblicherweise an Stellen, die CpG-Dinukleotide genannt werden. Diese Markierungen sind für die normale Entwicklung, die Prägung elterlicher Gene und die langfristige Stabilität unseres Genoms von zentraler Bedeutung. Wie ein leistungsstarker Farbsprüher muss DNMT3A jedoch präzise gesteuert werden. Es arbeitet mit einem Partnerprotein, DNMT3L, zusammen und besitzt mehrere „Reader“-Domänen, die benachbarte Proteine namens Histone wahrnehmen, welche die DNA zu Chromatin verpacken. Diese Reader helfen DNMT3A zu erkennen, wo es wirken soll und wo es still bleiben muss.
eingebaute Bremsen im Enzym
Mithilfe der Kryo-Elektronenmikroskopie haben die Autoren die dreidimensionale Struktur einer wichtigen DNMT3A-Form (DNMT3A2) gebunden an DNMT3L gelöst. Sie fanden heraus, dass DNMT3A gestaffelte Selbsthemmung, also Autoinhibition, enthält. Zwei Reader-Domänen, genannt PWWP und ADD, klappen zurück auf den katalytischen Kern des Enzyms und blockieren physisch den Teil des Proteins, der CpG-Stellen erkennt, sowie Taschen, die normalerweise chemische Histonmarkierungen wahrnehmen. Diese kompakte Anordnung verhindert, dass DNMT3A Zugang zur DNA erhält, und hält seine methylierende Aktivität niedrig, bis die richtigen Signale erscheinen.
Histonsignale lösen die Bremsen
Das Team überlagerte ihre Struktur mit zuvor bekannten Strukturen von DNMT3A und verwandten Proteinen, die an Histonfragmente gebunden sind. Dieser Vergleich zeigte, dass, wenn Histonschwänze bestimmte Markierungen tragen — speziell unmodifiziertes Lysin-4 (H3K4me0) und dimethyliertes Lysin-36 (H3K36me2) — diese mit den internen Kontakten von DNMT3A konkurrieren. Die Bindung dieser Histonmarkierungen hebelt die PWWP- und ADD-Domänen vom katalytischen Kern und von einer flexiblen Schleife, die CpG-Stellen erkennt, weg. Molekulardynamik-Simulationen, die die Proteinbewegung über die Zeit modellieren, zeigten, dass, sobald diese internen Klemmen gelockert sind, die CpG-Erkennungs-Schleife beweglicher und exponierter wird und besser positioniert ist, um die DNA zu binden. Im Grunde schaltet DNMT3A nur dann von einer geschlossenen, ruhenden in eine offenere, aktive Form um, wenn es eine geeignete Chromatinumgebung erkennt.
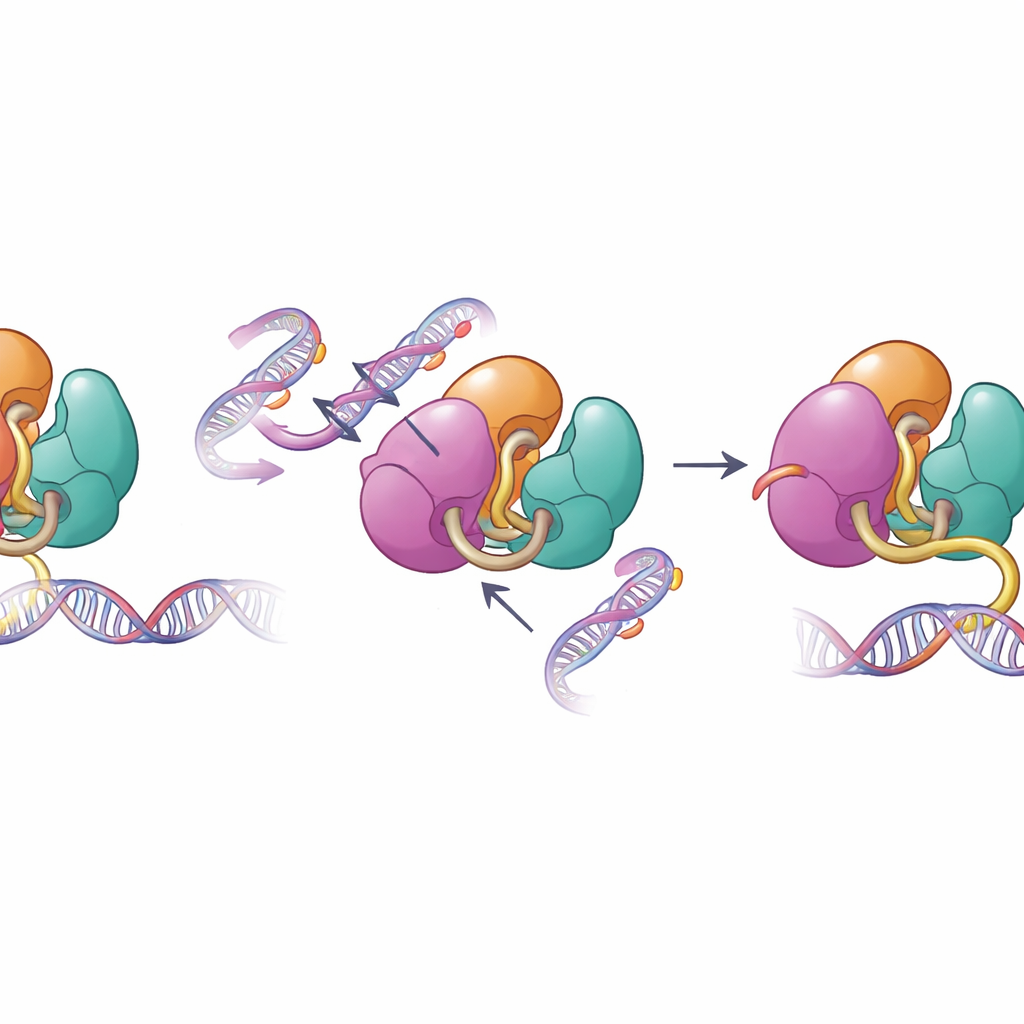
Wenn strukturelle Schutzmechanismen versagen
Die gleichen Oberflächen, die die Autoinhibition vermitteln, sind bei menschlichen Erkrankungen häufig verändert. Die Autoren untersuchten krankheitsassoziierte Veränderungen in DNMT3A, die bei Blutkrebs und Entwicklungsstörungen gefunden werden, einschließlich Mutationen in den PWWP- und ADD-Domänen. Biochemische Tests zeigten, dass diese Mutationen die internen Kontakte schwächen, die DNMT3A in Schach halten, und seine Fähigkeit verstärken, DNA zu binden und sie in Reagenzgläsern zu methylieren. Als das Team Methylierungsmuster in murinen Stammzellen mit einer dieser Mutationen untersuchte, stellten sie fest, dass DNMT3A weniger auf das normale Histonsignal H3K36me2 reagierte und begann, Genomabschnitte zu methylieren, die sonst weniger markiert bleiben würden. Dieser Verlust an Zielgenauigkeit erklärt, warum solche Mutationen mit weitverbreiteter, fehlplatzierter DNA-Methylierung bei Patienten in Zusammenhang stehen.
Warum das für die Gesundheit wichtig ist
Insgesamt zeigt die Studie DNMT3A als eine fein abgestimmte Maschine, deren Aktivität durch verschachtelte Selbsthemmungsmechanismen geregelt wird, die nur in der richtigen Chromatinumgebung aufgehoben werden. Indem genau kartiert wird, wie diese internen Bremsen funktionieren — und wie krankheitsverursachende Mutationen sie außer Kraft setzen — liefert die Arbeit einen strukturellen Bauplan zum Verständnis abnormaler DNA-Methylierung bei Krebs und Entwicklungsstörungen. Langfristig könnten Erkenntnisse über diese Kontrollpunkte die Entwicklung von Wirkstoffen leiten, die die korrekte DNMT3A-Regulation behutsam wiederherstellen und fehlangepasste DNA-Markierungen korrigieren, ohne dieses lebenswichtige Enzym vollständig zu blockieren.
Zitation: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Schlüsselwörter: DNA-Methylierung, Epigenetik, DNMT3A, Chromatin-Regulation, Krebsmutationen