Clear Sky Science · ja
階層的なDNMT3A自己抑制の構造的洞察と疾患におけるその破綻
細胞はどうやってDNAに印を付けるか
体のすべての細胞は同じDNAを持っているにもかかわらず、心筋細胞と脳細胞では挙動が大きく異なります。細胞がこの違いを生み出す手段の一つが、DNAに小さな化学的タグを付けて遺伝子のオン・オフを制御することです。本稿では、主要なタグ付け酵素であるDNMT3Aがどのように厳密に制御されているか、そしてその構造に小さな変化が生じるとどうやってこれらのタグの付け先が誤り、人間の疾患に寄与しうるかを解説します。
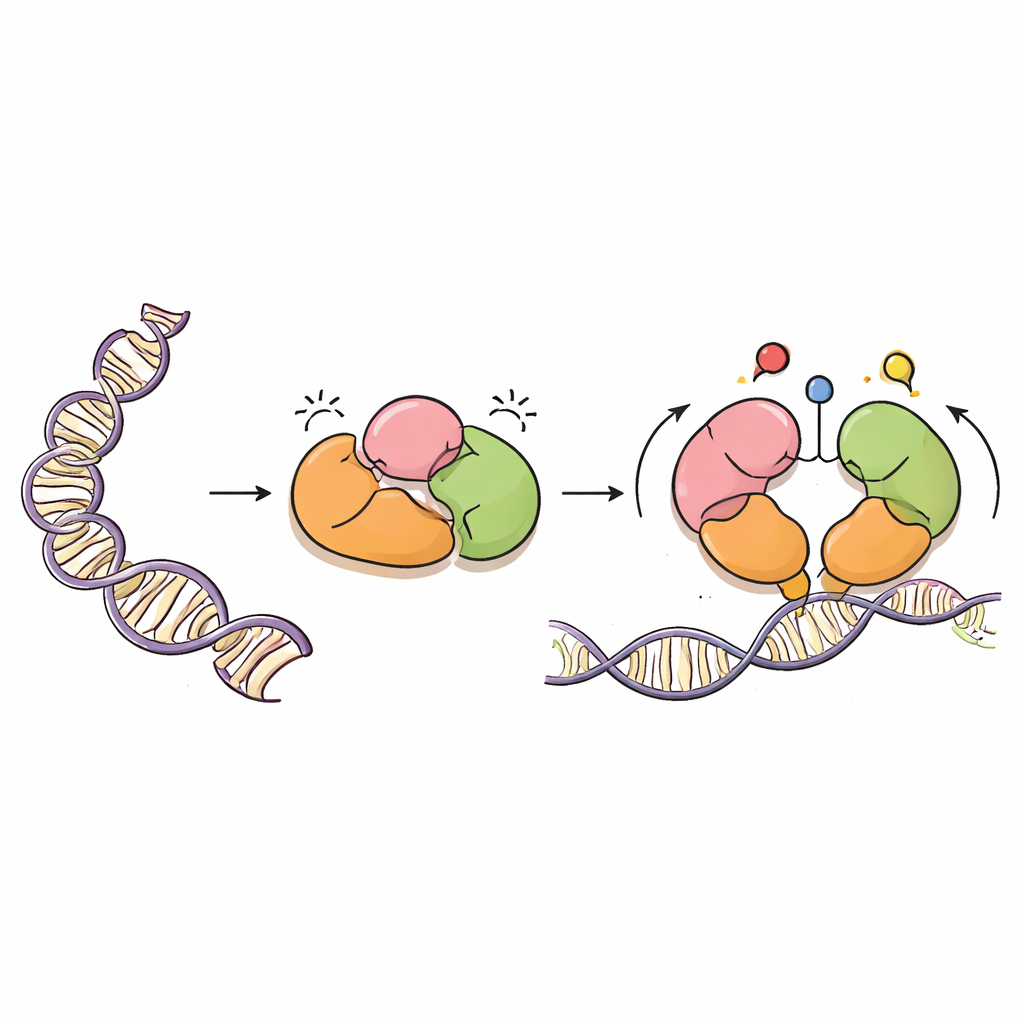
DNAの慎重な“塗装者”
DNMT3Aはメチル基――単純な炭素を含むマーク――を特定のDNA塩基、通常はCpG二核酸に付加する酵素です。これらのマークは正常な発生、遺伝子のインプリンティング、ゲノムの長期的安定性に不可欠です。しかし強力な塗装機のように、DNMT3Aは正確に導かれる必要があります。DNMT3Lという相方タンパク質と協働し、ヒストンと呼ばれるDNAをパッケージするタンパク質の近傍を感知するいくつかの“リーダー”領域を持っています。これらのリーダー領域が、DNMT3Aがどこで作用すべきか、どこで静かにしているべきかを判断する手助けをします。
酵素内に組み込まれたブレーキ
著者らはクライオ電子顕微鏡を用いて、主要なDNMT3Aの形(DNMT3A2)がDNMT3Lに結合した三次元構造を解明しました。その結果、DNMT3Aには階層化された自己抑制、つまりオートインヒビションが存在することが明らかになりました。PWWPとADDと呼ばれる二つのリーダー領域が触媒コアに折り返して結合し、CpG部位を認識する領域や通常ヒストン上の化学マークを感知するポケットを物理的に遮断しています。この緊密な配置はDNMT3AがDNAにアクセスするのを防ぎ、適切なシグナルが現れるまでメチル化活性を低く保ちます。
ヒストンのシグナルがブレーキを解く
研究チームは、自らの構造を既知のヒストン断片と結合したDNMT3Aや関連タンパク質の構造と重ね合わせました。この比較により、ヒストンテールが特定のマーク、具体的には非修飾リジン4(H3K4me0)と二量化メチル化リジン36(H3K36me2)を持つとき、これらがDNMT3Aの内部接触と競合することが示されました。これらのヒストンマークの結合はPWWPとADD領域を触媒コアおよびCpGを認識する柔軟なループから引き離します。分子動力学シミュレーション(時間経過でのタンパク質の動きをモデル化する手法)は、これらの内部クランプが緩むとCpG認識ループがより可動になり露出してDNAと相互作用しやすくなることを示しました。本質的には、DNMT3Aは適切なクロマチン環境を感知したときにのみ閉じた休止形状からより開いた活性形状へと切り替わります。
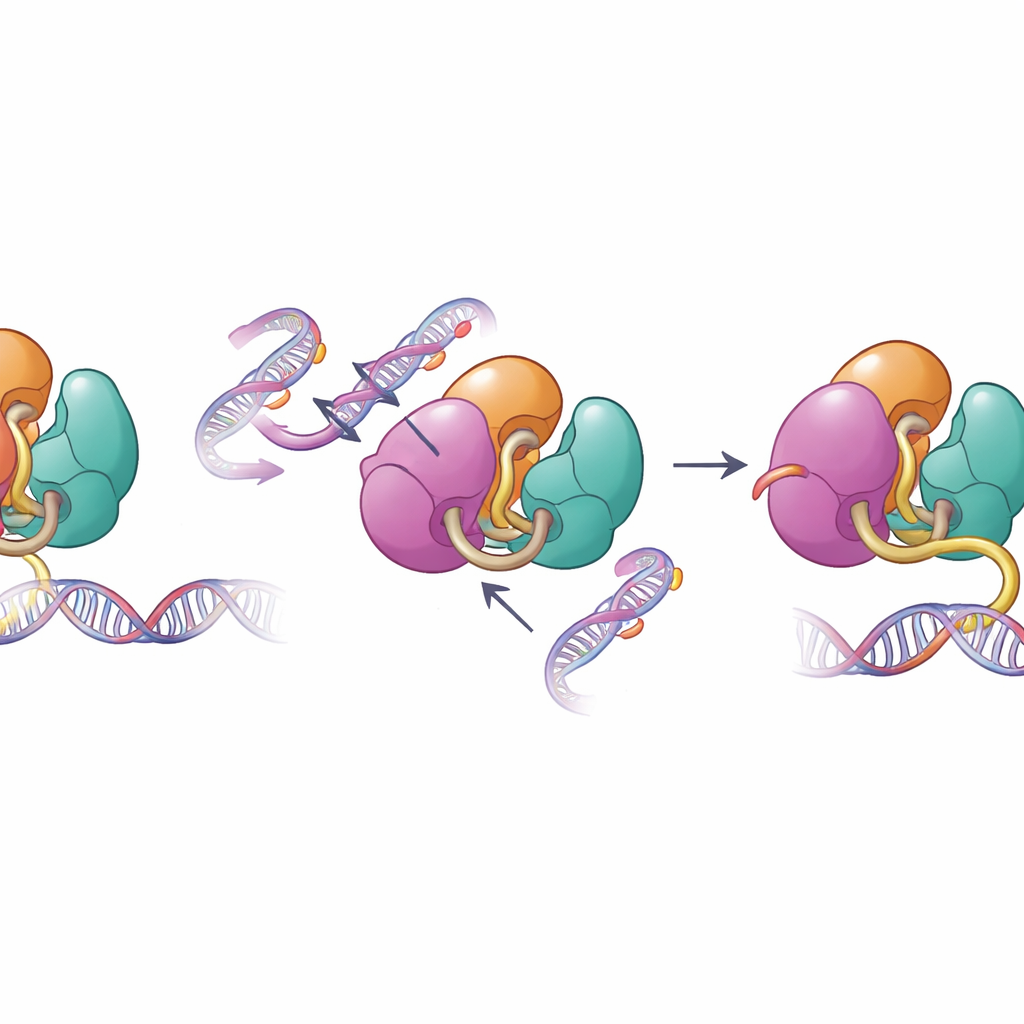
構造的安全装置が破綻するとき
オートインヒビションを仲介する同じ表面はヒトの疾患でしばしば変化します。著者らは血液がんや発達障害で見られるDNMT3Aの疾患関連変化、特にPWWPおよびADD領域の変異を調べました。生化学的試験により、これらの変異はDNMT3Aを抑える内部接触を弱め、試験管内でのDNA結合能とメチル化能を高めることが示されました。チームがこれらの変異の一つを持つマウス幹細胞のメチル化パターンを調べると、DNMT3Aは正常なヒストンシグナルH3K36me2に対する応答性が低下し、本来はあまりマークされない領域を新たにメチル化し始めていました。この標的の精度喪失は、患者で観察される広範で誤ったDNAメチル化とこれらの変異との関連を説明する助けになります。
なぜ健康にとって重要か
総じて、この研究はDNMT3Aを、入れ子状の自己抑制層によってその活性が精密に制御され、適切なクロマチン状況でのみ解除される精巧な機械として明らかにしました。これら内部ブレーキがどのように働くか、また疾患を引き起こす変異がそれをどのように無効化するかを正確に示すことで、がんや発達症候群における異常なDNAメチル化を理解するための構造的青写真を提供します。長期的には、これらの制御点に関する洞察が、DNMT3Aの規制を穏やかに回復させ、誤って付けられたDNAマークを修正しつつこの必須酵素を完全に停止させないような薬剤設計の指針になる可能性があります。
引用: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
キーワード: DNAメチル化, エピジェネティクス, DNMT3A, クロマチン制御, がん変異