Clear Sky Science · pt
Visão estrutural sobre a autoinibição hierárquica da DNMT3A e sua desregulação em doenças
Como as células marcam seu DNA
Cada célula do nosso corpo carrega o mesmo DNA, mas células do coração se comportam de forma bem diferente das células do cérebro. Uma maneira pela qual as células conseguem isso é colocando pequenas marcas químicas no DNA, ajudando a ligar ou desligar genes. Este artigo explora como uma enzima-chave de marcação, a DNMT3A, é mantida sob controle rigoroso — e como pequenas alterações em sua estrutura podem desviar essas marcas e contribuir para doenças humanas.
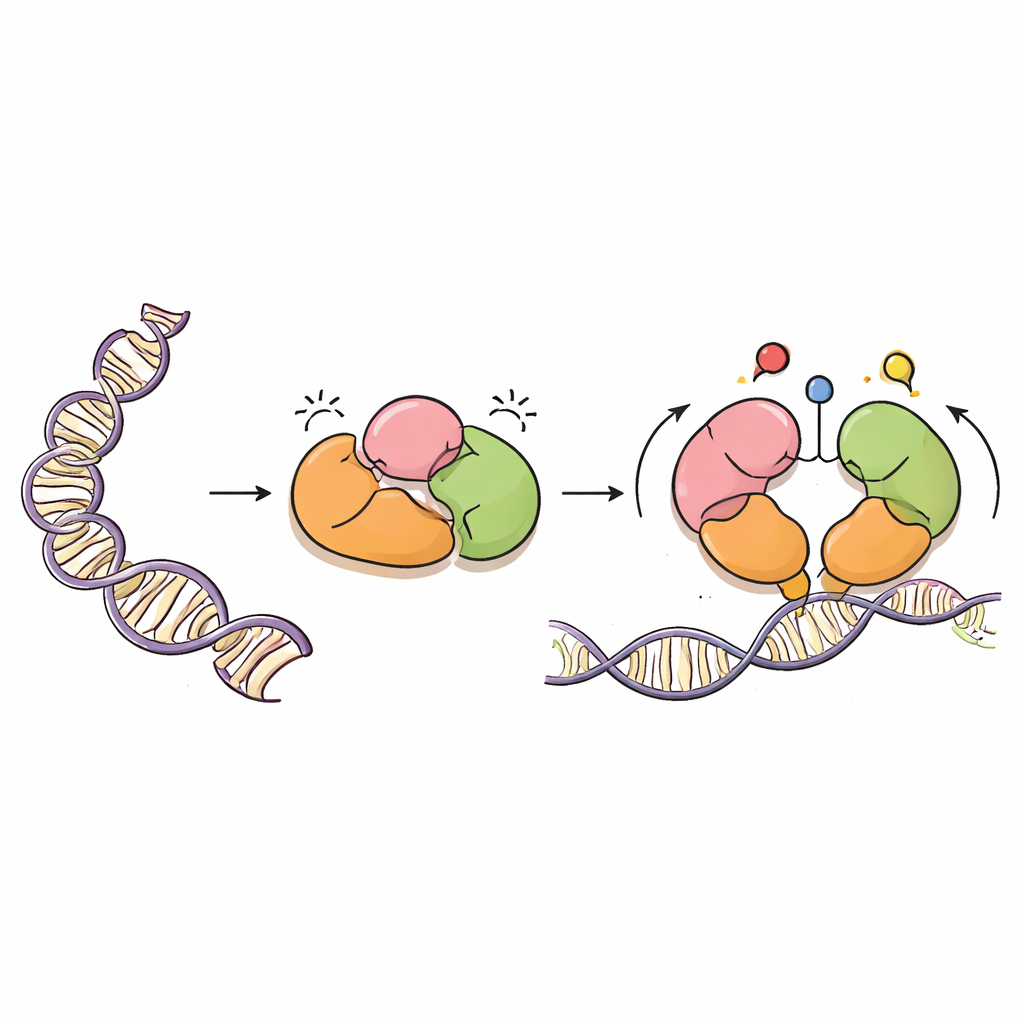
Um pintor cuidadoso do DNA
A DNMT3A é uma enzima que adiciona grupos metila — marcas simples à base de carbono — a letras específicas do DNA, geralmente em locais chamados dinucleotídeos CpG. Essas marcas são vitais para o desenvolvimento normal, para o imprinting de genes parentais e para a estabilidade a longo prazo dos nossos genomas. Mas, como um potente pulverizador de tinta, a DNMT3A precisa ser direcionada com precisão. Ela funciona ao lado de uma proteína parceira, a DNMT3L, e possui várias regiões “leitoras” que detectam proteínas próximas chamadas histonas, que empacotam o DNA em cromatina. Essas regiões leitoras ajudam a DNMT3A a saber onde deve atuar e onde deve permanecer inativa.
Freios internos dentro da enzima
Usando criomicroscopia eletrônica, os autores resolveram a estrutura tridimensional de uma forma importante da DNMT3A (DNMT3A2) ligada à DNMT3L. Eles descobriram que a DNMT3A contém camadas de autorregulação inibitória, ou autoinibição. Duas regiões leitoras, chamadas PWWP e ADD, dobram-se sobre o núcleo catalítico da enzima de forma a bloquear fisicamente a parte da proteína que reconhece sítios CpG, bem como bolsões que normalmente detectam marcas químicas nas histonas. Essa disposição compacta impede que a DNMT3A acesse o DNA, mantendo sua atividade metiladora baixa até que surjam os sinais apropriados.
Sinais das histonas liberam os freios
O grupo sobrepôs sua estrutura a estruturas previamente conhecidas da DNMT3A e proteínas relacionadas ligadas a fragmentos de histona. Essa comparação mostrou que, quando as caudas das histonas carregam certas marcas — especificamente a lisina-4 não modificada (H3K4me0) e a lisina-36 dimetilada (H3K36me2) — elas competem com os contatos internos da DNMT3A. A ligação dessas marcas histônicas afasta as regiões PWWP e ADD do núcleo catalítico e de um laço flexível que reconhece sítios CpG. Simulações de dinâmica molecular, que modelam o movimento da proteína ao longo do tempo, revelaram que, uma vez afrouxadas essas trava internas, o laço de reconhecimento de CpG torna-se mais móvel e exposto, melhor posicionado para interagir com o DNA. Em essência, a DNMT3A alterna de uma forma fechada e em repouso para uma forma mais aberta e ativa somente quando detecta um ambiente de cromatina adequado.
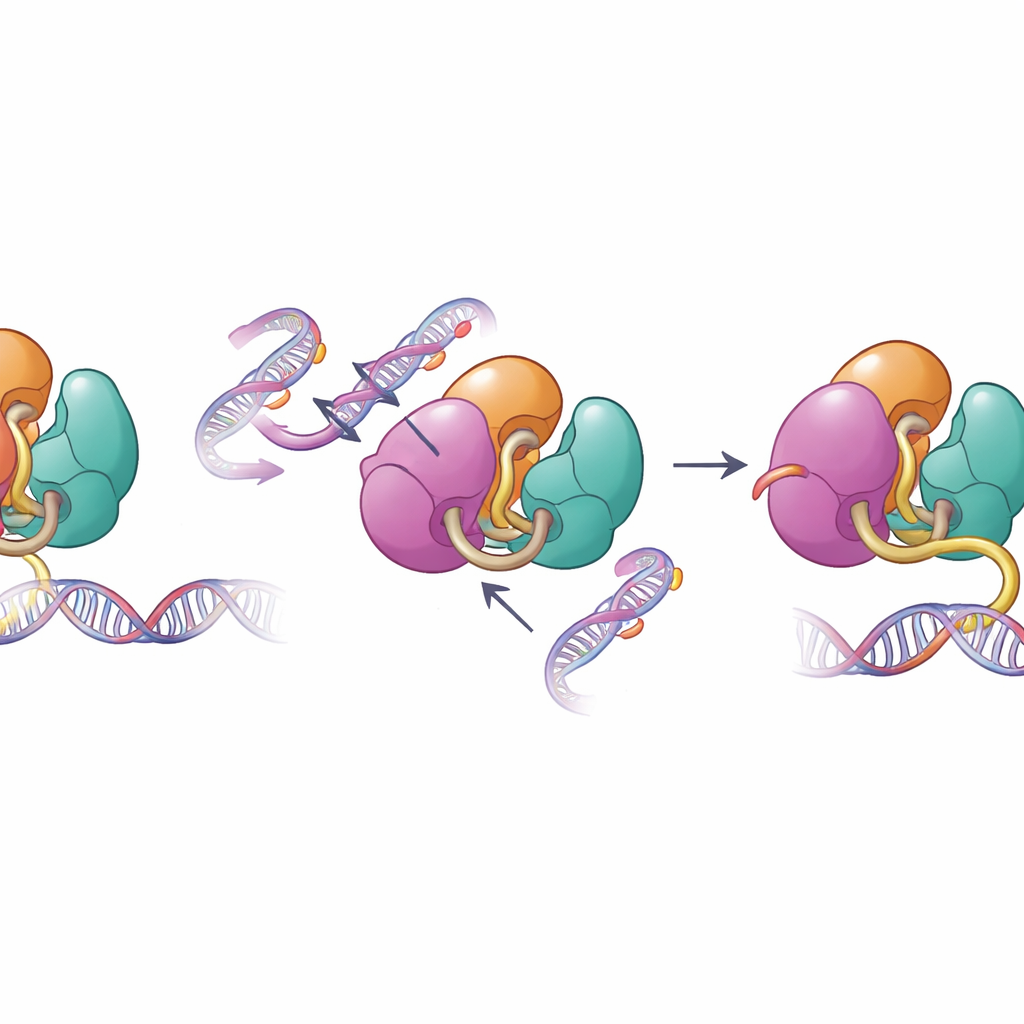
Quando as salvaguardas estruturais falham
As mesmas superfícies que mediam a autoinibição são frequentemente alteradas em doenças humanas. Os autores examinaram alterações ligadas a doenças na DNMT3A encontradas em cânceres do sangue e em distúrbios do desenvolvimento, incluindo mutações nas regiões PWWP e ADD. Testes bioquímicos mostraram que essas mutações enfraquecem os contatos internos que mantêm a DNMT3A sob controle, reforçando sua capacidade de se ligar ao DNA e metilá-lo em experimentos de bancada. Quando a equipe analisou padrões de metilação em células-tronco de camundongos que carregavam uma dessas mutações, descobriram que a DNMT3A ficou menos responsiva ao sinal histônico normal H3K36me2 e começou a metilar trechos do genoma que normalmente permaneceriam menos marcados. Essa perda de precisão no direcionamento ajuda a explicar por que tais mutações estão associadas a metilação do DNA extensa e mal posicionada em pacientes.
Por que isso importa para a saúde
No geral, o estudo revela a DNMT3A como uma máquina finamente ajustada cuja atividade é governada por camadas aninhadas de autorrepressão, liberadas apenas no contexto cromatínico apropriado. Ao mapear exatamente como esses freios internos funcionam — e como mutações causadoras de doenças os desativam — o trabalho fornece um roteiro estrutural para entender a metilação anômala do DNA em câncer e síndromes do desenvolvimento. A longo prazo, os insights sobre esses pontos de controle podem orientar esforços para projetar fármacos que restaurem suavemente a regulação adequada da DNMT3A, corrigindo marcas de DNA aplicadas de forma inadequada sem desligar completamente essa enzima essencial.
Citação: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Palavras-chave: metilação do DNA, epigenética, DNMT3A, regulação da cromatina, mutações cancerígenas