Clear Sky Science · nl
Structureel inzicht in hiërarchische DNMT3A-autoremming en de deregulatie daarvan bij ziekte
Hoe cellen hun DNA markeren
Elke cel in ons lichaam draagt hetzelfde DNA, maar hartcellen gedragen zich heel anders dan hersencellen. Een manier waarop cellen dit voor elkaar krijgen, is door kleine chemische labels op het DNA aan te brengen, die helpen genen aan of uit te zetten. Dit artikel onderzoekt hoe een sleutel-enzym voor die labeling, DNMT3A, strak wordt gecontroleerd — en hoe kleine structurele veranderingen deze labels kunnen misrichten en bijdragen aan menselijke ziekte.
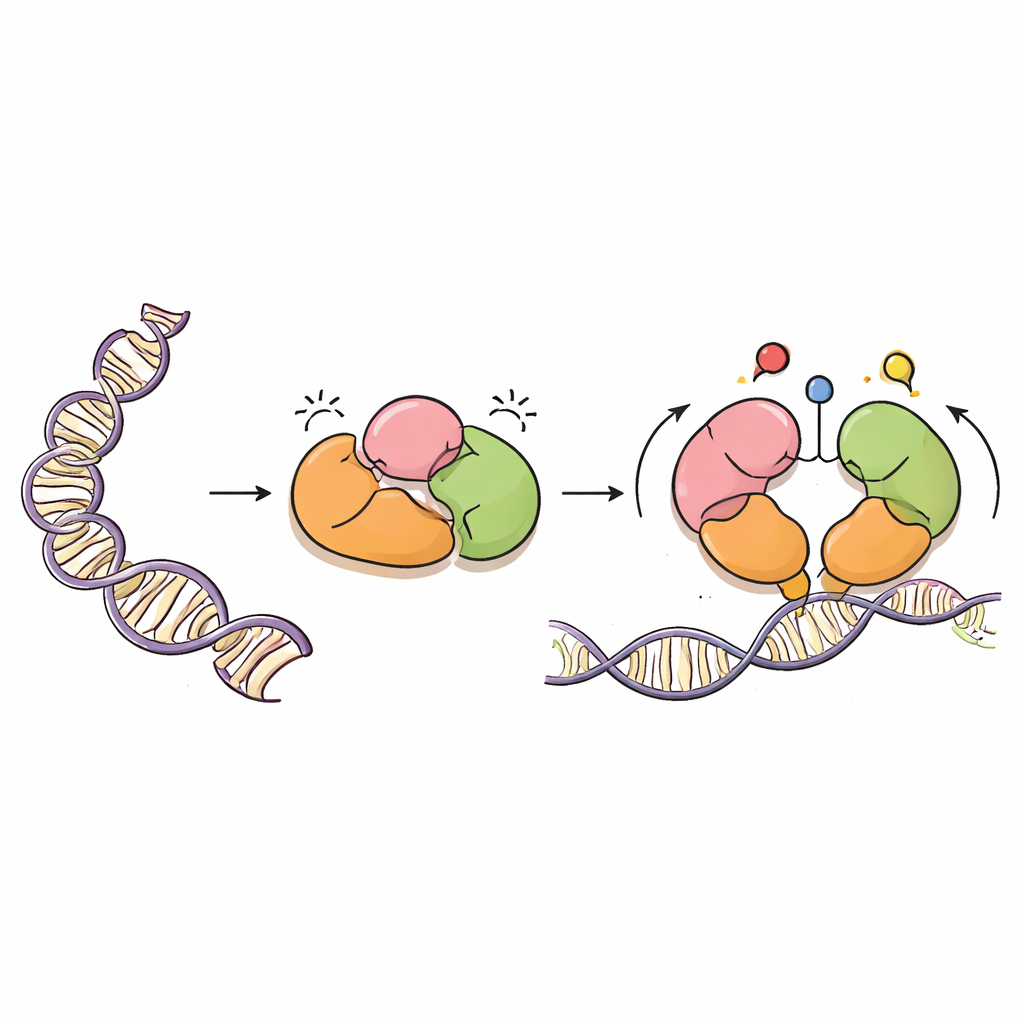
Een voorzichtige schilder van DNA
DNMT3A is een enzym dat methylgroepen toevoegt — eenvoudige koolstofhoudende labels — aan specifieke DNA-letters, meestal op locaties die CpG-dinucleotiden worden genoemd. Deze labels zijn essentieel voor normale ontwikkeling, het imprinten van ouderlijke genen en de langetermijnstabiliteit van onze genomen. Maar net als een krachtige verfspuit moet DNMT3A precies worden gestuurd. Het werkt samen met een partnerproteïne, DNMT3L, en draagt meerdere "lezer"-domeinen die naburige eiwitten, histonen genaamd, kunnen herkennen; histonen pakken DNA in tot chromatine. Deze lezer-domeinen helpen DNMT3A te weten waar het actief moet zijn en waar het stil moet blijven.
Ingebouwde remmen in het enzym
Met cryo-elektronenmicroscopie losten de auteurs de driedimensionale structuur van een belangrijke DNMT3A-vorm (DNMT3A2) opgelost in complex met DNMT3L. Ze ontdekten dat DNMT3A gelaagde zelfremming, oftewel autoremming, bevat. Twee lezer-domeinen, PWWP en ADD genaamd, vouwen terug op de katalytische kern van het enzym op een manier die fysiek het deel van het eiwit dat CpG-locaties herkent blokkeert, evenals pockets die normaalchemische merken op histonen voelen. Deze compacte opstelling verhindert dat DNMT3A toegang krijgt tot DNA, waardoor zijn methylatie-activiteit laag blijft totdat de juiste signalen verschijnen.
Histoonsignalen lossen de remmen
Het team legde hun structuur over eerder bekende structuren van DNMT3A en verwante eiwitten gebonden aan histonfragmenten. Deze vergelijking toonde aan dat wanneer histontails bepaalde merken dragen — specifiek niet-gemodificeerde lysine-4 (H3K4me0) en dimethylering op lysine-36 (H3K36me2) — ze concurreren met de interne contacten van DNMT3A. Binding van deze histonmerken wrikt de PWWP- en ADD-domeinen weg van de katalytische kern en van een flexibele lus die CpG-sites herkent. Moleculaire dynamicasimulaties, die eiwitbeweging in de tijd modelleren, lieten zien dat zodra deze interne klemmen losser worden, de CpG-herkenningslus mobieler en toegankelijker wordt, beter gepositioneerd om DNA te binden. In wezen schakelt DNMT3A van een gesloten, rustende vorm naar een meer open, actieve vorm alleen wanneer het een geschikt chromatine-milieu detecteert.
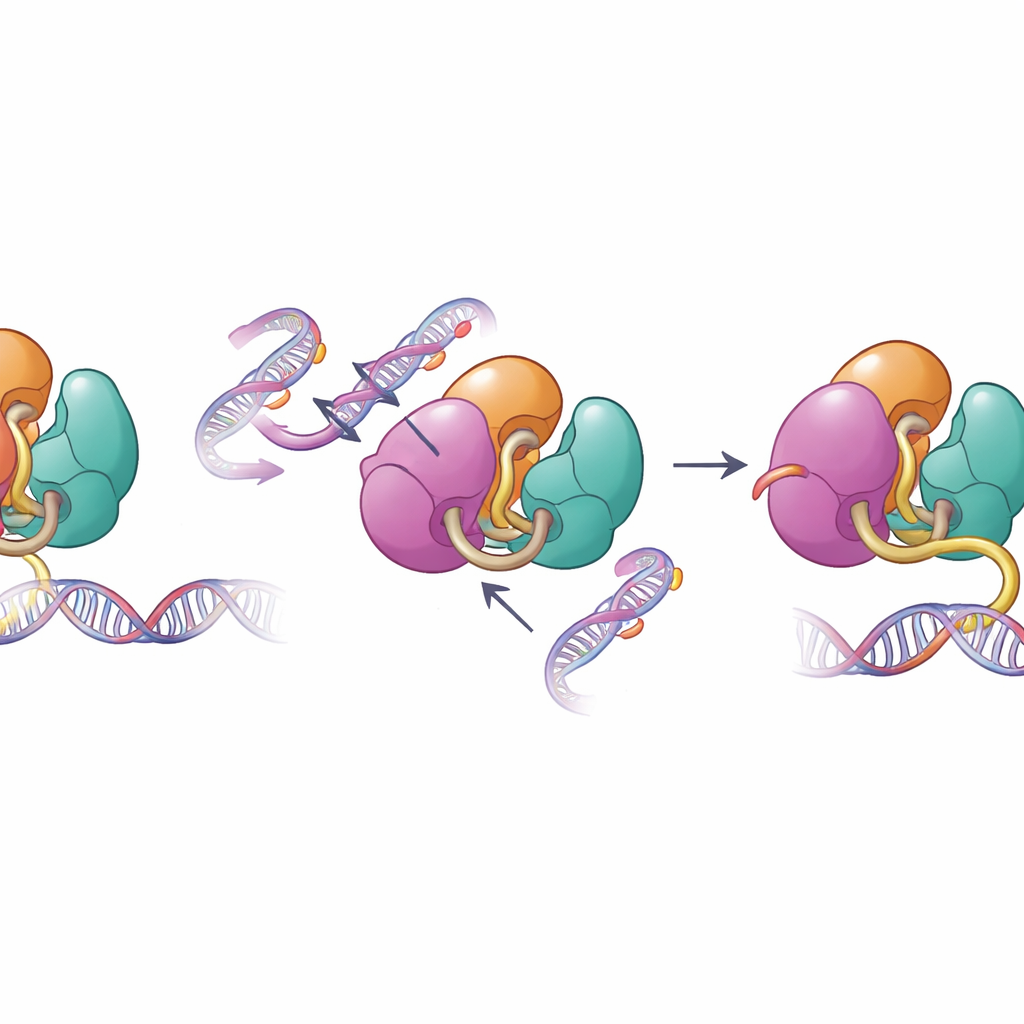
Wanneer structurele waarborgen falen
Dezelfde oppervlakken die autoremming verzorgen, zijn vaak veranderd bij menselijke ziekte. De auteurs onderzochten ziektegerelateerde varianten in DNMT3A die voorkomen bij bloedkankers en ontwikkelingsstoornissen, waaronder mutaties in de PWWP- en ADD-domeinen. Biochemische tests toonden aan dat deze mutaties de interne contacten verzwakken die DNMT3A onder controle houden, waardoor zijn vermogen om DNA te binden en te methyleren in reageerbuisexperimenten toeneemt. Toen het team naar methylatiepatronen keek in muis-stamcellen die een van deze mutaties droegen, vonden ze dat DNMT3A minder responsief werd voor het normale histonsignaal H3K36me2 en begon met het methyleren van delen van het genoom die normaal minder gemarkeerd zouden blijven. Dit verlies aan nauwkeurige targeting draagt bij aan waarom zulke mutaties geassocieerd zijn met wijdverspreide, verkeerd toegepaste DNA-methylatie bij patiënten.
Waarom dit belangrijk is voor de gezondheid
Samenvattend toont de studie DNMT3A als een fijn afgestelde machine waarvan de activiteit wordt gestuurd door geneste lagen van zelfbeperking, die alleen in het juiste chromatine-omgeving worden opgeheven. Door precies in kaart te brengen hoe deze interne remmen werken — en hoe ziekteveroorzakende mutaties ze uitschakelen — levert het werk een structureel stappenplan om abnormale DNA-methylatie bij kanker en ontwikkelingssyndromen te begrijpen. Op de lange termijn kunnen inzichten in deze controlepunten inspanningen sturen om geneesmiddelen te ontwerpen die de juiste DNMT3A-regulatie voorzichtig herstellen, en zo verkeerd aangebrachte DNA-labels corrigeren zonder dit essentiële enzym volledig uit te schakelen.
Bronvermelding: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Trefwoorden: DNA-methylatie, epigenetica, DNMT3A, chromatine-regulatie, kankermutaties