Clear Sky Science · ar
رؤية تركيبية لكبح الذات الهرمي لإنزيم DNMT3A واضطرابه في الأمراض
كيف تميّز الخلايا حمضها النووي
تحمل كل خلية في أجسامنا نفس الحمض النووي، ومع ذلك تتصرف خلايا القلب بشكل مختلف تمامًا عن خلايا الدماغ. إحدى الطرق التي تحقق بها الخلايا هذا الاختلاف هي بوضع وسمات كيميائية دقيقة على الحمض النووي، تساعد في تشغيل الجينات أو إيقافها. تستعرض هذه المقالة كيف يُحفظ إنزيم وسم رئيسي، DNMT3A، تحت رقابة مشددة—وكيف أن تغييرات صغيرة في بنيته يمكن أن توجه هذه الوسمات في اتجاه خاطئ وتساهم في الأمراض البشرية.
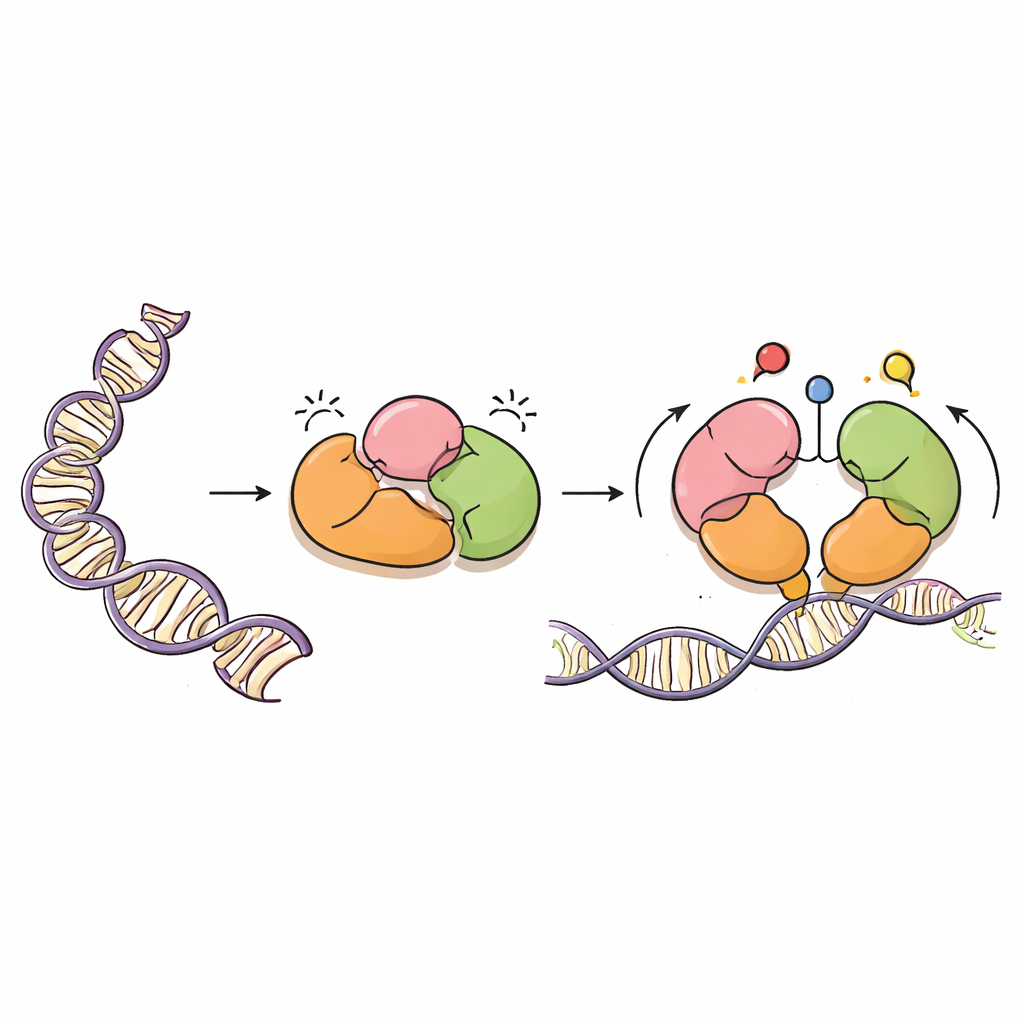
رسام دقيق للحمض النووي
DNMT3A هو إنزيم يضيف مجموعات مثيلة — وسمات كربونية بسيطة — إلى حروف معينة من الحمض النووي، عادة في مواقع تُعرف ثنائيات CpG. هذه الوسمات ضرورية للتطور الطبيعي، ولطبع الجينات الأبوية، وللاستقرار طويل الأمد للجينوم. لكن مثل بخاخ طلاء قوي، يجب توجيه DNMT3A بدقة. يعمل هذا الإنزيم إلى جانب بروتين شريك، DNMT3L، ويحمل عدة مناطق «قارئة» تستشعر البروتينات المجاورة المسماة هستونات، وهي التي تعبئ الحمض النووي في الكروماتين. تساعد هذه المناطق القارئة DNMT3A على معرفة المواضع التي ينبغي أن يعمل فيها وتلك التي يجب أن يظل فيها هادئًا.
فرامل مدمجة داخل الإنزيم
باستخدام المجهر الإلكتروني بالتبريد، حلّل الباحثون البنية الثلاثية الأبعاد لشكل رئيسي من DNMT3A (DNMT3A2) مرتبطًا بـDNMT3L. اكتشفوا أن DNMT3A يحتوي على طبقات من الكبح الذاتي، أو الكبح الذاتي الداخلي. منطقتان قارئتان، تُسمّيان PWWP وADD، تنثنيان على نواة الإنزيم التحفيزية بطريقة تحجب فعليًا الجزء من البروتين الذي يتعرف على مواقع CpG، وكذلك الجيوب التي تستشعر عادة الوسمات الكيميائية على الهستونات. هذا الترتيب المدمج يمنع DNMT3A من الوصول إلى الحمض النووي، ويبقي نشاطه في إضافة الميثيل منخفضًا حتى تظهر الإشارات المناسبة.
إشارات الهستون تفرج عن الفرامل
قام الفريق بمطابقة بنيتهم مع بنى معروفة سابقًا لـDNMT3A وبروتينات ذات صلة مرتبطة بشظايا هستون. أظهرت هذه المقارنة أنه عندما تحمل ذيول الهستون وسمات معينة — وبشكل خاص ليسين-4 غير المعدّل (H3K4me0) وليسين-36 ثنائي الميثيل (H3K36me2) — فإنها تتنافس مع الاتصالات الداخلية في DNMT3A. ارتباط هذه الوسمات الهستونية يزيح منطقتي PWWP وADD بعيدًا عن النواة التحفيزية وعن حلقة مرنة تتعرف على مواقع CpG. كشفت محاكاة الديناميكيات الجزيئية، التي تحاكي حركة البروتين عبر الزمن، أنه بمجرد أن تُرخى هذه المِشابك الداخلية، تصبح حلقة التعرف على CpG أكثر حركة وانكشافًا، مما يجعلها في وضع أفضل للتفاعل مع الحمض النووي. بعبارة أخرى، ينتقل DNMT3A من شكل مغلق وراكد إلى شكل أكثر انفتاحًا ونشاطًا فقط عند استشعاره لبيئة كروماتينية مناسبة.
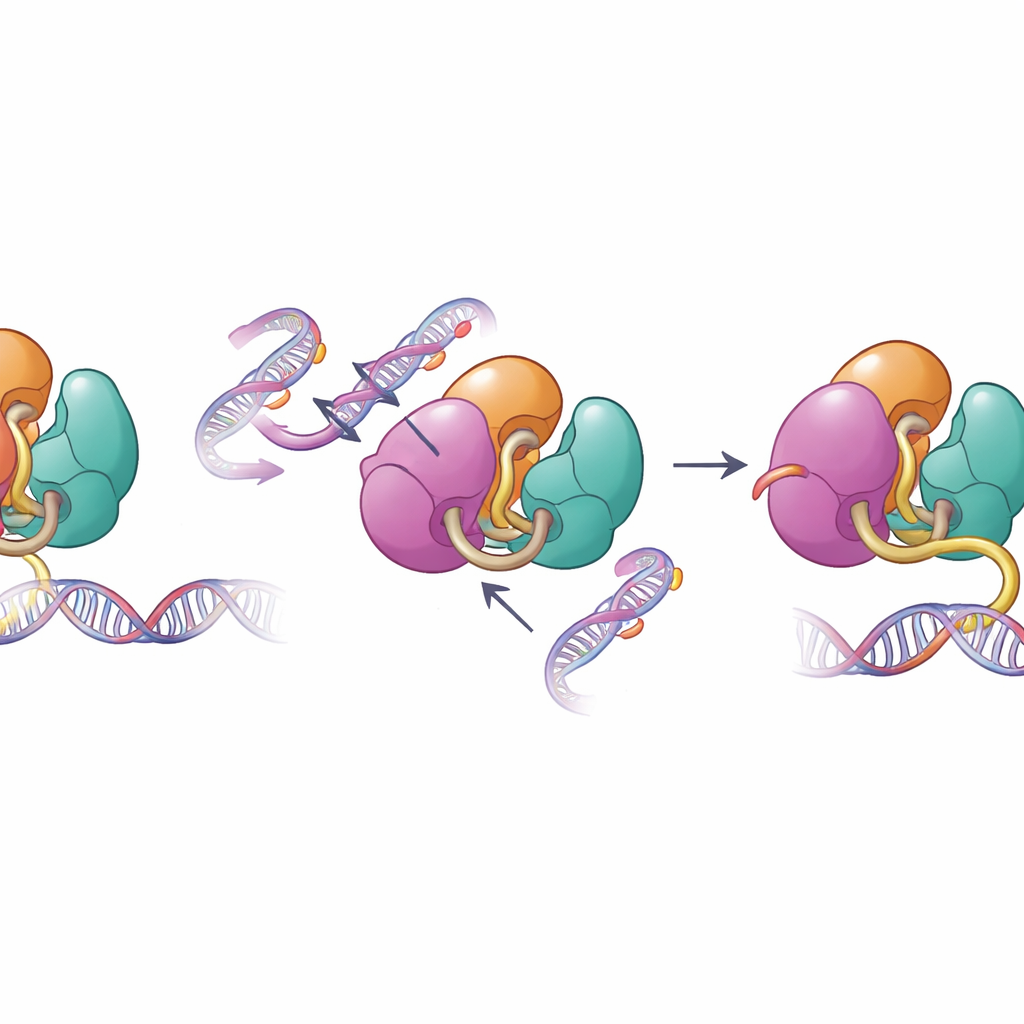
عندما تفشل الضوابط التركيبية
الأسطح نفسها التي تتوسط الكبح الذاتي غالبًا ما تتعرض للتغيير في الأمراض البشرية. فحص الباحثون التغيرات المرتبطة بالأمراض في DNMT3A الموجودة في سرطانات الدم واضطرابات التطور، بما في ذلك طفرات في مناطق PWWP وADD. أظهرت الاختبارات الكيميائية الحيوية أن هذه الطفرات تُضعف الاتصالات الداخلية التي تُبقي DNMT3A تحت السيطرة، مما يعزز قدرته على ربط الحمض النووي وميثلته في تجارب الاختبار المختبري. عندما نظر الفريق إلى أنماط المثيلة في خلايا جذعية فأرية تحمل إحدى هذه الطفرات، وجدوا أن DNMT3A أصبح أقل استجابة للإشارة الهستونية العادية H3K36me2 وبدأ في مثيلة مناطق من الجينوم التي عادةً ما تبقى أقل وسمًا. يساهم هذا الفقد في دقة الاستهداف في تفسير سبب ارتباط مثل هذه الطفرات بمثيلة واسعة وغير مناسبة للحمض النووي لدى المرضى.
لماذا هذا مهم للصحة
بشكل عام، تكشف الدراسة أن DNMT3A آلة دقيقة الضبط تُحكم نشاطها بطبقات متداخلة من الكبح الذاتي، تُفرَج فقط في بيئة كروماتينية مناسبة. من خلال رسم خريطة دقيقة لكيفية عمل هذه الفرامل الداخلية — وكيف تُعطلها الطفرات المسببة للمرض — يوفر العمل مخططًا تركيبيا لفهم المثيلة الشاذة للحمض النووي في السرطان والمتلازمات التنموية. على المدى الطويل، قد تُرشد الرؤى حول نقاط الضبط هذه الجهود لتصميم عقاقير تستعيد بلطف تنظيم DNMT3A الصحيح، مصحّحة الوسمات المطبقة بشكل خاطئ دون إيقاف هذا الإنزيم الأساسي تمامًا.
الاستشهاد: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
الكلمات المفتاحية: مثيلة الحمض النووي, علم فوق الجينات, DNMT3A, تنظيم الكروماتين, طفرات السرطان