Clear Sky Science · sv
Strukturell inblick i hierarkisk DNMT3A-autoinhibering och dess dysreglering vid sjukdom
Hur celler märker sitt DNA
Varje cell i vår kropp bär på samma DNA, ändå beter sig hjärtceller mycket annorlunda än hjärnceller. Ett sätt celler åstadkommer detta är genom att placera små kemiska markörer på DNA, vilket hjälper till att slå gener på eller av. Den här artikeln undersöker hur ett nyckelenzym för märkning, DNMT3A, hålls noga under kontroll — och hur små förändringar i dess struktur kan leda till felaktig märkning och bidra till mänsklig sjukdom.
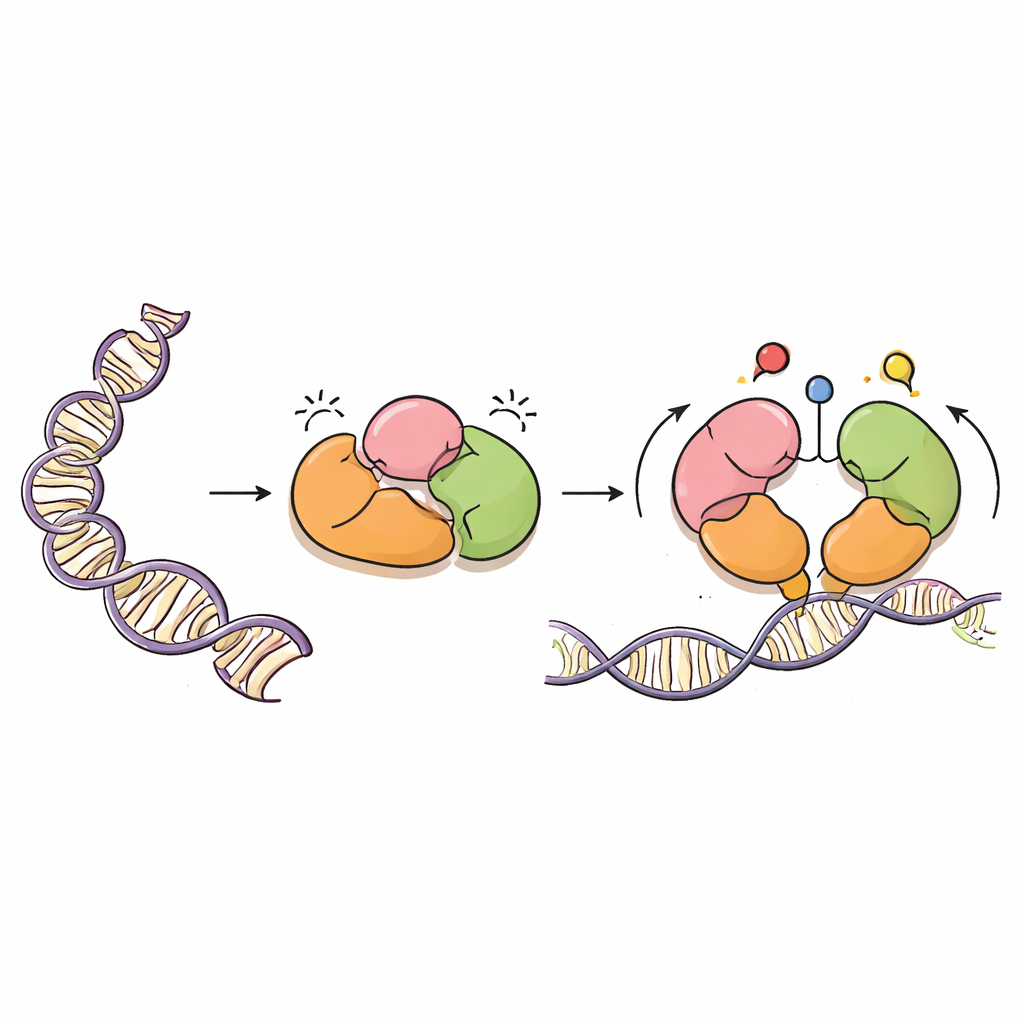
En försiktig DNA-målare
DNMT3A är ett enzym som lägger till metylgrupper — enkla kolbaserade märken — på specifika DNA-bokstäver, vanligen vid platser som kallas CpG-dinukleotider. Dessa märken är viktiga för normal utveckling, föräldragenuppmärkning (imprinting) och den långsiktiga stabiliteten i vårt genom. Men precis som en kraftfull färgspruta måste DNMT3A styras noggrant. Det samarbetar med ett partnerprotein, DNMT3L, och har flera ”läsar”-regioner som känner av närliggande proteiner kallade histoner, som paketerar DNA till kromatin. Dessa läsarregioner hjälper DNMT3A att veta var det bör verka och var det ska förbli tyst.
Inbyggda bromsar i enzymet
Med kryo-elektronmikroskopi löste författarna tredimensionella strukturen av en viktig DNMT3A-form (DNMT3A2) bunden till DNMT3L. De upptäckte att DNMT3A innehåller lager av självbegränsning, eller autoinhibering. Två läsarregioner, kallade PWWP och ADD, viker tillbaka mot enzymets katalytiska kärna på ett sätt som fysiskt blockerar den del av proteinet som känner igen CpG-platser, liksom fickor som normalt känner av kemiska märken på histoner. Denna kompakta uppställning hindrar DNMT3A från att komma åt DNA och håller dess metyleringsaktivitet låg tills rätt signaler uppträder.
Histonsignaler släpper bromsarna
Teamet överlagrade sin struktur med tidigare kända strukturer av DNMT3A och närbesläktade proteiner bundna till histonfragment. Jämförelsen visade att när histonstjärtar bär vissa märken — specifikt omodifierad lysin-4 (H3K4me0) och dimetylerad lysin-36 (H3K36me2) — konkurrerar de med DNMT3A:s interna kontakter. Bindning av dessa histonmärken bänder loss PWWP- och ADD-regionerna från den katalytiska kärnan och från en flexibel slinga som känner igen CpG-platser. Molekyldynamiksimuleringar, som modellerar proteinrörelse över tid, visade att när dessa interna klämmor lossnar blir CpG-recognitionsslingan mer rörlig och exponerad, bättre positionerad för att engagera DNA. I praktiken växlar DNMT3A från en sluten, vilande form till en mer öppen, aktiv form först när den känner av en lämplig kromatinmiljö.
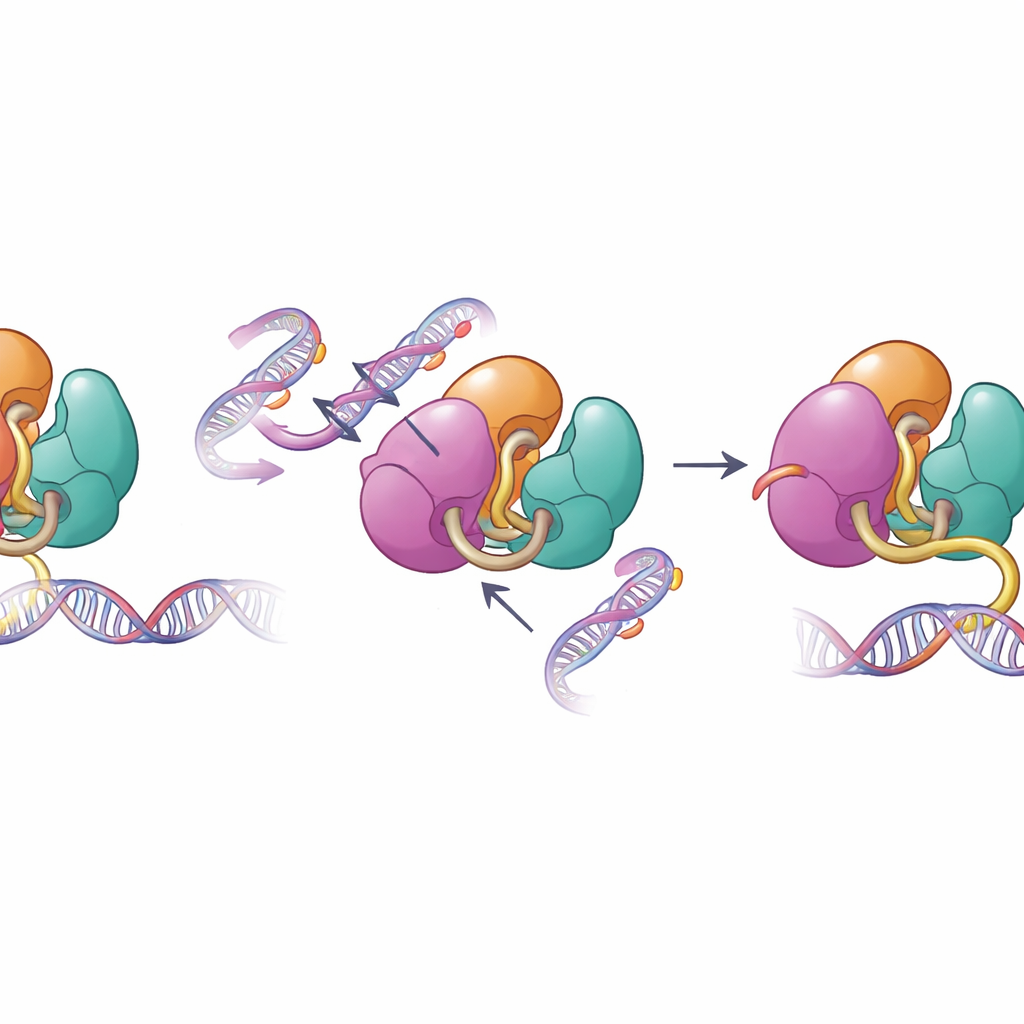
När strukturella skyddsmekanismer misslyckas
Samma ytor som medierar autoinhibering ändras ofta vid mänsklig sjukdom. Författarna undersökte sjukdomsassocierade förändringar i DNMT3A som hittats i blodcancer och utvecklingsstörningar, inklusive mutationer i PWWP- och ADD-regionerna. Biokemiska tester visade att dessa mutationer försvagar de interna kontakterna som håller DNMT3A i schack, vilket ökar dess förmåga att binda DNA och metylera det i provrörsexperiment. När teamet studerade metyleringsmönster i musstamceller som bar en av dessa mutationer fann de att DNMT3A blev mindre lyhört för den normala histonsignalen H3K36me2 och började metylera områden av genomet som vanligtvis skulle förbli mindre märkta. Denna förlust av riktprecision hjälper till att förklara varför sådana mutationer är kopplade till utbredd, felplacerad DNA-metylering hos patienter.
Varför detta spelar roll för hälsan
Sammanfattningsvis visar studien att DNMT3A är en fint avvägd maskin vars aktivitet styrs av inbäddade lager av självkontroll, frigjorda endast i rätt kromatinmiljö. Genom att kartlägga exakt hur dessa interna bromsar fungerar — och hur sjukdomsframkallande mutationer inaktiverar dem — ger arbetet en strukturell ritning för att förstå onormal DNA-metylering vid cancer och utvecklingssyndrom. I längden kan insikter om dessa kontrollpunkter vägleda ansträngningar att utforma läkemedel som varsamt återställer korrekt DNMT3A-reglering och korrigerar felplacerade DNA-märken utan att helt stänga av detta viktiga enzym.
Citering: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Nyckelord: DNA-metylering, epigenetik, DNMT3A, kromatinreglering, cancermutationer