Clear Sky Science · ru
Структурное понимание иерархической аутоингибии DNMT3A и её нарушение при заболеваниях
Как клетки помечают свою ДНК
Каждая клетка нашего тела несёт одинаковую ДНК, но клетки сердца ведут себя совсем иначе, чем клетки мозга. Один из способов, которым клетки добиваются этого различия, — нанесение крошечных химических меток на ДНК, что помогает включать или выключать гены. В этой статье рассматривается, как ключевой фермент, наносящий такие метки — DNMT3A — удерживается под строгим контролем и как незначительные изменения его структуры могут исказить распределение меток и способствовать развитию заболеваний у человека.
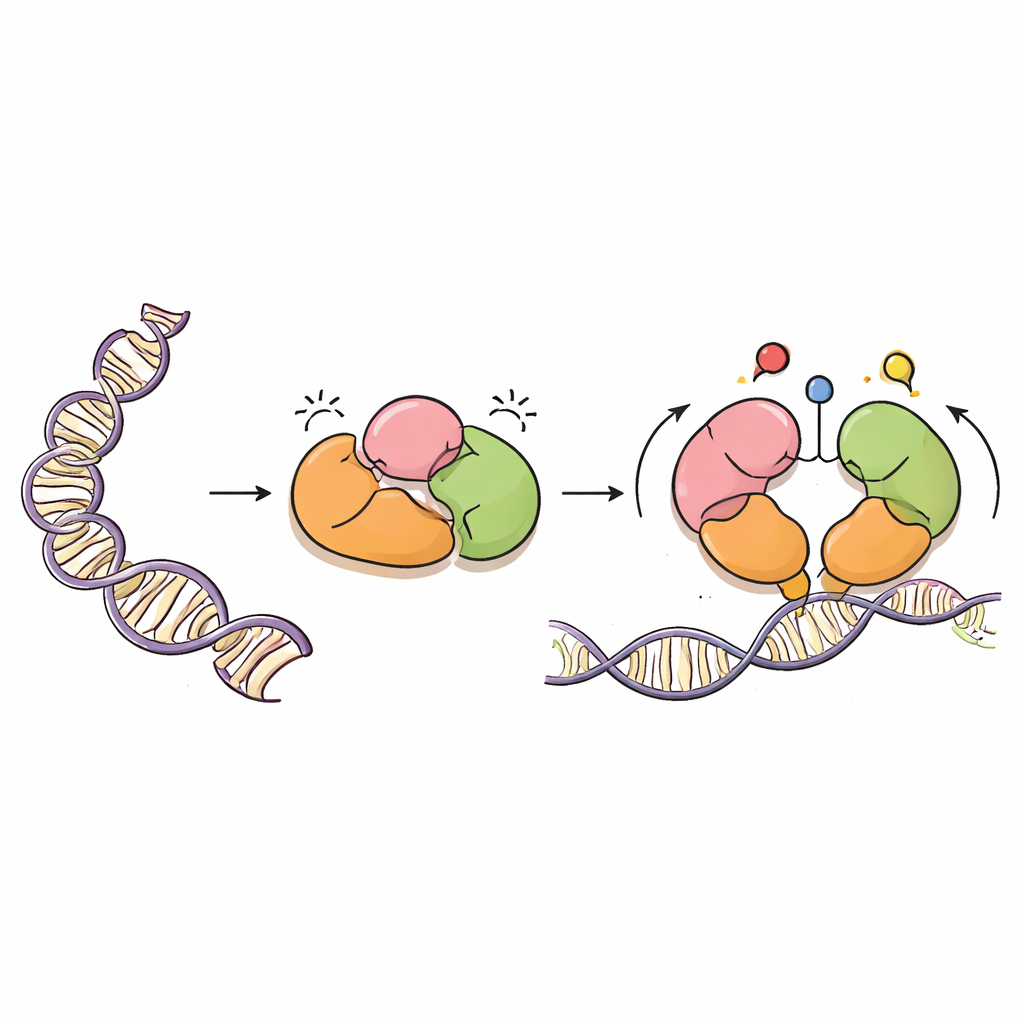
Точный «маляр» ДНК
DNMT3A — это фермент, добавляющий метильные группы — простые углеродные метки — к определённым буквам ДНК, обычно в местах, называемых CpG-динуклеотидами. Эти метки необходимы для нормального развития, материнской/отцовской отпечатанности генов и долгосрочной стабильности генома. Но, как мощный краскораспылитель, DNMT3A должен направляться очень точно. Он работает вместе с партнёром DNMT3L и содержит несколько «ридерных» областей, которые ощущают соседние белки — гистоны, упаковывающие ДНК в хроматин. Эти ридеры помогают DNMT3A понимать, где ему следует работать, а где оставаться пассивным.
Встроенные тормоза внутри фермента
С помощью крио-электронной микроскопии авторы определили трёхмерную структуру основной формы DNMT3A (DNMT3A2) в комплексе с DNMT3L. Они обнаружили, что у DNMT3A существуют многослойные собственные тормоза, или аутоингибиция. Две ридерные области, называемые PWWP и ADD, складываются обратно на каталитическое ядро фермента так, что физически блокируют участок белка, распознающий CpG-сайты, а также карманы, которые обычно чувствуют химические метки на гистонах. Такая компактная организация препятствует доступу DNMT3A к ДНК, удерживая его метилирующую активность на низком уровне до появления соответствующих сигналов.
Сигналы гистонов снимают тормоза
Команда наложила полученную структуру на ранее известные структуры DNMT3A и родственных белков, связанных с фрагментами гистонов. Сравнение показало, что когда хвосты гистонов несут определённые метки — в частности немодифицированную лизин-4 (H3K4me0) и диметилированный лизин-36 (H3K36me2) — они конкурируют с внутренними контактами DNMT3A. Связывание этих гистоновых меток отодвигает области PWWP и ADD от каталитического ядра и от гибкой петли, распознающей CpG-сайты. Молекулярно-динамические симуляции, моделирующие движение белка во времени, показали, что после ослабления этих внутренних зажимов петля распознавания CpG становится более подвижной и доступной, лучше ориентированной для взаимодействия с ДНК. По сути, DNMT3A переходит из закрытой, «спящей» формы в более открытую, активную форму только когда он ощущает подходящую среду хроматина.
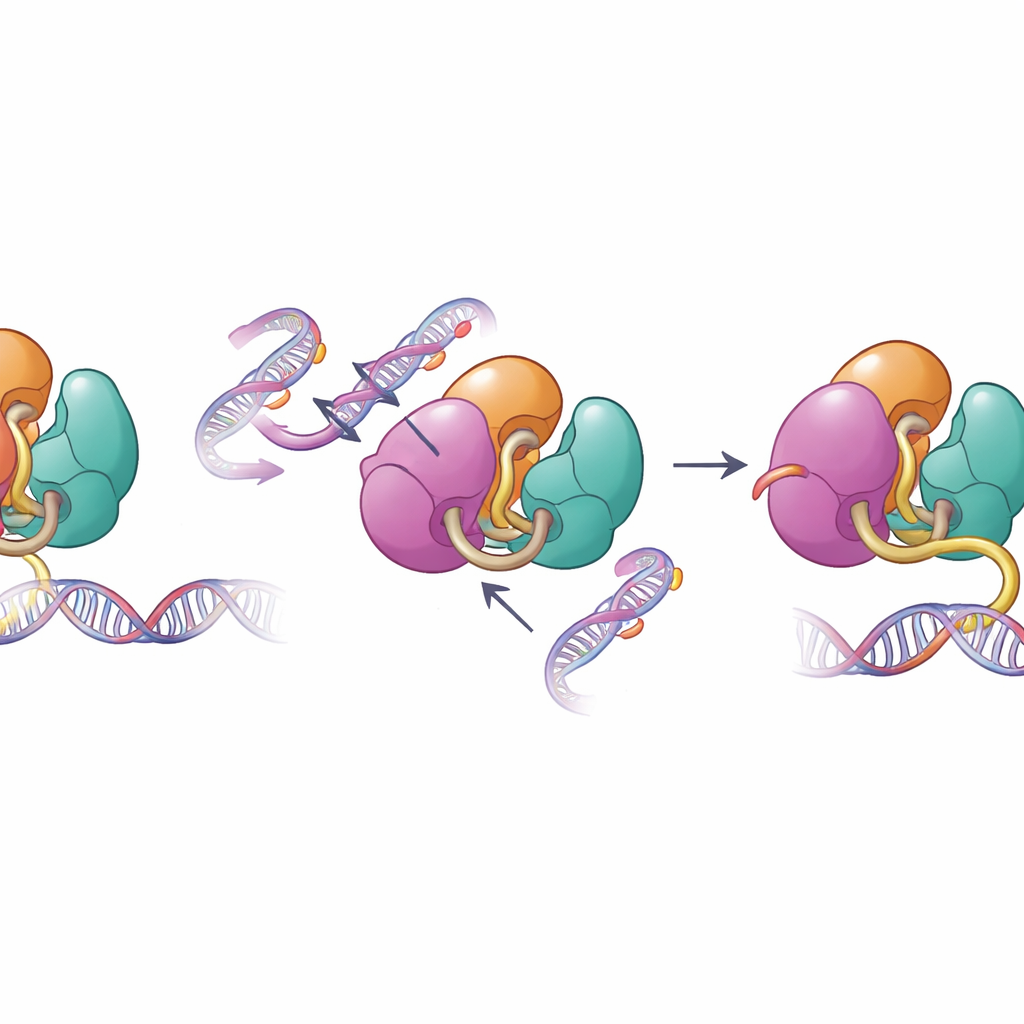
Когда структурные предохранители проваливаются
Те же поверхности, которые обеспечивают аутоингибицию, часто изменяются при человеческих заболеваниях. Авторы изучили изменения DNMT3A, связанные с болезнями крови и нарушениями развития, включая мутации в областях PWWP и ADD. Биохимические тесты показали, что эти мутации ослабляют внутренние контакты, которые удерживают DNMT3A под контролем, повышая его способность связываться с ДНК и метилировать её в пробирочных экспериментах. При анализе паттернов метилирования в стволовых клетках мыши, несущих одну из таких мутаций, выяснилось, что DNMT3A стал менее отзывчив к нормальному гистоновому сигналу H3K36me2 и начал метилировать участки генома, которые обычно остаются менее помеченными. Эта потеря точности нацеливания помогает объяснить, почему такие мутации связаны с распространённым, неправильным метилированием ДНК у пациентов.
Почему это важно для здоровья
В целом исследование показывает DNMT3A как тонко настроенную «машину», чья активность регулируется вложенными слоями самоограничения, снимаемыми лишь в подходящем хроматиновом контексте. Точное картирование того, как эти внутренние тормоза работают — и как мутации, вызывающие болезни, их деактивируют — даёт структурный план для понимания аномального метилирования ДНК при раке и синдромах развития. В перспективе знания об этих контрольных точках могут помочь в разработке лекарств, которые мягко восстанавливают надлежащую регуляцию DNMT3A, корректируя неправильно нанесённые метки ДНК, не отключая полностью этот жизненно важный фермент.
Цитирование: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Ключевые слова: метилирование ДНК, эпигенетика, DNMT3A, регуляция хроматина, мутации при раке