Clear Sky Science · he
תובנה מבנית על אוטו-עיכוב היררכי של DNMT3A והפרתו במחלות
איך התאים מסמנים את ה‑DNA שלהם
כל תא בגופנו נושא את אותו ה‑DNA, ובכל זאת תאי לב מתנהגים בצורה שונה מאוד מתאי מוח. אחת הדרכים בהן תאים משיגים את הגיוון הזה היא על‑ידי הצמדת תגיות כימיות זעירות ל‑DNA, שמסייעות להפעיל או לכבות גנים. מאמר זה בוחן כיצד אנזים מפתח שמצמיד תגיות אלה, DNMT3A, נשלט בקפדנות — וכיצד שינויים קלים במבנה שלו עלולים להסיט את המידול של התגים ולתרום למחלות אנושיות.
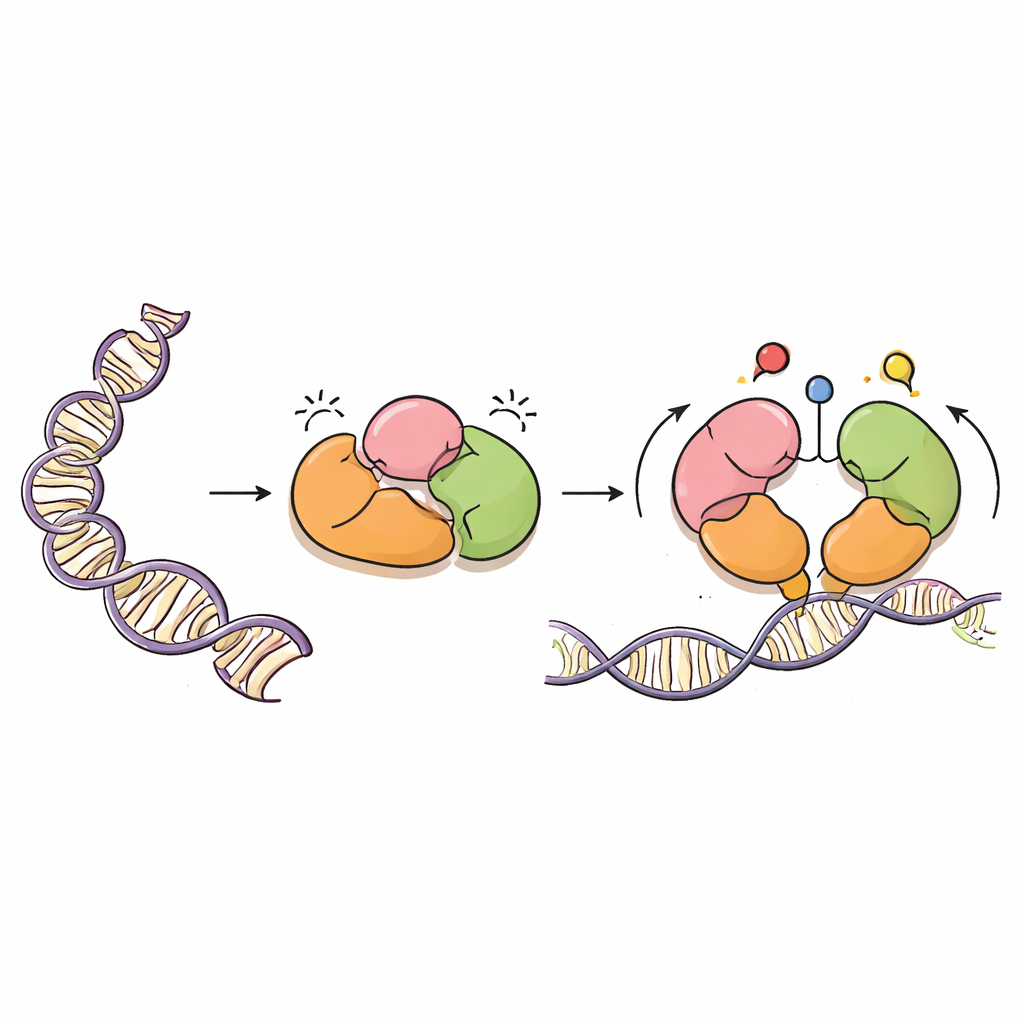
צייר זהיר של ה‑DNA
DNMT3A הוא אנזים שמוסיף קבוצות מתיל — סימנים פשוטים מבוססי פחמן — לאותיות ספציפיות ב‑DNA, בדרך כלל באתרים הנקראים דינוקלאוטידים CpG. סימנים אלה חיוניים להתפתחות תקינה, להטבעת גנים הוריים וליציבות ארוכת הטווח של הגנום שלנו. אך בדומה למרסס צבע עוצמתי, יש לכוון את DNMT3A במדויק. הוא פועל לצד חלבון שותף, DNMT3L, ונושא כמה אזורי "קורא" שמרגישים חלבונים סמוכים הקרויים היסטונים, המארזים את ה‑DNA לתוך כרומטין. אזורי הקורא האלה מסייעים ל‑DNMT3A לדעת היכן עליו לפעול והיכן עליו להישאר שקט.
בלמים מובנים בתוך האנזים
באמצעות מיקרוסקופיה קריואלקטרונית, החוקרים פתרו את המבנה התלת‑ממדי של צורת DNMT3A מרכזית (DNMT3A2) כאשר היא קשורה ל‑DNMT3L. הם גילו של‑DNMT3A יש רמות של אוטו‑עיכוב, סוג של בלימה עצמית בשכבות. שני אזורי קורא, הנקראים PWWP ו‑ADD, מתקפלים חזרה אל הליבה הקטליטית של האנזים באופן שמחסום פיזית את החלק בחלבון שמזהה את אתרי CpG, וכן כיסים שלרוב מרגישים סימנים כימיים על ההיסטונים. סידור קומפקטי זה מונע מ‑DNMT3A לגשת ל‑DNA, ומשמר את פעילות המתילציה שלו נמוכה עד שיופיעו האיתותים המתאימים.
אותות היסטון משחררים את הבלמים
הקבוצה הכניסה את המבנה שלהם בהשוואה למבנים ידועים קודמים של DNMT3A וחלבונים קרובים הקשורים לפירגמנטים של היסטונים. ההשוואה הראתה שכאשר זנבות ההיסטון נושאים סימנים מסוימים — במיוחד ליזין‑4 לא מעובד (H3K4me0) וליזין‑36 בי‑מתילציה (H3K36me2) — הם מתחרים בקשרים הפנימיים של DNMT3A. קשירת סימני ההיסטון הללו מפשיטה את אזורי ה‑PWWP וה‑ADD מהליבה הקטליטית ומהלולאה הגמישה שמזהה את אתרי ה‑CpG. סימולציות של דינמיקת מולקולות, המאפשרות לדמות תנועת חלבון לאורך זמן, הראו כי ברגע שהקלאמפיים הפנימיים אלה נרפים, הלולאה שמזהה CpG נעשית ניידת ומחשיפה יותר, וממוקמת טוב יותר להתחבר ל‑DNA. במילים אחרות, DNMT3A עובר מצורה סגורה ונחה לצורה פתוחה ופעילה רק כשהוא חווה סביבה כרומטינית מתאימה.
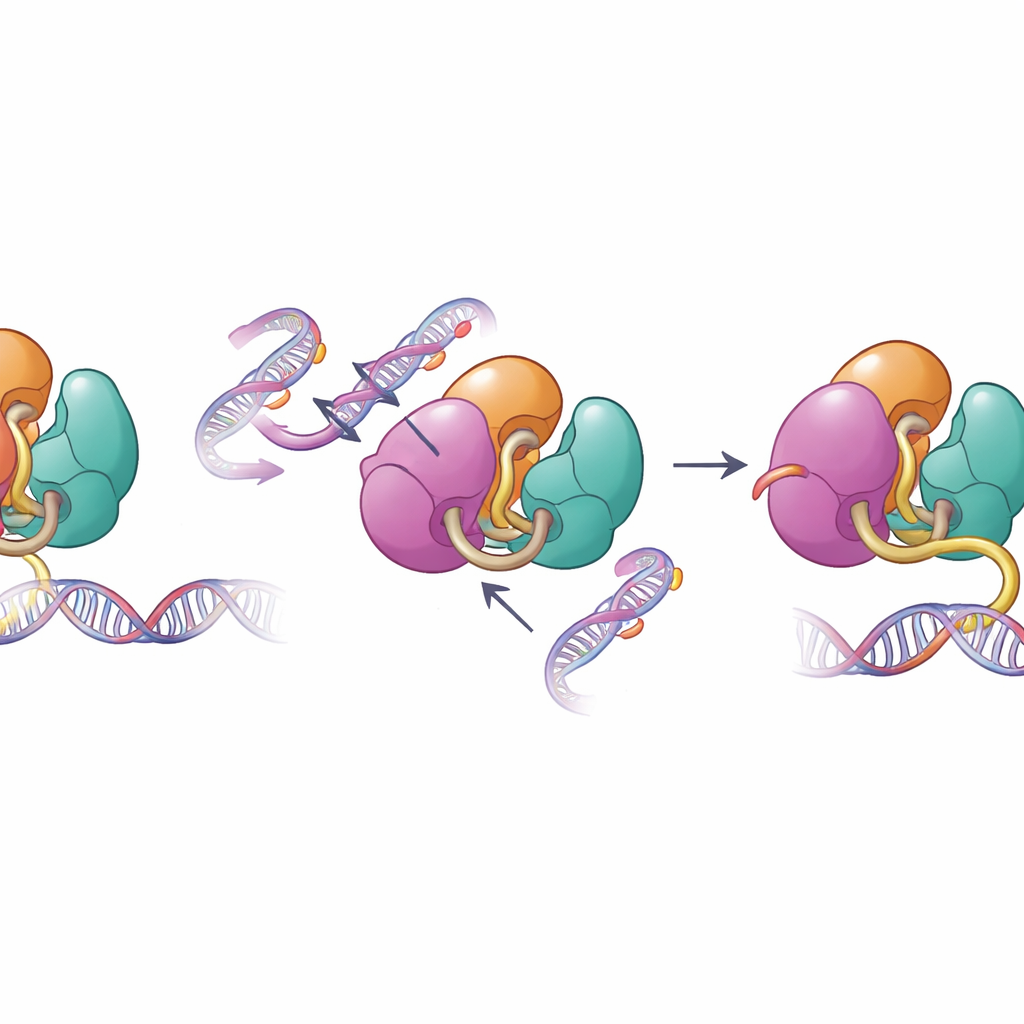
כשמנגנוני ההגנה המבניים נכשלים
אותן משטחים שמתווכים את האוטו‑עיכוב משתנים לעתים קרובות במחלות אנושיות. החוקרים בחנו שינויים ב‑DNMT3A המקושרים למחלות בדם והפרעות בהתפתחות, כולל מוטציות באזורי PWWP ו‑ADD. בדיקות ביוכימיות הראו שמוטציות אלה מחלישות את הקשרים הפנימיים שמקבעים את DNMT3A, מה שמגביר את יכולתו להיקשר ל‑DNA ולבצע מתילציה בניסויי מבחנה. כשהצוות בדק דפוסי מתילציה בתאי גזע עכבריים שנשאו אחת מהמוטציות הללו, הם מצאו ש‑DNMT3A הפך לפחות רגיש לאות ההיסטון הנורמלי H3K36me2 והחל למתיל אזורים של הגנום שבדרך כלל היו נשארים פחות מסומנים. איבוד הדיוק ביעד הזה מסייע להסביר מדוע מוטציות כאלה מקושרות למתילציה נרחבת ומושמת במקומות שגויים בחולים.
מדוע זה חשוב לבריאות
בסך הכל, המחקר מגדיר את DNMT3A כמכונה מכוּננת בעדינות, שפעילותה נשלטת על‑ידי שכבות משולשות של עיכוב עצמי, המשוחררות רק בהקשר הכרומטיני הנכון. על‑ידי מיפוי מדויק של אופן פעולת הבלמים הפנימיים — וכיצד מוטציות מחוללות מחלות מנטרלות אותם — העבודה מספקת שרטוט מבני להבנת מתילציה חריגה של DNA בסרטן ובתסמונות התפתחותיות. בטווח הארוך, תובנות על נקודות בקרה אלה עשויות לסייע בפיתוח תרופות שישיבו בעדינות את ויסות DNMT3A, ובכך לתקן סימני DNA שיישמו בעוולה מבלי לכבות לחלוטין את האנזים החיוני הזה.
ציטוט: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
מילות מפתח: מתילציה של DNA, אפיגנטיקה, DNMT3A, ויסות כרומטין, מוטציות סרטניות