Clear Sky Science · pl
Wgląd strukturalny w hierarchiczną autoinhibicję DNMT3A i jej zaburzenia w chorobie
Jak komórki oznaczają swoje DNA
Każda komórka w naszym ciele nosi to samo DNA, a mimo to komórki serca zachowują się zupełnie inaczej niż komórki mózgu. Jednym ze sposobów osiągania tej różnorodności jest umieszczanie drobnych chemicznych znaczników na DNA, co pomaga włącząć lub wyłączyć geny. Ten artykuł opisuje, jak kluczowy enzym znakujący, DNMT3A, jest ściśle kontrolowany — oraz jak drobne zmiany jego struktury mogą skierować te znaczniki nie tam, gdzie trzeba, i przyczynić się do chorób u ludzi.
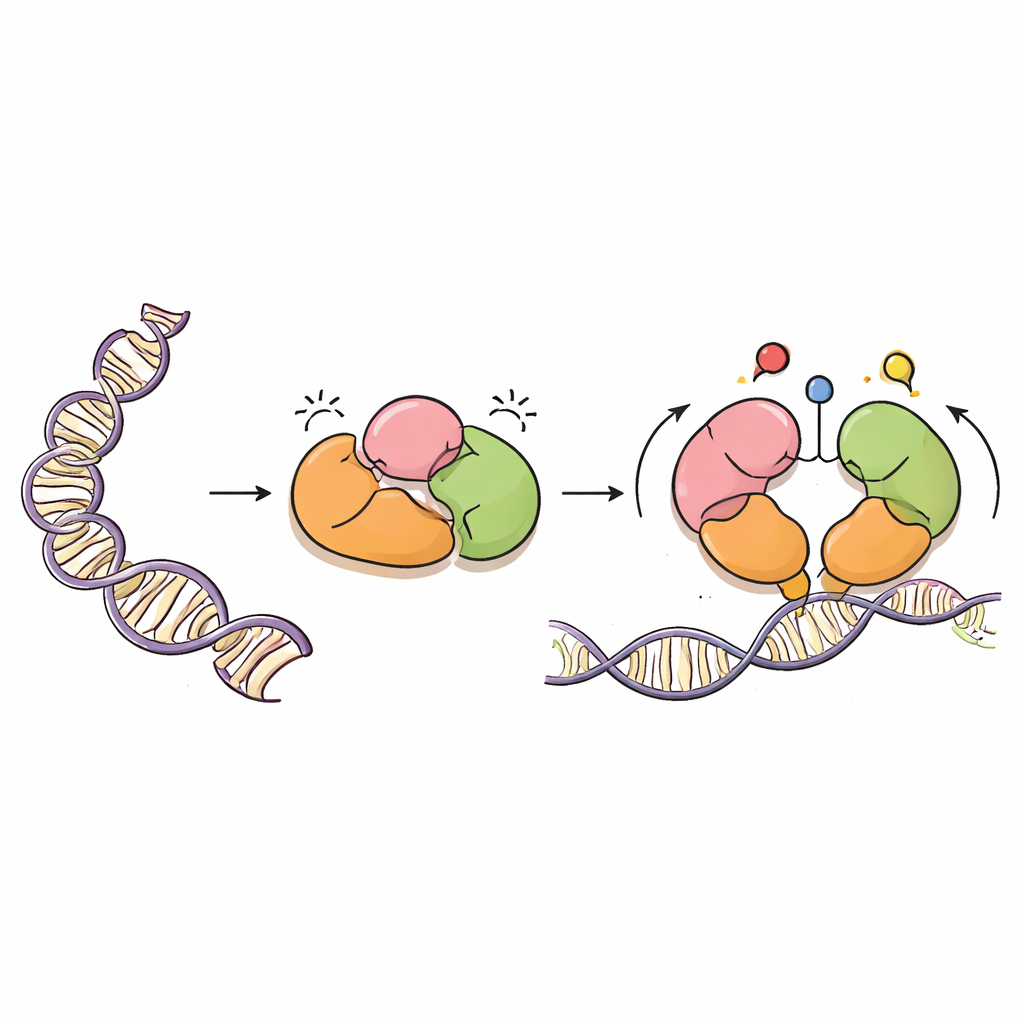
Precyzyjny malarz DNA
DNMT3A to enzym dodający grupy metylowe — proste węglowe znaczniki — do określonych liter DNA, zwykle w miejscach zwanych dinukleotydami CpG. Te znaki są niezbędne dla prawidłowego rozwoju, imprintingu genów rodzicielskich i długotrwałej stabilności genomu. Ale podobnie jak potężny pistolet natryskowy, DNMT3A musi być precyzyjnie ukierunkowany. Działa razem z białkiem partnerem, DNMT3L, i posiada kilka regionów „czytających”, które wyczuwają pobliskie białka zwane histonami, w które DNA jest zapakowane w chromatynę. Te regiony pomagają DNMT3A rozpoznać, gdzie powinien działać, a gdzie ma pozostać w spoczynku.
Wbudowane hamulce w enzymie
Autorzy, używając krioelektronowego mikroskopu, rozwiązali trójwymiarową strukturę głównej formy DNMT3A (DNMT3A2) w kompleksie z DNMT3L. Odkryli, że DNMT3A zawiera warstwową autoinhibicję, czyli samohamulące mechanizmy. Dwa regiony czytające, zwane PWWP i ADD, składają się z powrotem na rdzeń katalityczny enzymu w sposób, który fizycznie blokuje część białka rozpoznającą miejsca CpG, jak również kieszenie, które normalnie wyczuwają chemiczne modyfikacje histonów. Ta zwarta aranżacja uniemożliwia DNMT3A dostęp do DNA, utrzymując jego aktywność metylującą na niskim poziomie, dopóki nie pojawią się odpowiednie sygnały.
Sygnały histonowe zwalniają hamulce
Zespół nałożył swoją strukturę na wcześniej znane struktury DNMT3A i powiązanych białek w kompleksie z fragmentami histonów. Porównanie to pokazało, że gdy ogony histonowe niosą określone znaczniki — w szczególności niezmodyfikowaną lizynę 4 (H3K4me0) i dimetylowaną lizynę 36 (H3K36me2) — konkurują one z wewnętrznymi kontaktami DNMT3A. Wiązanie tych znaków histonowych podważa regiony PWWP i ADD, odsuwając je od rdzenia katalitycznego i od elastycznej pętli rozpoznającej miejsca CpG. Symulacje dynamiki molekularnej, modelujące ruch białka w czasie, wykazały, że gdy te wewnętrzne zaciski zostaną poluzowane, pętla rozpoznająca CpG staje się bardziej ruchoma i odsłonięta, lepiej przygotowana do związania DNA. W istocie DNMT3A przełącza się z zamkniętej, spoczynkowej konformacji do bardziej otwartej, aktywnej konformacji dopiero wtedy, gdy wykryje odpowiednie środowisko chromatynowe.
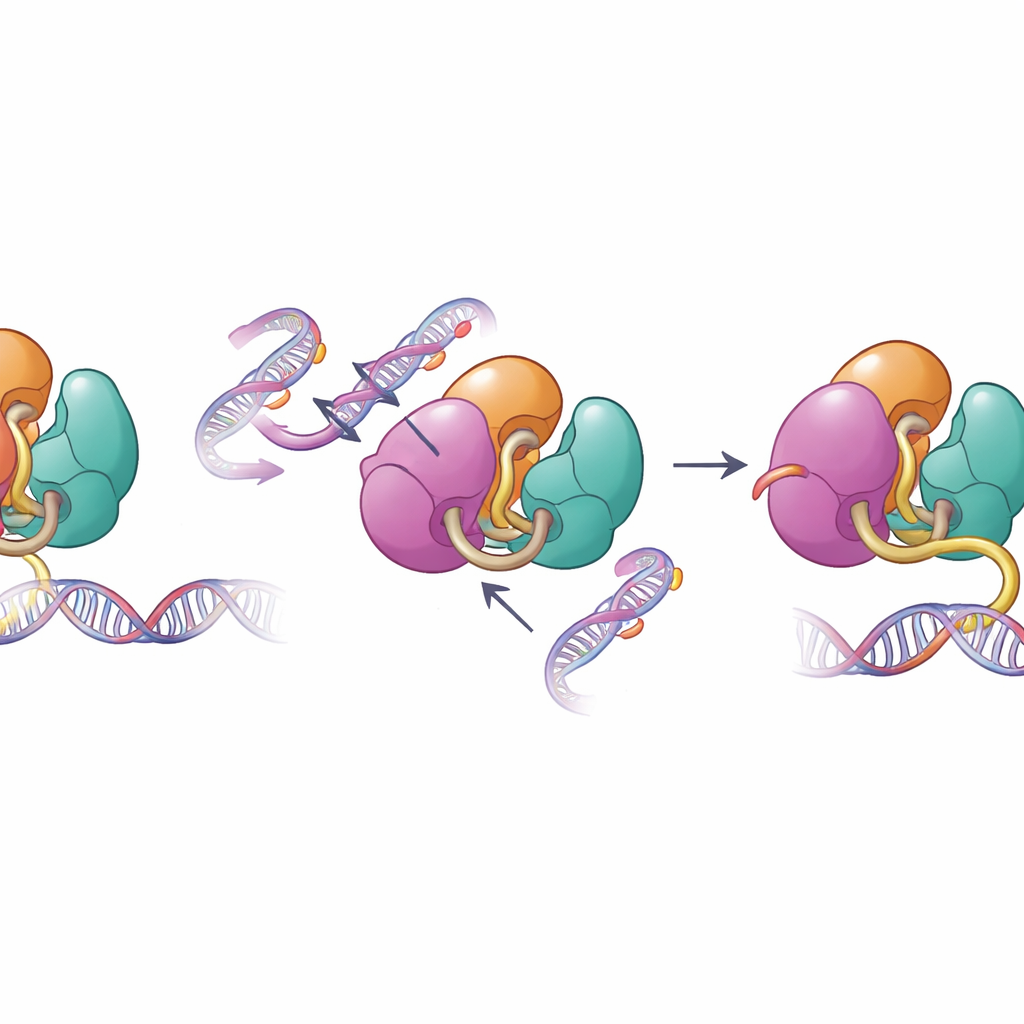
Gdy zabezpieczenia strukturalne zawodzą
Te same powierzchnie, które pośredniczą w autoinhibicji, są często zmieniane w chorobach ludzkich. Autorzy przeanalizowali zmiany związane z chorobami w DNMT3A występujące w nowotworach krwi i zaburzeniach rozwojowych, w tym mutacje w regionach PWWP i ADD. Testy biochemiczne wykazały, że te mutacje osłabiają wewnętrzne kontakty utrzymujące DNMT3A w ryzach, zwiększając jego zdolność do wiązania DNA i metylacji w eksperymentach in vitro. Gdy zespół przyjrzał się wzorom metylacji w komórkach macierzystych myszy niosących jedną z tych mutacji, stwierdzili, że DNMT3A stał się mniej wrażliwy na normalny sygnał histonowy H3K36me2 i zaczął metylować odcinki genomu, które zwykle pozostają mniej oznaczone. Ta utrata precyzji celowania pomaga wyjaśnić, dlaczego takie mutacje wiążą się z rozległą, nieprawidłową metylacją DNA u pacjentów.
Dlaczego to ma znaczenie dla zdrowia
Podsumowując, badanie ujawnia DNMT3A jako precyzyjnie wyregulowaną maszynę, której aktywność rządzona jest przez zagnieżdżone warstwy samohamowania, uwalniane tylko w odpowiednim kontekście chromatynowym. Mapując dokładnie, jak działają te wewnętrzne hamulce — i jak mutacje wywołujące choroby je dezaktywują — praca dostarcza strukturalnej mapy do zrozumienia nieprawidłowej metylacji DNA w nowotworach i zespołach rozwojowych. W dłuższej perspektywie wgląd w te punkty kontrolne może nakierować wysiłki na opracowanie leków, które delikatnie przywrócą właściwą regulację DNMT3A, korygując błędnie naniesione znaczniki DNA bez całkowitego wyłączania tego niezbędnego enzymu.
Cytowanie: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Słowa kluczowe: metylacja DNA, epigenetyka, DNMT3A, regulacja chromatyny, mutacje nowotworowe