Clear Sky Science · es
Perspectiva estructural sobre la autoinhibición jerárquica de DNMT3A y su desregulación en enfermedad
Cómo las células marcan su ADN
Cada célula de nuestro cuerpo porta el mismo ADN, sin embargo las células del corazón actúan de forma muy distinta a las del cerebro. Una manera en que las células logran esto es colocando diminutas etiquetas químicas en el ADN, que ayudan a encender o apagar genes. Este artículo examina cómo una enzima clave para etiquetar, DNMT3A, se mantiene bajo estricto control —y cómo pequeños cambios en su estructura pueden desviar estas marcas y contribuir a enfermedades humanas.
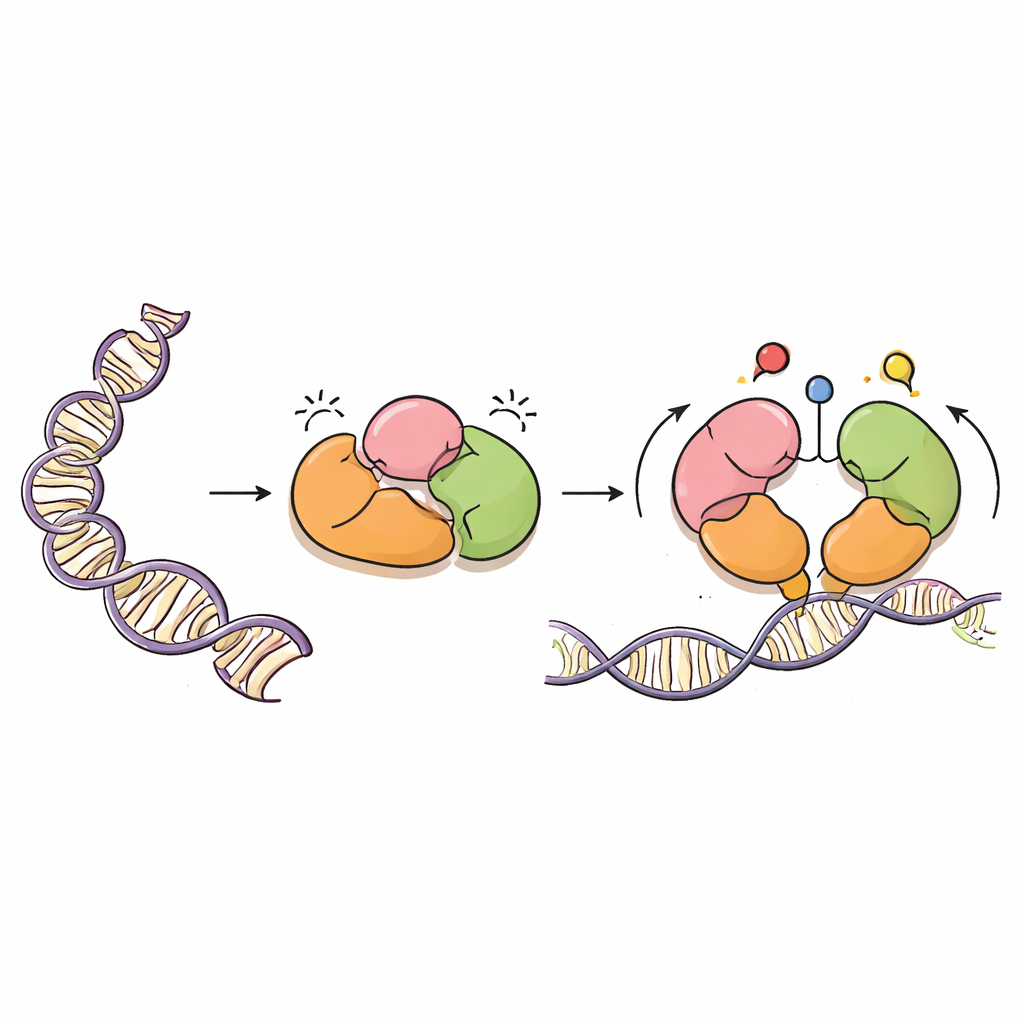
Un pintor cuidadoso del ADN
DNMT3A es una enzima que añade grupos metilo —marcas simples basadas en carbono— a letras específicas del ADN, por lo general en sitios llamados dinucleótidos CpG. Estas marcas son vitales para el desarrollo normal, la impronta de genes parentales y la estabilidad a largo plazo de nuestros genomas. Pero, como un potente pulverizador de pintura, DNMT3A debe estar guiado con precisión. Funciona junto a una proteína compañera, DNMT3L, y posee varias regiones “lectoras” que detectan proteínas próximas llamadas histonas, que empaquetan el ADN en cromatina. Estas regiones lectoras ayudan a DNMT3A a saber dónde debe actuar y dónde debe permanecer silenciosa.
Frenos integrados dentro de la enzima
Mediante criomicroscopía electrónica, los autores resolvieron la estructura tridimensional de una forma mayor de DNMT3A (DNMT3A2) unida a DNMT3L. Descubrieron que DNMT3A contiene frenos internos en capas, es decir, autoinhibición. Dos regiones lectoras, llamadas PWWP y ADD, se pliegan sobre el núcleo catalítico de la enzima de una manera que bloquea físicamente la parte de la proteína que reconoce los sitios CpG, así como bolsillos que normalmente detectan marcas químicas en las histonas. Esta disposición compacta impide que DNMT3A acceda al ADN, manteniendo su actividad metilante baja hasta que aparecen las señales adecuadas.
Señales de histonas que liberan los frenos
El equipo superpuso su estructura con estructuras previamente conocidas de DNMT3A y proteínas relacionadas unidas a fragmentos de histonas. Esta comparación mostró que cuando las colas de histona llevan ciertas marcas —específicamente lisina-4 no modificada (H3K4me0) y lisina-36 dimetilada (H3K36me2)— compiten con los contactos internos de DNMT3A. La unión de estas marcas de histona separa las regiones PWWP y ADD del núcleo catalítico y de un bucle flexible que reconoce sitios CpG. Simulaciones de dinámica molecular, que modelan el movimiento de las proteínas en el tiempo, revelaron que una vez que estas abrazaderas internas se aflojan, el bucle de reconocimiento de CpG se vuelve más móvil y expuesto, mejor posicionado para interaccionar con el ADN. En esencia, DNMT3A cambia de una forma cerrada y en reposo a una forma más abierta y activa solo cuando detecta un entorno de cromatina apropiado.
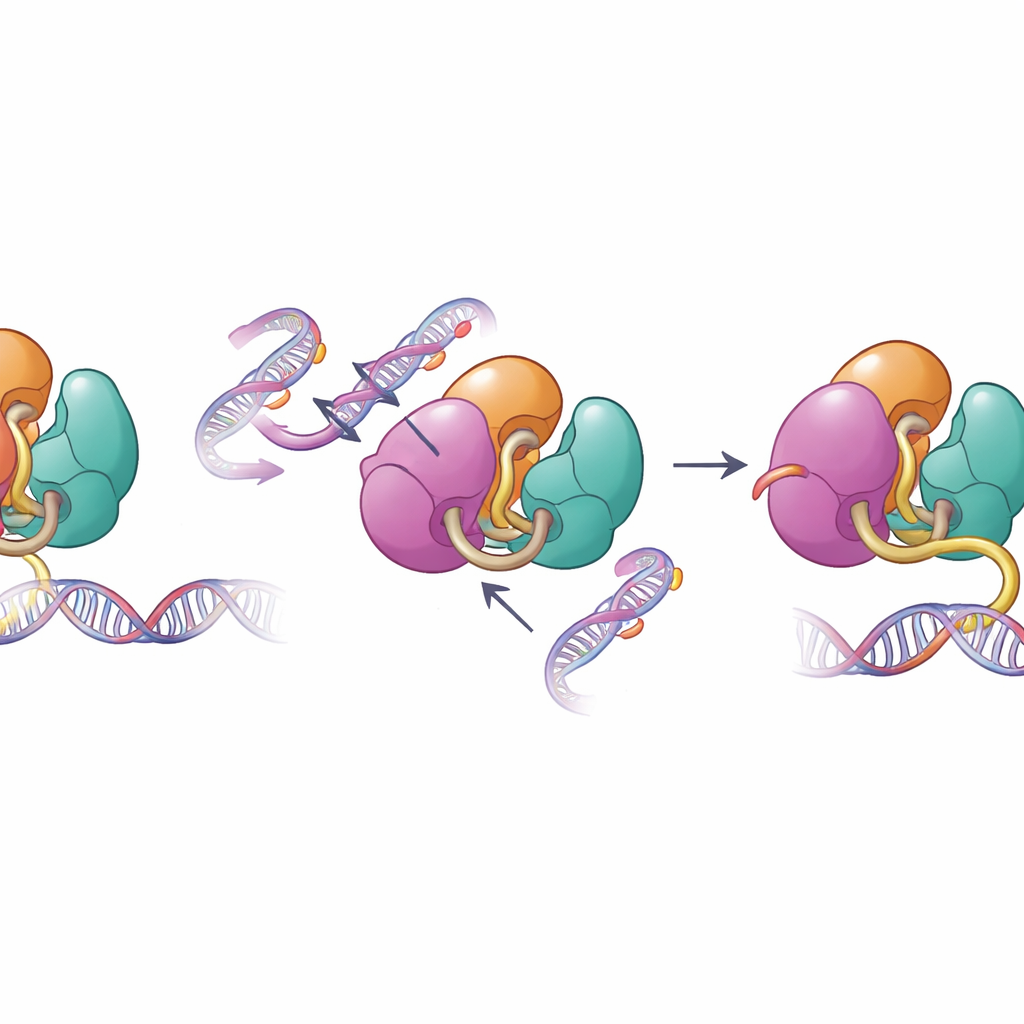
Cuando fallan las salvaguardias estructurales
Las mismas superficies que median la autoinhibición con frecuencia están alteradas en enfermedades humanas. Los autores examinaron cambios vinculados a enfermedades en DNMT3A encontrados en cánceres hematológicos y trastornos del desarrollo, incluidas mutaciones en las regiones PWWP y ADD. Ensayos bioquímicos mostraron que estas mutaciones debilitan los contactos internos que mantienen a DNMT3A bajo control, aumentando su capacidad para unirse al ADN y metilarlo en experimentos de tubo de ensayo. Cuando el equipo analizó los patrones de metilación en células madre de ratón que portaban una de estas mutaciones, encontró que DNMT3A se volvió menos sensible a la señal histona normal H3K36me2 y empezó a metilar tramos del genoma que normalmente permanecerían menos marcados. Esta pérdida de precisión en la localización ayuda a explicar por qué tales mutaciones se asocian con metilación del ADN extensa y mal dirigida en pacientes.
Por qué esto importa para la salud
En conjunto, el estudio revela a DNMT3A como una máquina finamente afinada cuya actividad está gobernada por capas anidadas de autorrestricción, liberadas solo en el contexto de cromatina adecuado. Al mapear exactamente cómo funcionan estos frenos internos —y cómo las mutaciones causantes de enfermedad los inhabilitan— el trabajo proporciona un plano estructural para entender la metilación anómala del ADN en el cáncer y los síndromes del desarrollo. A largo plazo, los conocimientos sobre estos puntos de control podrían guiar esfuerzos para diseñar fármacos que restauren de forma sutil la regulación apropiada de DNMT3A, corrigiendo marcas de ADN aplicadas incorrectamente sin desactivar por completo esta enzima esencial.
Cita: Lu, J., Vig, E., Chen, J. et al. Structural insight into hierarchical DNMT3A autoinhibition and its dysregulation in disease. Nat Commun 17, 2901 (2026). https://doi.org/10.1038/s41467-026-69563-1
Palabras clave: Metilación del ADN, epigenética, DNMT3A, regulación de la cromatina, mutaciones asociadas al cáncer