Clear Sky Science · zh
HECT连接酶HECTD3的结构与机制
细胞如何为蛋白质贴上功能标签
在每个细胞内,有一套微小的信号系统决定哪些蛋白质被修复、回收或重定向以承担新任务。本研究聚焦于运行该系统的一类酶中的一种——称为HECTD3的蛋白。HECTD3与癌症、炎症和病毒感染有关,但其在原子层面上的工作方式一直不清楚。通过结合强大的成像与生化手段,作者揭示了HECTD3的构成、它如何选择分子伙伴,以及它如何在其他蛋白上附加小标签,从而改变这些蛋白的命运。
具有多种功能的细胞标记机器
细胞常用一种叫泛素的小分子修饰蛋白质,类似仓库中不同颜色的标签。不同方式排列的标签链传递不同信息:有些标记蛋白质以便被降解,另一些则调节其活性或定位。被称为E3连接酶的酶类负责挑选哪些蛋白被标记以及如何标记。HECTD3属于E3连接酶的一支,这类酶在将泛素传给底物之前,会与泛素形成临时化学连接。HECTD3在多种癌症中异常活跃,并与程序性细胞死亡、免疫信号传导和病毒复制等过程相关联,但其结构与工作逻辑此前大多未知。
一种持续活跃且构型独特的酶
研究者首先探问HECTD3是否像开关那样可被开启或关闭。许多相关的连接酶通过折叠成自我阻断的构型或通过寡聚体配对来抑制自身。通过生化测试和测量溶液中蛋白质尺寸的技术,团队发现HECTD3主要以单体形式存在,且看起来不会通过自我抑制或稳定聚集来关闭自身。其核心催化片段和全长蛋白均具有活性,并明显偏好与一类负责转移泛素的辅助酶家族协作。这表明HECTD3本质上“随时可用”,在细胞内的调控更可能依赖于除简单自我阻断以外的其他因素。
揭示一种新的蛋白质构架
为了解HECTD3的构造,作者使用低温电子显微镜拍摄了单分子在薄冰中冷冻的影像。他们解析了蛋白单独存在时以及泛素牢固连接到活性位点时的结构。这些快照显示HECTD3呈紧凑形态,而非环形,在一端有经典的双叶催化区,另一端则是此前神秘的N端区域。N端半区形成了两个全新的折叠域,作者命名为D3NA和D3NB,它们排列成一个螺旋平台以支撑一个底物结合的DOC模组。当泛素加载时,催化叶片采用特定的L形构象,且位于活性位点附近的特定酸性残基有助于准备进入的蛋白侧链以接受标签。该工作表明,尽管HECTD3遵循该酶家族的一般规则,但它使用了一套独特的结构元件组合来实现功能。
HECTD3如何标记自身及其底物
接着,团队研究了HECTD3产生何种泛素图案。该酶并非主要构建长的单一类型链,而是主要附加多个单个泛素单元和短链,同时存在一些倾向产生促进蛋白质降解的连接类型的证据。这表明HECTD3更擅长发起标记事件,而不是将其延伸为长的信号链。作者随后转向一个拟议的底物PARP1——一个已知影响癌症治疗反应的DNA修复因子。在体外反应中,HECTD3高效修饰PARP1,在其DNA结合半区的多个赖氨酸位点附加了包含与蛋白移除相关链型的标签。通过化学交联与质谱,他们绘制出HECTD3与PARP1之间的接触点,证实DOC模组与催化区域共同参与将底物定位。将DOC表面两个暴露氨基酸突变会显著降低对PARP1的标记,而不影响核心化学活性,强调它们作为底物识别关键锚点的作用。
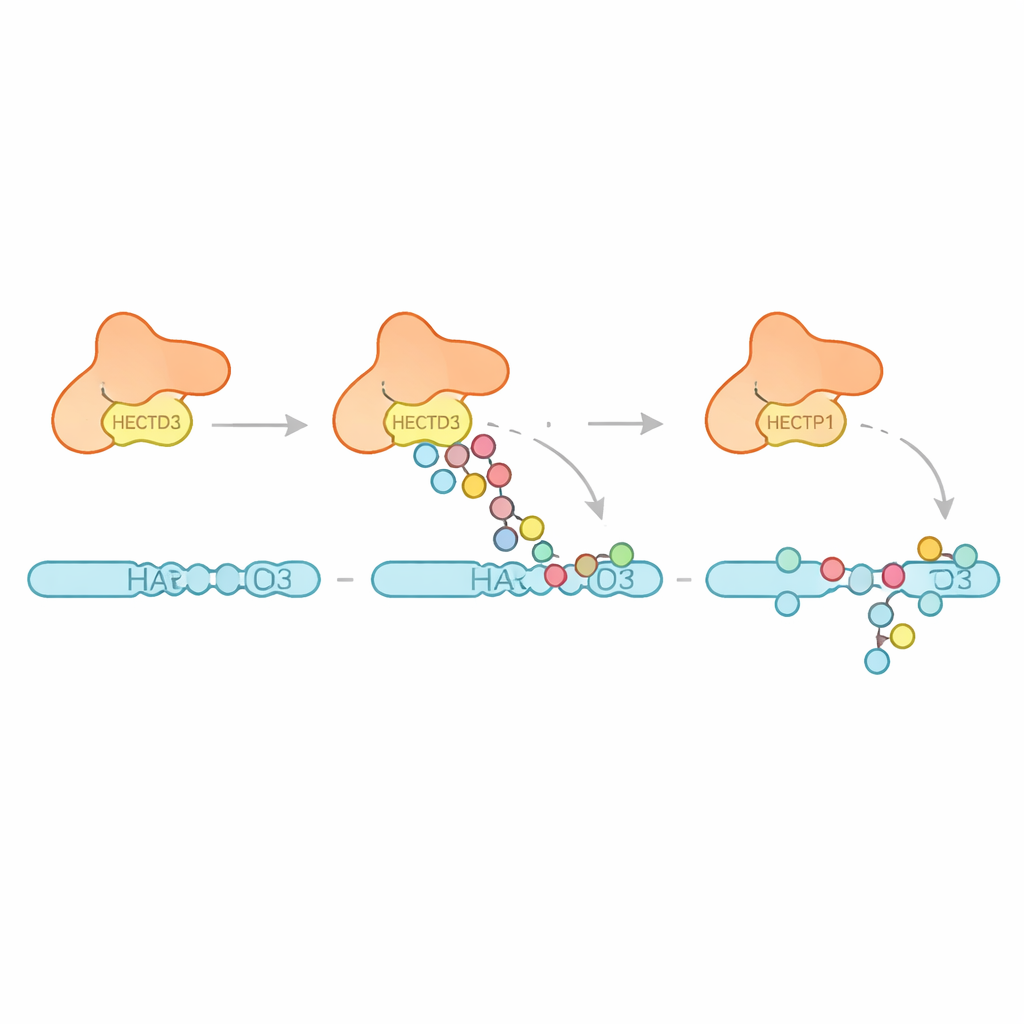
这项工作为何对疾病与治疗重要
总体而言,这些发现将HECTD3描绘为一种持续活跃但结构上复杂的标记机器:它主要负责发起泛素标记,并依赖灵活且独特的N端区域来识别像PARP1这样的特定伙伴。由于HECTD3在多种癌症中活性升高并影响DNA修复蛋白的处理,了解其结构与机制为设计干扰其停靠界面或催化中心的小分子打开了可能性。理论上,这类针对性干预可以改变细胞在癌症、感染和炎症疾病中决定关键蛋白命运的方式。
引用: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
关键词: 泛素连接酶, HECTD3, 蛋白质标记, PARP1, 癌症生物学