Clear Sky Science · pt
Estrutura e mecanismo da ligase HECT HECTD3
Como as Células Marcam Suas Proteínas para Ação
Dentro de cada célula, um pequeno sistema de sinalização decide quais proteínas serão reparadas, recicladas ou redirecionadas para novas funções. Este estudo foca em uma das enzimas que comandam esse sistema, uma proteína chamada HECTD3. HECTD3 tem sido associada ao câncer, à inflamação e à infecção viral, mas seu funcionamento em nível atômico permanecia obscuro. Ao combinar técnicas avançadas de imagem e análises bioquímicas, os autores revelam como HECTD3 é construída, como escolhe seus parceiros moleculares e como adorna outras proteínas com pequenas marcas que podem alterar seu destino.
Uma Máquina Celular de Marcação com Muitos Papéis
As células frequentemente modificam suas proteínas com uma pequena molécula chamada ubiquitina, que pode funcionar como uma etiqueta colorida em um armazém de triagem. Cadeias dessas etiquetas, organizadas de maneiras diferentes, transmitem mensagens distintas: algumas sinalizam uma proteína para degradação, outras ajustam sua atividade ou localização. Enzimas chamadas ligases E3 são responsáveis por escolher quais proteínas são etiquetadas e como. HECTD3 pertence a um ramo das ligases E3 conhecido por formar um elo químico temporário com a ubiquitina antes de transferi‑la ao alvo. Ela está incomumente ativa em vários cânceres e tem sido vinculada a processos como morte celular programada, sinalização imune e replicação viral, contudo sua estrutura e lógica de funcionamento eram em grande parte desconhecidas.
Uma Enzima Constantemente Ativa com Uma Forma Única
Os pesquisadores primeiro sondaram se HECTD3 se comporta como um interruptor que pode ser ligado ou desligado. Muitas ligases relacionadas mantêm‑se sob controle dobrando‑se em formas auto‑bloqueantes ou associando‑se em agregados maiores. Usando testes bioquímicos e uma técnica que mede o tamanho de proteínas em solução, a equipe constatou que HECTD3 existe majoritariamente como uma cópia única e não parece se desligar por auto‑inibição ou por aglomeração estável. Tanto sua seção catalítica central quanto a proteína em comprimento total são ativas, com preferência clara por trabalhar com uma família específica de enzimas auxiliares que transferem a ubiquitina. Isso significa que HECTD3 está essencialmente “pronta para funcionar” e provavelmente é regulada nas células por fatores além de uma simples auto‑inibição.
Revelando Uma Nova Arquitetura Proteica
Para entender como HECTD3 é construída, os autores usaram criomicroscopia eletrônica para capturar imagens de moléculas isoladas congeladas em uma fina camada de gelo. Eles determinaram estruturas da proteína isolada e de um estado no qual uma ubiquitina está firmemente ligada ao seu sítio ativo. Esses instantâneos mostram que HECTD3 é compacta em vez de em forma de anel, com uma clássica região catalítica de dois lóbulos em uma extremidade e uma região N‑terminal previamente misteriosa na outra. A metade N‑terminal revela formar duas dobras inteiramente novas, que os autores denominam D3NA e D3NB, arranjadas como uma plataforma helicoidal que sustenta um módulo DOC de ligação ao substrato. Quando a ubiquitina está carregada, os lóbulos catalíticos adotam uma disposição particular em L, e resíduos ácidos específicos próximos ao sítio ativo ajudam a preparar as cadeias laterais de aminoácidos entrantes para aceitar a marca. O trabalho mostra que, embora HECTD3 siga as regras gerais de sua família enzimática, ela utiliza uma combinação distinta de elementos estruturais para fazê‑lo.
Como HECTD3 Marca a Si Mesma e Seus Alvos
Em seguida, a equipe examinou que tipos de padrões de ubiquitina HECTD3 gera. Em vez de construir longas cadeias de um tipo específico, a enzima principalmete anexa múltiplas unidades simples de ubiquitina e cadeias curtas, com evidências de algumas cadeias que favorecem uma ligação conhecida por promover a degradação proteica. Isso sugere que HECTD3 é mais eficiente em iniciar eventos de marcação do que em alongá‑los em sinais longos. Os autores então se voltaram a uma proteína alvo proposta chamada PARP1, um fator de reparo de DNA já conhecido por influenciar respostas a terapias contra o câncer. Em reações em tubo de ensaio, HECTD3 modificou PARP1 de forma eficiente, decorando vários sítios de lisina em sua metade de ligação ao DNA com marcas que incluem cadeias associadas à remoção de proteínas. Usando entrecruzamento químico e espectrometria de massa, mapearam pontos de contato entre HECTD3 e PARP1, confirmando que tanto o módulo DOC quanto a região catalítica ajudam a posicionar o substrato. A mutação de dois aminoácidos expostos na superfície do DOC reduziu drasticamente a marcação de PARP1 sem prejudicar a química central, destacando‑os como âncoras chave para o reconhecimento do substrato.
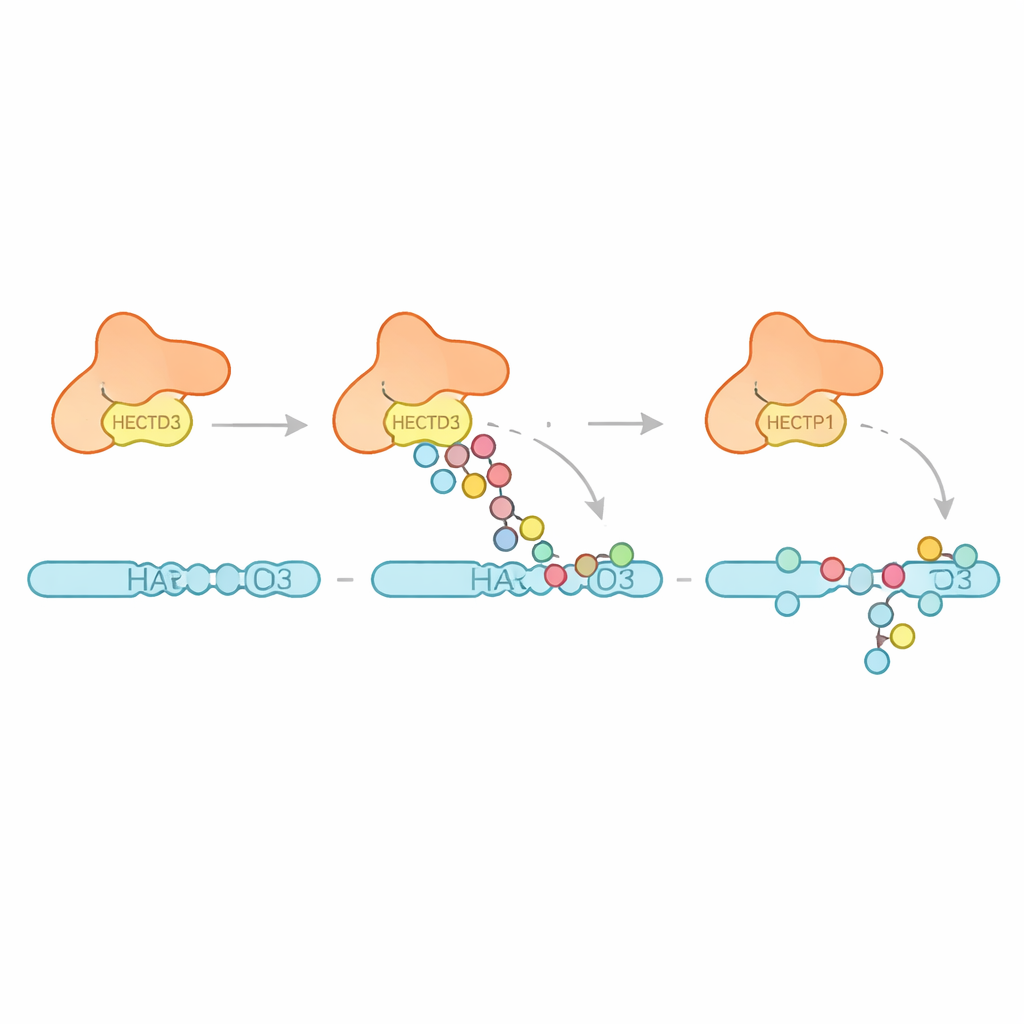
Por Que Isso Importa para Doença e Tratamento
Em conjunto, esses achados pintam HECTD3 como uma máquina de marcação constantemente ativa, mas estruturalmente sofisticada, que principalmente inicia marcas de ubiquitina e depende de uma região N‑terminal flexível e única para reconhecer parceiros específicos como PARP1. Como a atividade de HECTD3 está aumentada em vários cânceres e influencia o modo como proteínas de reparo de DNA são tratadas, entender sua estrutura e mecanismo abre portas para projetar moléculas que interfiram em suas superfícies de ancoragem ou no centro catalítico. Intervenções direcionadas desse tipo poderiam, em princípio, alterar a forma como as células decidem o destino de proteínas críticas em câncer, infecção e doenças inflamatórias.
Citação: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Palavras-chave: ligase de ubiquitina, HECTD3, marcação de proteínas, PARP1, biologia do câncer